Folate receptor 1 is a stemness trait-associated diagnostic and prognostic marker for hepatocellular carcinoma
叶酸受体 1 是肝细胞癌的干性特征相关诊断和预后标志物
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2025 | 起止号: | 2025 Mar 4;13(1):37. |
| doi: | 10.1186/s40364-025-00752-8 | 研究方向: | 免疫、细胞生物学 |
| 疾病类型: | 肝癌 | 细胞类型: | 肿瘤细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Folate receptor 1 is a stemness trait-associated diagnostic and prognostic marker for hepatocellular carcinoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肝细胞癌(HCC)生物标志物研究
原发性肝癌是全球第六大常见恶性肿瘤,预计2025年全球发病率将突破100万例,其中肝细胞癌占比约80%。尽管诊断与治疗技术不断进步,HCC患者的预后仍不理想,根据巴塞罗那临床肝癌(BCLC)分期,A到D期患者的5年生存率分别为54.5%、29.2%、9.8%和4.0%,早期诊断是改善患者预后的关键。近年来,HCC的分子分型研究取得进展,包括Hoshida的3簇分类、Boyault的6簇分类、TCGA的3簇分类等,各分类系统均识别出一类具有干细胞/祖细胞特征的不良预后亚型,这类亚型与染色体不稳定、DNA低甲基化及KRT19、EPCAM、PROM1等干细胞标志物高表达相关,但目前识别该亚型依赖侵入性肿瘤活检,临床应用受限。现有HCC血清生物标志物以甲胎蛋白(AFP)为主,但其敏感性不足,约半数早期HCC患者AFP呈阴性,且无法有效区分侵袭性亚型。因此,亟需开发兼具非侵入性与特异性的生物标志物,用于识别不良预后的HCC亚型并指导临床决策。本研究旨在筛选与HCC干细胞标志物相关的分泌型蛋白,作为侵袭性HCC的循环生物标志物。
2. 文献综述解析
作者在综述部分围绕HCC分子分型的临床价值与非侵入性生物标志物的研究空白展开,首先系统梳理了HCC分子分型的发展脉络,指出分子分型可有效实现HCC患者的预后分层,但现有分型系统依赖肿瘤组织样本,难以在临床常规应用。随后聚焦于干细胞特征相关的不良预后亚型,现有研究已证实这类亚型与HCC侵袭性及耐药性相关,但缺乏可非侵入性识别该亚型的生物标志物。
现有HCC诊断生物标志物中,AFP是应用最广泛的血清标志物,但存在敏感性不足、特异性有限的问题,其水平在肝硬化或肝炎患者中也可能升高,无法精准识别不良预后的干细胞相关亚型。针对这一研究空白,本文创新性地将干细胞标志物与分泌型蛋白筛选相结合,首次发现叶酸受体1(FOLR1)作为干细胞特征相关的循环生物标志物,同时具备HCC诊断效能与早期预后预测价值,弥补了现有生物标志物在识别不良预后亚型方面的局限,为HCC的精准诊疗提供了新的方向。
3. 研究思路总结与详细解析
本研究整体遵循“公共数据库筛选候选标志物→独立队列验证肿瘤标志物预后价值→血清标志物诊断性能验证→血清标志物预后性能及联合评分优化”的闭环逻辑,核心科学问题是寻找可非侵入性识别干细胞相关不良预后HCC亚型的循环生物标志物,最终证实FOLR1兼具诊断与预后双重价值,为HCC的精准诊疗提供新的生物标志物。
3.1 基于公共数据库的候选生物标志物筛选
实验目的是筛选与HCC干细胞标志物正相关且具有预后价值的分泌型蛋白生物标志物。研究人员首先分析了癌症基因组图谱(TCGA)数据库中HCC队列的RNA测序数据,聚焦于KRT19、EPCAM、PROM1三个已被证实与HCC侵袭性及不良预后相关的干细胞标志物,筛选出与三者均呈正相关且在肿瘤组织中显著上调的基因,再通过人类蛋白质图谱数据库筛选其中的分泌型蛋白,最后结合总生存期分析筛选具有预后价值的候选基因。结果显示,共筛选出25个符合条件的分泌型蛋白,其中仅FOLR1在TCGA队列中高表达与不良预后显著相关,且其表达与三个干细胞标志物均呈显著正相关,提示FOLR1可能与HCC的干细胞特征相关。文献未提及具体实验产品,领域常规使用公共数据库分析平台、生物信息学分析软件。
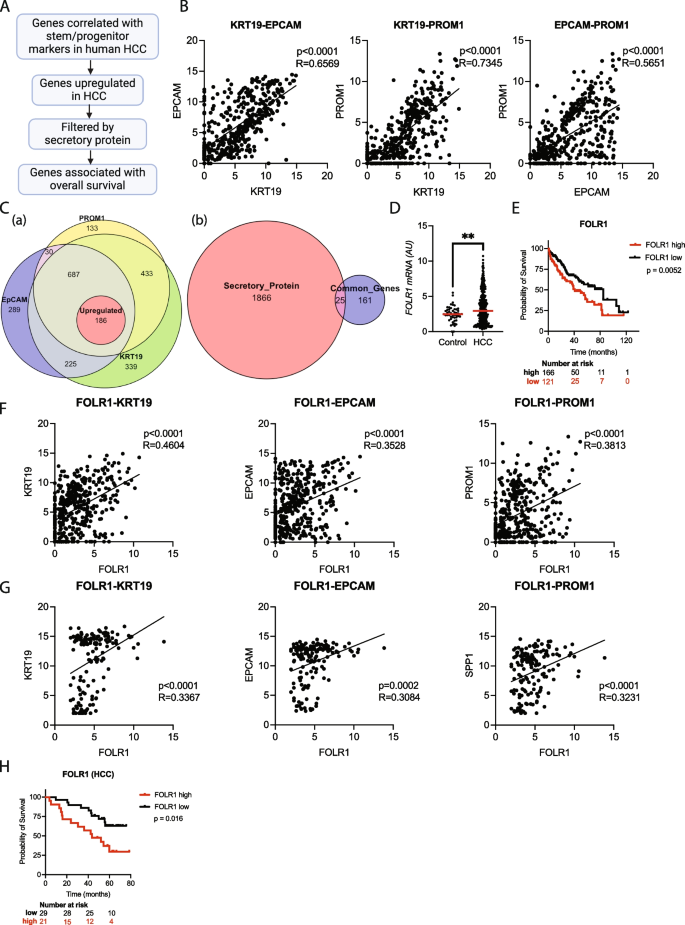
3.2 独立队列验证肿瘤FOLR1的预后价值与分子特征
实验目的是在外部独立队列中验证肿瘤FOLR1与干细胞标志物的关联及预后价值,并解析其相关的分子通路。研究人员利用泰国肝癌基因组与表达研究(TIGER-LC)队列的50例HCC样本RNA测序数据进行验证,同时通过基因集富集分析(GSEA)探索高FOLR1表达组的通路特征。结果显示,在TIGER-LC队列中,FOLR1表达与三个干细胞标志物仍呈显著正相关,高FOLR1表达患者的总生存期显著短于低表达患者(n=50,P<0.05);分子通路分析显示,高FOLR1表达组中p53、DNA修复、MYC、E2F、PI3K/AKT/mTOR等致癌通路显著激活,且FOLR1高表达与多个分类系统中的不良预后亚型相关,进一步证实FOLR1与HCC的侵袭性干细胞特征相关。文献未提及具体实验产品,领域常规使用基因集富集分析工具、生存分析软件。
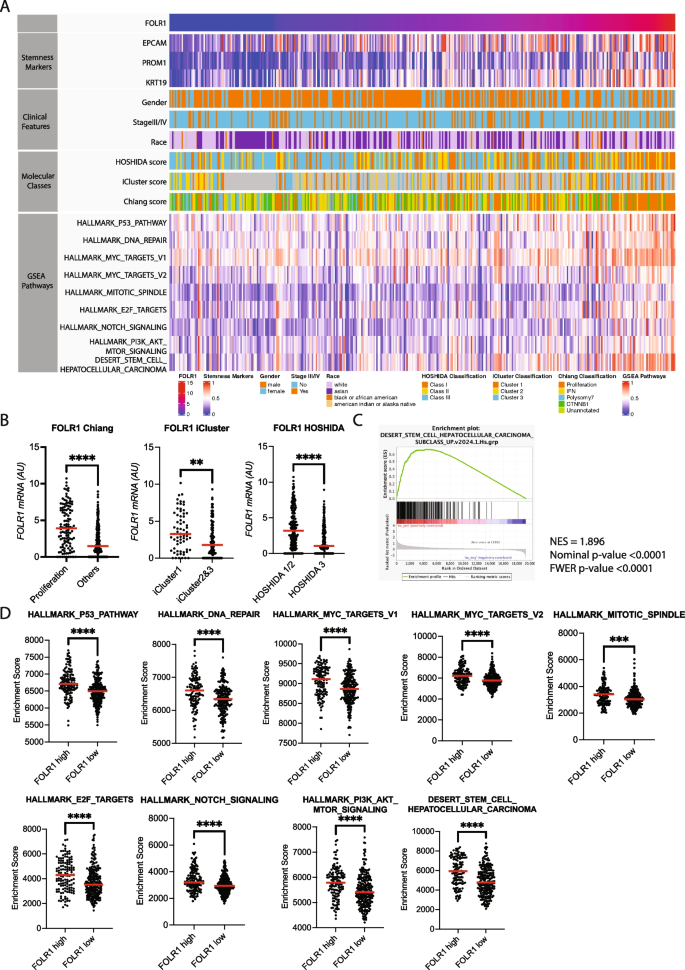
3.3 血清FOLR1的HCC诊断性能验证
实验目的是验证血清FOLR1与肿瘤组织FOLR1表达的相关性,并评估其作为HCC诊断标志物的效能,以及联合AFP的诊断价值。研究人员收集了238例慢性肝病患者和247例HCC患者的血清样本,采用酶联免疫吸附试验(ELISA)检测血清FOLR1水平,同时分析32例手术切除HCC患者的肿瘤组织FOLR1表达与血清水平的相关性,通过受试者工作特征(ROC)曲线评估诊断效能。结果显示,血清FOLR1水平与肿瘤组织FOLR1表达呈显著正相关;HCC患者的血清FOLR1水平显著高于慢性肝病患者(n=485,P<0.0001);血清FOLR1诊断HCC的ROC曲线下面积(AUROC)为0.685,与AFP的AUROC(0.708)相当,两者联合后AUROC提升至0.764(P=0.019),显著提高了诊断准确性。实验所用关键产品:R&D Systems的Human FOLR1 ELISA Kit(货号DFLR10)、Qiagen的RNeasy Mini Kit、Toyobo的ReverTra Ace qPCR RT Kit和THUNDERBIRD Probe qPCR Mix、Thermo Fisher Scientific的QuantStudio 7 Real-Time PCR System。
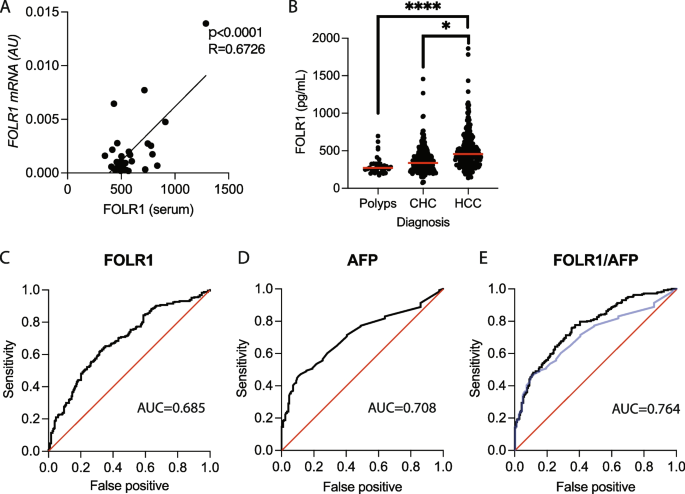
3.4 血清FOLR1的HCC预后性能及联合GALAD评分的价值
实验目的是评估血清FOLR1作为HCC预后标志物的价值,尤其是在早期患者中的效能,并探索其与GALAD评分联合的预后分层能力。研究人员对247例HCC患者进行了生存分析,按血清FOLR1水平分组后比较总生存期,同时进行分层分析(治疗方式、肿瘤分期)和多因素Cox比例风险回归分析,进一步验证FOLR1与GALAD评分联合的预后价值。结果显示,高血清FOLR1水平患者的总生存期显著短于低水平患者(n=247,P<0.0001),且这一差异不受治疗方式(射频消融、经动脉化疗栓塞、手术)影响;在早期HCC患者(1、2期)中,高FOLR1水平仍与不良预后显著相关;多因素分析显示,血清FOLR1水平和GALAD评分是HCC不良预后的独立预测因子,两者联合可将患者进一步分为低危、中危、高危三组,显著提升预后分层能力。实验所用关键产品:R&D Systems的Human FOLR1 ELISA Kit(货号DFLR10)。
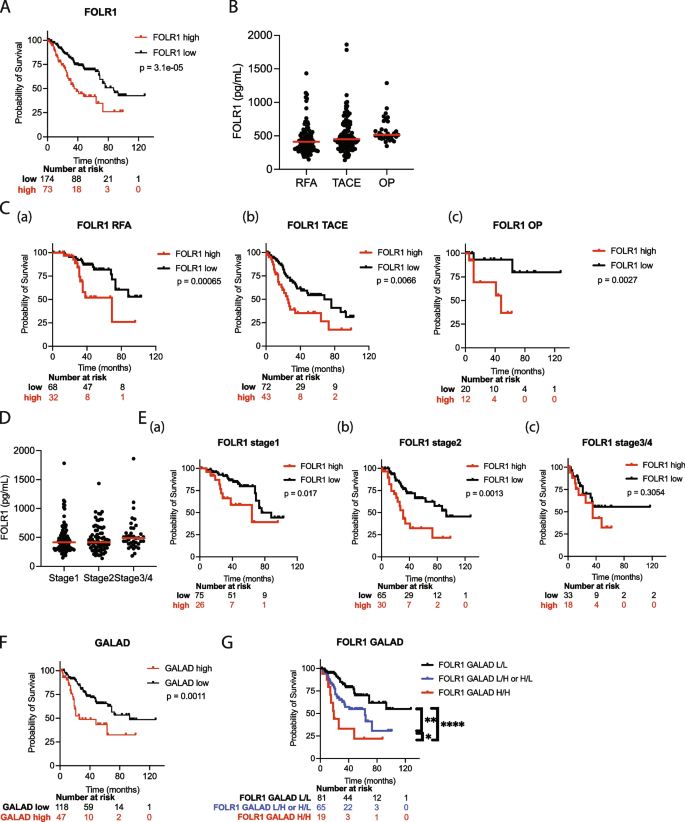
4. Biomarker研究及发现成果解析
本研究聚焦的生物标志物为叶酸受体1(FOLR1),包括肿瘤组织FOLR1与血清FOLR1,属于分泌型蛋白类生物标志物,筛选与验证逻辑为“公共数据库关联干细胞标志物→独立队列验证肿瘤标志物预后价值→临床样本验证血清标志物诊断与预后价值”,形成了完整的生物标志物开发链条。
研究过程中,肿瘤组织FOLR1的来源为TCGA和TIGER-LC队列的HCC手术样本,通过定量实时聚合酶链反应(qRT-PCR)检测表达水平;血清FOLR1的来源为247例HCC患者和238例慢性肝病患者的外周血样本,通过ELISA检测水平。验证结果显示,血清FOLR1诊断HCC的AUROC为0.685,最佳阈值为409.45 pg/mL,对应敏感性61.5%、特异性68.5%;在预后方面,高血清FOLR1水平患者的总生存期显著缩短,多因素分析证实其为独立预后因素,尤其是在早期HCC患者中具有重要的预后预测价值。
核心成果方面,FOLR1是首个被证实与HCC干细胞特征相关的循环生物标志物,其血清水平不仅可辅助HCC诊断,联合AFP可提升诊断准确性,还可作为早期HCC的独立预后指标,与GALAD评分联合可进一步优化预后分层。本研究的创新性在于首次揭示了FOLR1在HCC中的诊断与预后价值,为非侵入性识别不良预后的干细胞相关HCC亚型提供了新的生物标志物,有望推动HCC的精准分层诊疗,同时为后续探索FOLR1在HCC干细胞调控中的功能机制奠定了基础。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。