RBM10对环状RNA生物合成的调控有助于其在肺腺癌中发挥抑癌作用
RBM10 modulation of circRNA biogenesis contributes to its tumor suppressor role in lung adenocarcinoma
1. 领域背景与文献
文献英文标题:RBM10 exerts tumor-suppressive functions via circRNA regulation and highlights circHIPK3 as a promising biomarker and potential therapeutic target in RBM10-deficient LUAD;发表期刊:Journal of Experimental & Clinical Cancer Research;影响因子:未公开;研究领域:肺腺癌分子调控与肿瘤生物标志物研究。
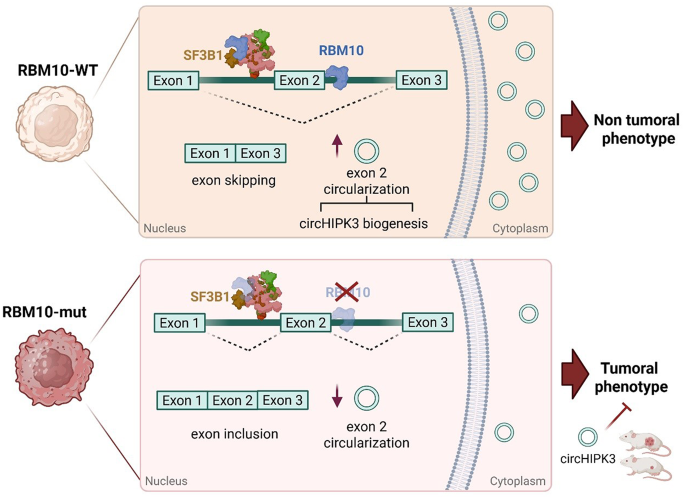
肺腺癌是全球癌症死亡的首要原因,领域共识显示约7%的肺腺癌患者存在RNA结合基序蛋白10(RBM10)的功能缺失突变,该蛋白作为剪接调控因子参与RNA加工过程,其抑癌功能受损是肺腺癌发生发展的重要驱动因素之一。近年来环状RNA(circRNA)作为稳定的非编码RNA,其失调广泛参与癌症进程,但RBM10是否参与环状RNA的生物发生调控此前尚未被阐明,领域内也缺乏RBM10突变型肺腺癌的特异性生物标志物与靶向干预靶点,本研究正是针对这一研究空白展开,旨在揭示RBM10调控环状RNA生成的分子机制,挖掘相关临床转化价值。
2. 文献综述解析
本研究的文献综述按分子类型对领域现有研究进行分类梳理,分别围绕RBM10的功能、环状RNA的调控机制两类核心内容展开评述。
现有研究已证实RBM10作为RNA结合蛋白参与可变剪接过程,其功能缺失突变是肺腺癌的明确驱动事件,技术层面已实现RBM10的功能敲除与回补模型构建,可稳定用于分子调控机制研究,但现有研究仅聚焦于RBM10对信使RNA的剪接调控作用,未涉及非编码RNA尤其是环状RNA的调控环节。针对环状RNA的研究显示,环状RNA由反向剪接生成,大多作为微小RNA海绵发挥基因调控作用,其失调广泛存在于各类癌症中,已有研究证实部分RNA结合蛋白可通过结合环状RNA的内含子侧翼序列调控其生成,但该调控模式是否适用于RBM10尚未被验证,且RBM10相关的环状RNA在肺腺癌中的临床价值也缺乏队列数据支持。本研究的创新价值在于首次揭示了RBM10调控环状RNA生物发生的位置依赖机制,明确了circHIPK3作为RBM10突变型肺腺癌的生物标志物与治疗靶点的潜力,填补了领域内的研究空白。
3. 研究思路总结与详细解析
本研究的核心研究目标是明确RBM10对环状RNA的调控作用及分子机制,验证相关环状RNA在肺腺癌中的功能与临床价值,核心科学问题为RBM10如何调控环状RNA生成、该调控通路如何介导RBM10的抑癌功能,整体技术路线遵循“调控靶点筛选→分子机制验证→功能表型验证→临床队列验证→上游调控轴解析”的逻辑闭环。
3.1 RBM10调控的环状RNA筛选与验证
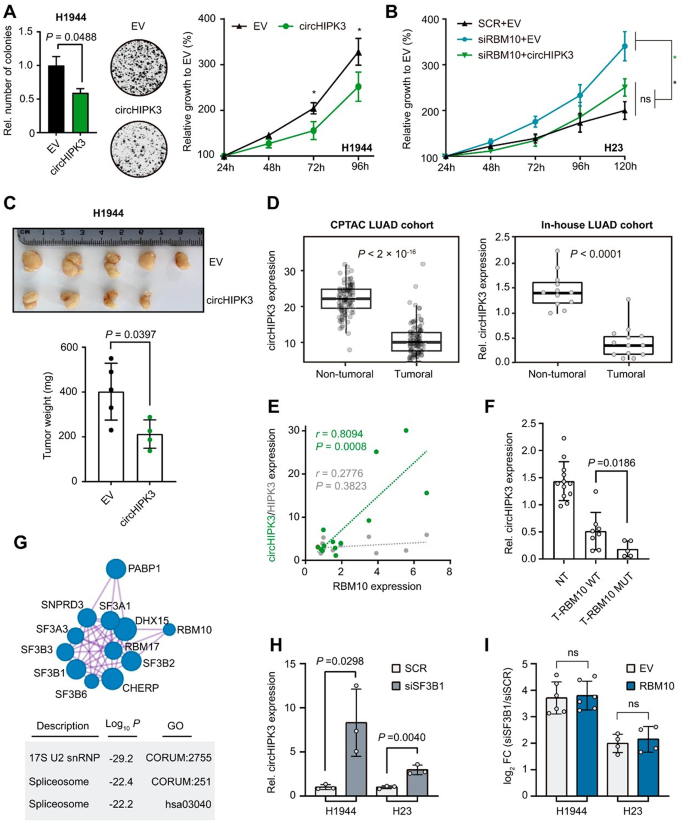
本环节核心目标为筛选并验证RBM10调控的环状RNA分子。实验采用RBM10功能缺失突变的NCIH1944细胞系,回补主流RBM10亚型2后进行总RNA测序,对测序筛选到的差异表达环状RNA采用逆转录定量PCR(RT-qPCR)结合核糖核酸酶R(RNase R)消化、收敛/发散引物验证特异性,同时在NCIH1944、NCIH2291两种回补模型及NCIH23敲低模型中验证RBM10对候选环状RNA的调控作用。实验结果显示测序共检测到656个环状RNA,其中99个在RBM10回补后下调(倍数变化≤0.8)、79个上调(倍数变化≥1.2),逆转录定量PCR验证最终确认circSMARCA5、circCYP24A1、circHIPK3的表达明确依赖于RBM10,统计学差异P均<0.05。文献未提及具体实验产品,领域常规使用总RNA提取试剂、环状RNA特异性PCR引物、核糖核酸酶R、逆转录定量PCR试剂盒等试剂。

3.2 RBM10调控环状RNA生成的分子机制验证
本环节核心目标为明确RBM10调控环状RNA生物发生的分子机制。实验采用亚细胞组分分离实验检测RBM10与候选环状RNA的细胞定位,采用光活化核糖核苷增强的交联免疫沉淀(PAR-CLIP)、RNA pull-down实验验证RBM10与环状RNA内含子侧翼序列的直接结合,利用剪接报告系统验证RBM10结合位置对可变剪接及环状RNA生成的影响,同时构建RBM10 RNA结合域点突变体验证结合功能的必要性。实验结果显示亚细胞分离实验显示RBM10仅定位于细胞核,环状RNA主要富集于细胞质,提示RBM10在细胞核层面调控环状RNA的生成;光活化核糖核苷增强的交联免疫沉淀与RNA pull-down实验证实RBM10可直接结合circHIPK3的3"侧翼序列及circSMARCA5的5"侧翼序列;剪接报告实验显示RBM10结合3"侧翼序列相比结合5"侧翼序列可提升约3倍的外显子跳读效率,从而促进环状RNA环化;RRM2结构域R343G突变、ZnF2结构域S781L突变均会显著削弱RBM10对circHIPK3、circSMARCA5的调控作用,且R343G突变严重破坏外显子跳读过程。文献未提及具体实验产品,领域常规使用亚细胞组分分离试剂盒、光活化核糖核苷增强的交联免疫沉淀试剂盒、生物素标记RNA探针、剪接报告质粒、定点突变试剂盒等试剂。
3.3 环状RNA的功能表型验证
本环节核心目标为验证RBM10调控的环状RNA的肿瘤相关功能。实验在NCIH1944、NCIH2291细胞中过表达circHIPK3、敲低circSMARCA5,检测细胞克隆形成能力与细胞活力;在RBM10敲低的NCIH23细胞中进行circHIPK3过表达或circSMARCA5敲低的回补实验,验证表型拯救效果;构建裸鼠异种移植瘤模型验证circHIPK3的体内抑癌功能。实验结果显示circHIPK3过表达与circSMARCA5敲低均能显著降低肺腺癌细胞的克隆形成能力与细胞活力,表型与RBM10回补一致;过表达circHIPK3或敲低circSMARCA5均可拯救RBM10缺失导致的促肿瘤表型;体内异种移植实验显示circHIPK3过表达可使肿瘤重量降低超过50%(文献未明确提供该实验样本量数据,P<0.05),而circSMARCA5敲低无显著体内效应。文献未提及具体实验产品,领域常规使用环状RNA过表达载体、小干扰RNA、细胞活力检测试剂、裸鼠异种移植相关实验试剂等。
3.4 临床队列验证与上游调控轴解析
本环节核心目标为验证circHIPK3的临床相关性及RBM10调控环状RNA生成的上游分子机制。实验分析CPTAC公共肺腺癌队列及70例样本的自建肺腺癌队列中circHIPK3的表达水平,分析其与RBM10表达、RBM10突变状态的相关性;通过免疫共沉淀(Co-IP)联合质谱分析筛选RBM10的互作蛋白,采用剪接因子敲低与回补实验验证调控轴的上下游关系。实验结果显示CPTAC队列与自建队列均显示circHIPK3在肺腺癌组织中显著下调,自建队列中13对配对样本(n=13)的分析结果与CPTAC公共队列趋势一致;circHIPK3表达与RBM10表达呈显著正相关(Pearson相关系数有统计学意义,P<0.05),且在RBM10突变的肿瘤组织中下调更为明显;质谱分析显示RBM10可与剪接体核心蛋白SF3B1等U2复合物蛋白互作,SF3B1敲低后circHIPK3表达显著上调,且SF3B1敲低后回补RBM10无法进一步提升circHIPK3的表达,证实SF3B1在该调控通路中位于RBM10的上游。文献未提及具体实验产品,领域常规使用组织RNA提取试剂、免疫共沉淀试剂盒、质谱检测试剂、小干扰RNA等试剂。
4. Biomarker研究及发现成果
本研究明确circHIPK3为肺腺癌的潜在生物标志物,筛选验证逻辑遵循“细胞系筛选→功能验证→临床双队列验证”的完整链条。
circHIPK3属于环状RNA类生物标志物,其检测样本为肺腺癌组织及对应癌旁组织,验证方法为环状RNA特异性逆转录定量PCR。临床队列数据显示,circHIPK3在肺腺癌组织中显著下调,自建队列中13对配对样本(n=13)的分析结果与CPTAC公共队列趋势一致;circHIPK3表达与RBM10表达呈显著正相关,且在RBM10突变的肿瘤组织中下调幅度更大,特异性针对RBM10缺陷型肺腺癌亚群。核心成果显示circHIPK3具有明确的抑癌功能,过表达circHIPK3可使体内异种移植瘤重量下降超过50%(P<0.05),首次明确了RBM10-SF3B1轴对circHIPK3的调控机制,提示circHIPK3可作为RBM10突变型肺腺癌的诊断与预后标志物,同时也是潜在的治疗靶点。文献未提供circHIPK3诊断的受试者工作特征曲线、敏感性与特异性具体数据。
推测:circHIPK3可进一步开发为RNA治疗药物,用于RBM10突变型肺腺癌的靶向干预,后续需扩大临床样本量验证其诊断效能。