利用增强型单次读取分析解码人类tRNA修饰和串扰
Decoding human tRNA modifications and crosstalk by enhanced single-read analysis
1. 领域背景与文献
文献英文标题:Decoding human tRNA modifications and crosstalk by enhanced single-read analysis;发表期刊:Genome Biology;影响因子:未公开;研究领域:RNA修饰与转运RNA功能基因组学。
领域共识:人类转运RNA(tRNA)组包含约40种修饰类型,胞质转运RNA平均携带13个修饰位点,线粒体转运RNA平均携带6个修饰位点,这些修饰的动态变化具有细胞类型与细胞状态依赖性,是调控翻译效率、保真性及细胞应激响应的重要表观转录组机制。近年来随着高通量测序技术的发展,转运RNA修饰的单碱基分辨率检测技术不断涌现,研究热点集中于新修饰的鉴定、修饰催化酶的功能解析及修饰与疾病的关联分析。但现有技术存在明显局限性:多数方法仅能单次检测1-2种修饰类型,无法实现同一转运RNA分子上多个修饰位点的并行分析,也难以关联修饰状态与转运RNA的氨酰化水平、翻译过程中的核糖体结合状态等功能属性,导致领域内对转运RNA修饰组的协同调控网络及功能机制的解析严重不足。
本研究针对这一核心未解决问题,开发了整合多重小RNA测序与化学修饰检测、单读长互作分析的技术平台增强型单读长互作分析(eSLAC),实现了人类转运RNA组超过60%修饰位点的覆盖,首次在单分子层面解析了转运RNA修饰间的互作模式及修饰与翻译功能的关联,为转运RNA修饰组的系统研究提供了新的技术范式。
2. 文献综述解析
作者按照转运RNA功能属性分类、修饰检测技术发展脉络的逻辑对现有研究进行系统评述。首先梳理了转运RNA的四大核心功能属性(丰度、氨酰化、修饰、片段化)的研究进展,明确转运RNA修饰可通过调控转运RNA稳定性、解码效率与保真性,实现对蛋白质合成过程的精细调控,且修饰的异常与多种人类疾病的发生发展密切相关。其次,作者对现有转运RNA测序及修饰检测技术进行分类总结:传统小分子RNA测序方法受转运RNA高度结构化、修饰丰富的影响,检测覆盖度低且难以区分修饰位点;基于逆转录的修饰检测技术多依赖单种修饰的特征信号(如逆转录终止、碱基突变),仅能针对特定修饰进行分析;基于基因敲除的功能研究多聚焦于单一修饰的生理功能,无法解析修饰间的协同调控关系。
现有研究的优势在于,已建立了如模拟转运RNA测序、去甲基化酶辅助转运RNA测序等可检测部分沃森-克里克碱基配对面甲基化修饰的测序方法,且针对丰度较高的假尿苷(Ψ)开发了亚硫酸氢盐诱导缺失测序等单碱基分辨率检测技术,为转运RNA修饰的系统研究奠定了基础。局限性在于,现有技术均无法实现同一条转运RNA分子上多种修饰的同时检测,也无法关联修饰状态与转运RNA的氨酰化水平、核糖体结合状态等功能属性,限制了对转运RNA修饰调控网络的系统解析。
本研究的创新价值在于,首次将多重小RNA测序(MSR-seq)与多种修饰的化学处理检测方法结合,同时开发了适配的单读长分析流程,不仅实现了人类转运RNA组超过60%修饰位点的覆盖,还可在单分子层面分析修饰间互作、修饰与氨酰化的关联,填补了领域内缺乏多维度转运RNA修饰组分析工具的空白,为转运RNA修饰的功能机制研究提供了全新的技术路径。
3. 研究思路总结与详细解析
本研究的核心目标是开发可同时解析人类转运RNA多类修饰、修饰互作及功能状态的整合分析平台,核心科学问题包括如何实现多种转运RNA修饰的并行单碱基检测、转运RNA修饰间的协同调控模式是什么、转运RNA修饰状态如何影响其翻译相关功能。技术路线遵循“技术开发→方法验证→机制解析→功能关联”的闭环逻辑:首先对已有的多重小RNA测序技术进行化学处理扩展,实现假尿苷、5-甲酰基胞苷(f⁵C)、N4-乙酰胞苷(ac⁴C)等修饰的检测;其次通过假尿苷合成酶敲除细胞系验证修饰检测的准确性,绘制人类转运RNA修饰图谱;随后开发增强型单读长互作分析算法,解析修饰间、修饰与氨酰化的互作模式;最后通过多聚核糖体转运RNA谱分析,关联修饰状态与转运RNA在翻译过程中的功能。
3.1 转运RNA修饰检测技术的开发与验证
实验目的:建立可同时检测多种转运RNA修饰的高通量测序方法,实现假尿苷的单碱基分辨率检测并验证其催化酶的底物特异性。
方法细节:在已有的多重小RNA测序流程中引入亚硫酸氢盐处理,使假尿苷转化为无碱基位点,逆转录时产生缺失信号用于修饰检测。实验采用人胚肾293T(HEK293T)细胞系,通过成簇规律间隔短回文重复序列相关核酸酶9(CRISPR-Cas9)构建假尿苷合成酶1(PUS1)、假尿苷合成酶7(PUS7)、TruB同源假尿苷合成酶1(TRUB1)三种假尿苷合成酶的敲除细胞系,通过免疫印迹验证敲除效率。
结果解读:免疫印迹结果显示三种合成酶的敲除效率符合实验要求(对应图1e)。亚硫酸氢盐处理可特异性检测转运RNA上的假尿苷位点,如胞质天冬氨酸转运RNA(GUC)-2的假尿苷13、假尿苷55位点,线粒体精氨酸转运RNA的假尿苷29、假尿苷36位点均显示出显著的处理依赖性缺失信号(对应图1c、1d)。通过敲除细胞系验证,明确了假尿苷合成酶1负责催化胞质转运RNA 5’反密码子茎区及线粒体转运RNA的假尿苷位点,敲除后该区域假尿苷的缺失率平均超过80%(n=28,P<10^-4);假尿苷合成酶7负责催化D茎区假尿苷13及酪氨酸转运RNA的假尿苷35位点,敲除后该类位点缺失率接近100%(n=21,P<10^-4);TruB同源假尿苷合成酶1负责催化T环区假尿苷54-55位点,敲除后胞质转运RNA该区域假尿苷缺失率约30%,线粒体转运RNA该区域缺失率接近100%(n=55,P<10^-3)(对应图1f-h)。此外还发现假尿苷合成酶7可催化D环区假尿苷20c及T茎区假尿苷50等未被充分表征的位点(对应图1i-j)。
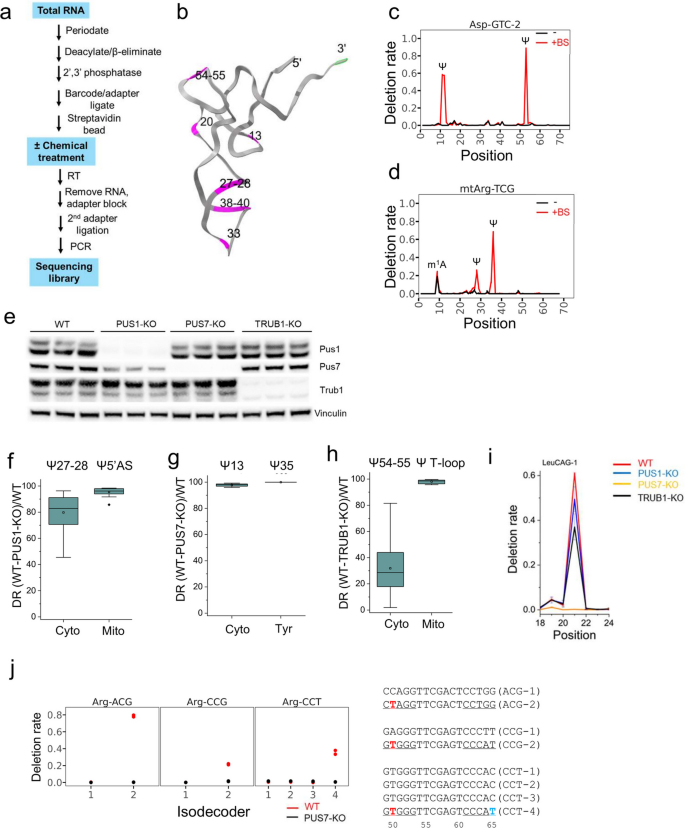
产品关联:文献未提及具体实验产品,领域常规使用成簇规律间隔短回文重复序列相关核酸酶9基因编辑试剂、RNA亚硫酸氢盐转化试剂盒、高通量测序文库构建试剂、特异性抗体验证试剂。
3.2 5-甲酰基胞苷与N4-乙酰胞苷修饰的检测及人类转运RNA修饰图谱构建
实验目的:扩展检测修饰类型,绘制人类胞质及线粒体转运RNA的修饰位点全景图。
方法细节:在多重小RNA测序流程中引入氰基硼氢化钠(NaCNBH₃)处理,使5-甲酰基胞苷和N4-乙酰胞苷产生C-T突变信号用于检测,结合已有的多重小RNA测序可检测的N1-甲基腺苷(m¹A)、N3-甲基胞苷(m³C)、N1-甲基鸟苷(m¹G)、N2,N2-二甲基鸟苷(m²₂G)、Q核苷(queuosine)、2-硫尿苷(s²U)等修饰信号,整合构建人类转运RNA修饰图谱。
结果解读:氰基硼氢化钠处理可特异性检测线粒体甲硫氨酸转运RNA的5-甲酰基胞苷34位点、胞质亮氨酸转运RNA(CAA)的5-甲酰基胞苷34位点,以及II型转运RNA(亮氨酸转运RNA、丝氨酸转运RNA)D茎区的N4-乙酰胞苷12位点,这些位点均显示出处理依赖性的C-T突变信号(对应图2b-e)。整合所有可检测的修饰信号,共鉴定到胞质转运RNA上374个修饰位点,覆盖约64%的预期修饰位点;线粒体转运RNA上84个修饰位点,覆盖约68%的已报道修饰位点(对应图3a、3c),其中N7-甲基鸟苷(m⁷G)也可通过亚硫酸氢盐处理产生的缺失信号被检测到(对应图3b)。
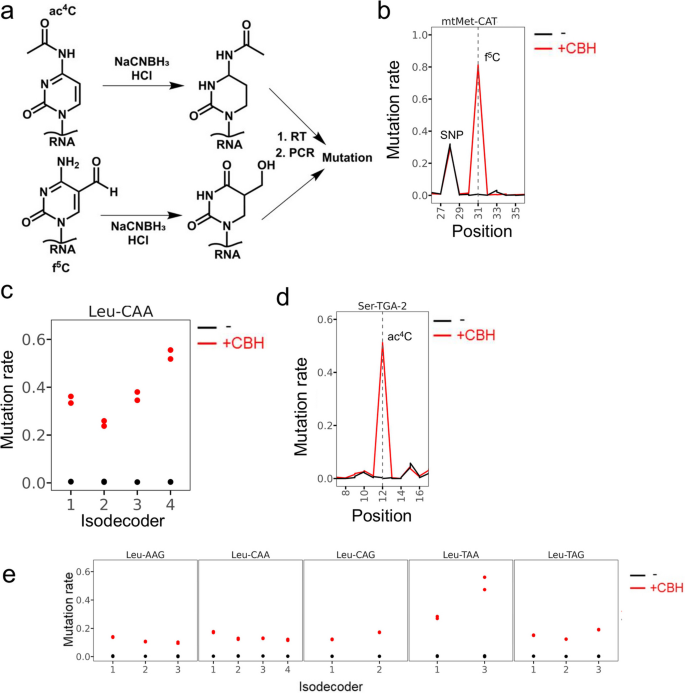
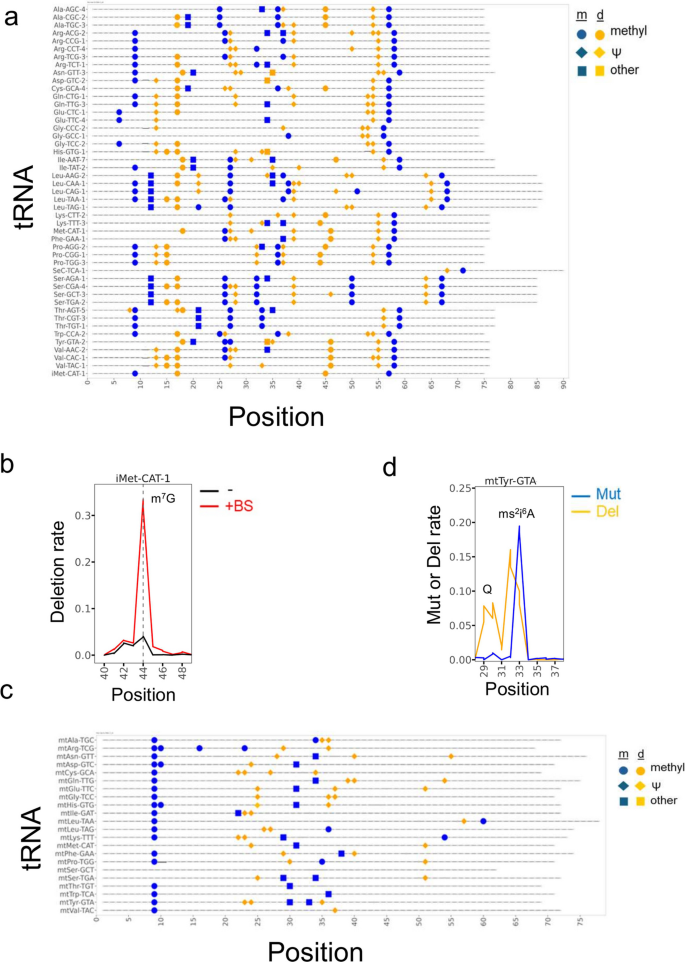
产品关联:文献未提及具体实验产品,领域常规使用化学试剂氰基硼氢化钠、高通量测序及数据分析相关试剂。
3.3 增强型单读长互作分析平台的开发与修饰互作解析
实验目的:建立单分子层面的转运RNA修饰互作分析方法,解析假尿苷修饰间、假尿苷与氨酰化的互作模式。
方法细节:在已有的单读长互作分析流程基础上扩展缺失信号分析能力,形成增强型单读长互作分析平台,通过单读长上两个修饰位点的信号共现频率计算比值比(OR),评估互作强度:比值比>1为正互作(协同存在),比值比<1为负互作(互斥存在)。分别在野生型及三种假尿苷合成酶敲除细胞系中验证互作模式的可靠性。
结果解读:全局分析显示假尿苷修饰间普遍存在正互作,其中T环区假尿苷55与其他区域的假尿苷位点(3’反密码子茎环区假尿苷38-40、5’反密码子茎区假尿苷27-28、D茎区假尿苷13等)均呈现显著正互作(log₂(比值比)>0,P<0.05)(对应图4b),其他区域的假尿苷位点间也以正互作为主(对应图4c)。敲除单一假尿苷合成酶会同时降低其他合成酶催化位点的假尿苷修饰水平,如TruB同源假尿苷合成酶1敲除会显著降低假尿苷27-28的修饰水平(对应图4d-e),验证了正互作的存在。推测:这种协同调控可能由La核糖核蛋白结构域家族成员3(LARP3)介导的多合成酶复合物实现。此外,假尿苷修饰与转运RNA氨酰化水平整体呈正相关,其中假尿苷38-40、假尿苷55等位点的正互作最为显著,而假尿苷27-28位点与氨酰化无显著关联,这与氨酰-转运RNA合成酶的识别元件分布一致(对应图4g)。
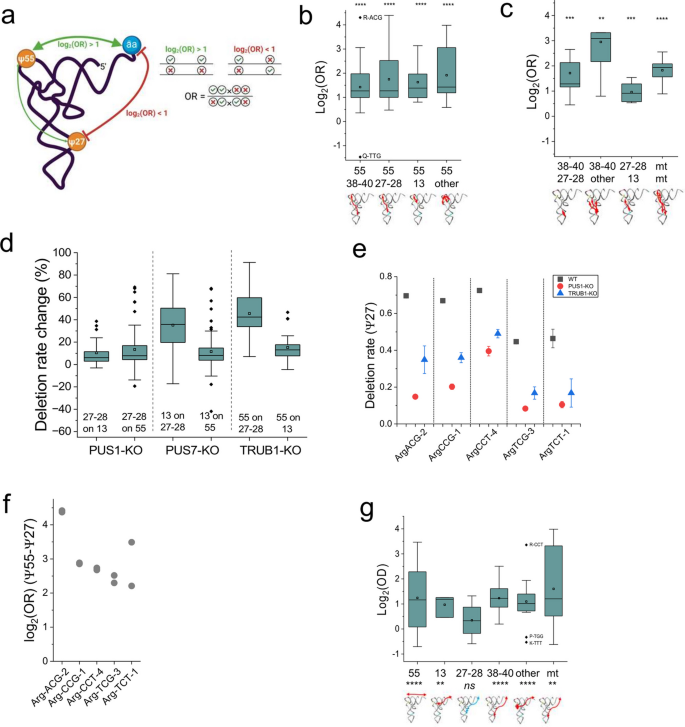
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析工具及相关计算资源。
3.4 多聚核糖体转运RNA谱分析修饰的翻译相关功能
实验目的:关联转运RNA修饰状态与翻译过程中的功能状态,解析修饰对转运RNA核糖体结合的影响。
方法细节:采用蔗糖密度梯度离心分离人胚肾293T细胞的多聚核糖体组分,提取结合的转运RNA进行多重小RNA测序分析,通过转运RNA 3’末端特征区分结合于核糖体A/P位点(3’CCA末端,带电)和E位点(3’CC末端,不带电)的转运RNA,比较不同位点的修饰水平差异。
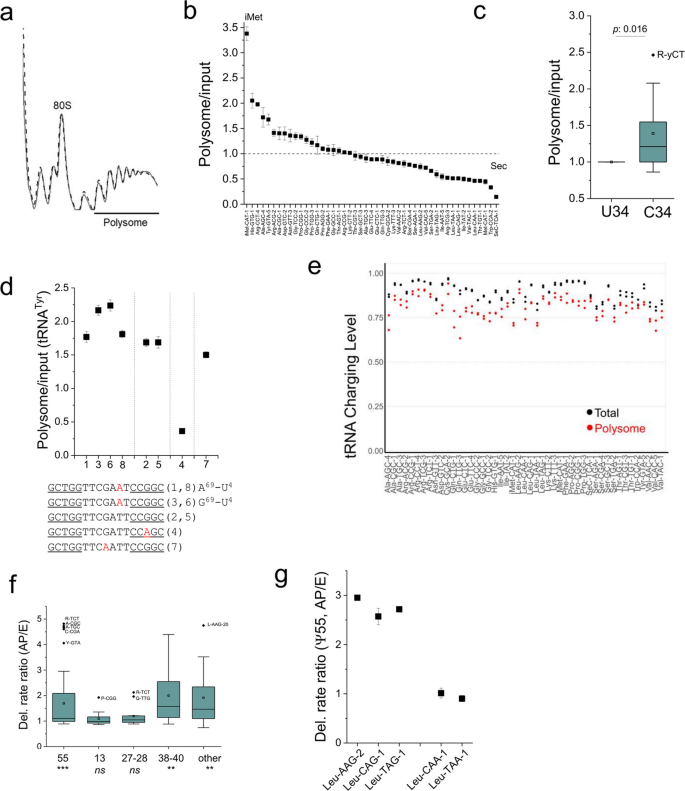
结果解读:多聚体中转运RNA的丰度分布呈现显著偏好性,起始甲硫氨酸转运RNA显著富集,而硒代半胱氨酸转运RNA显著缺失; wobble位为胞嘧啶34的转运RNA异构体整体比尿嘧啶34的异构体更富集于多聚体(对应图5b-c)。转运RNA异构体的核糖体结合效率存在差异,如酪氨酸转运RNA的不同异构体仅因单核苷酸差异就呈现出显著的结合丰度差异(对应图5d)。比较A/P位点与E位点的转运RNA修饰水平发现,假尿苷55、假尿苷38-40及可变环区假尿苷位点在A/P位点的水平显著高于E位点,而假尿苷13、假尿苷27-28无显著差异(对应图5f),提示这些位点的假尿苷修饰可能促进转运RNA的核糖体A位点加载或减慢E位点释放。
产品关联:文献未提及具体实验产品,领域常规使用蔗糖密度梯度离心试剂、多聚体分离相关耗材。
4. Biomarker 研究及发现成果
本研究涉及的Biomarker为转运RNA上的各类修饰位点,尤其是不同区域的假尿苷位点,筛选验证逻辑为“测序技术开发→化学处理识别特征信号→敲除细胞系验证催化酶→功能样本验证修饰的功能相关性”。
研究过程详述:修饰位点的检测来源为人胚肾293T细胞的总RNA及多聚体结合RNA,验证方法包括化学处理依赖性的信号检测(缺失或突变信号)、假尿苷合成酶敲除后的信号变化验证。检测的特异性方面,假尿苷位点的缺失信号仅在亚硫酸氢盐处理后出现,且在对应合成酶敲除后信号显著降低;敏感性方面,最低覆盖度阈值为50条读长即可实现位点的稳定检测。文献未提供诊断相关的受试者工作特征曲线、敏感性特异性等临床数据。
核心成果提炼:共鉴定到3种假尿苷合成酶的特异性催化底物位点:假尿苷合成酶1负责5’反密码子茎区及线粒体转运RNA的假尿苷位点,假尿苷合成酶7负责D茎区假尿苷13、假尿苷20c、T茎区假尿苷50及酪氨酸转运RNA的假尿苷35,TruB同源假尿苷合成酶1负责T环区假尿苷54-55及线粒体转运RNA的T环假尿苷位点。假尿苷修饰间普遍存在正互作(比值比>1,假发现率(FDR)<0.05),且多数假尿苷位点与转运RNA氨酰化水平呈正相关,提示修饰协同调控转运RNA的功能状态。多聚体分析显示假尿苷55、假尿苷38-40等位点的修饰水平与转运RNA的核糖体A/P位点结合显著相关,可作为转运RNA翻译活跃状态的潜在标志物。本研究首次在单分子层面解析了人类转运RNA修饰的互作网络,且实现了修饰状态与翻译功能的直接关联,所有统计学结果均经过多重检验校正(假发现率<0.05),样本测序覆盖度均满足≥50读长的分析阈值要求。