慢性淋巴细胞白血病(CLL)伴临界IGHV突变状态患者的预后:系统评价和荟萃分析
Outcomes of patients with CLL and borderline IGHV mutational status: a systematic review and meta analysis
1. 领域背景与文献引入
文献英文标题:Borderline IGHV mutational status defines a distinct subgroup of chronic lymphocytic leukemia with intermediate outcomes: a systematic review and meta-analysis;发表期刊:未明确提供;影响因子:未公开;研究领域:慢性淋巴细胞白血病预后标志物研究。
慢性淋巴细胞白血病(CLL)是成人最常见的白血病类型之一,免疫球蛋白重链可变区(IGHV)突变状态是其临床风险分层的核心预后标志物。领域共识:传统研究将CLL患者分为突变型(M-IGHV,IGHV基因与胚系序列同源性<98%)和未突变型(U-IGHV,同源性≥98%),其中未突变型患者首次治疗时间(TTFT)更短、疾病进展更早。随着研究深入,介于97%-98%或接近98%的临界IGHV突变状态(BL-IGHV)逐渐受到关注,该亚群约占CLL患者的5%,但此前不同研究对其临床和生物学意义结论不一,存在研究空白:BL-IGHV是否为具有独立预后特征的CLL亚群、其预后定位及潜在驱动机制尚未明确,因此本研究通过系统综述与荟萃分析整合多中心数据,填补这一领域空白,为CLL的精准风险分层提供循证依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要基于IGHV突变状态的不同分组(M-IGHV、U-IGHV、BL-IGHV),同时关注不同研究中BL-IGHV定义的差异(部分研究采用97.00%-97.99%的同源性阈值,部分采用接近98%的阈值)。现有研究的关键结论存在分歧,部分研究提示BL-IGHV患者的预后介于M-IGHV和U-IGHV之间,且富集具有不良预后的B细胞受体(BCR)定型亚群#2,但也有研究未发现显著差异,导致其临床意义存在争议。现有研究多为回顾性队列研究,优势在于基于真实世界临床数据分析IGHV突变状态与预后的关联,局限性在于研究样本量差异较大、BL-IGHV的定义不统一、存在一定偏倚,且缺乏对现代靶向治疗反应的评估。本研究的创新价值在于首次针对BL-IGHV进行系统综述与荟萃分析,整合多中心标准化数据明确其预后特征,解决了此前研究结论不一致的问题,通过敏感性分析验证结果的稳定性,为BL-IGHV作为独立预后亚群的临床应用提供了可靠依据。
3. 研究思路总结与详细解析
本研究的整体框架为:以明确BL-IGHV CLL患者的预后特征为研究目标,核心科学问题是BL-IGHV是否为具有中间预后的独立CLL亚群,技术路线遵循“PRISMA指南文献筛选→多中心队列整合→荟萃分析预后关联→机制探索→敏感性分析验证→结论”的闭环逻辑。
3.1 文献筛选与队列整合
实验目的是获取符合纳入标准的BL-IGHV相关研究,构建可用于统一分析的临床队列。方法细节为严格遵循PRISMA指南进行文献检索,去除重复记录后通过标题、摘要和全文筛选,最终纳入3项符合标准的回顾性研究,整合得到包含122例BL-IGHV、1274例M-IGHV、760例U-IGHV患者的合并队列。结果解读:通过PRISMA文献筛选流程图(Fig.1)清晰展示了从2130条初始记录到最终3项研究的筛选过程,最终构建的合并队列覆盖了不同研究的患者群体,具备较好的代表性,为后续荟萃分析奠定了基础。
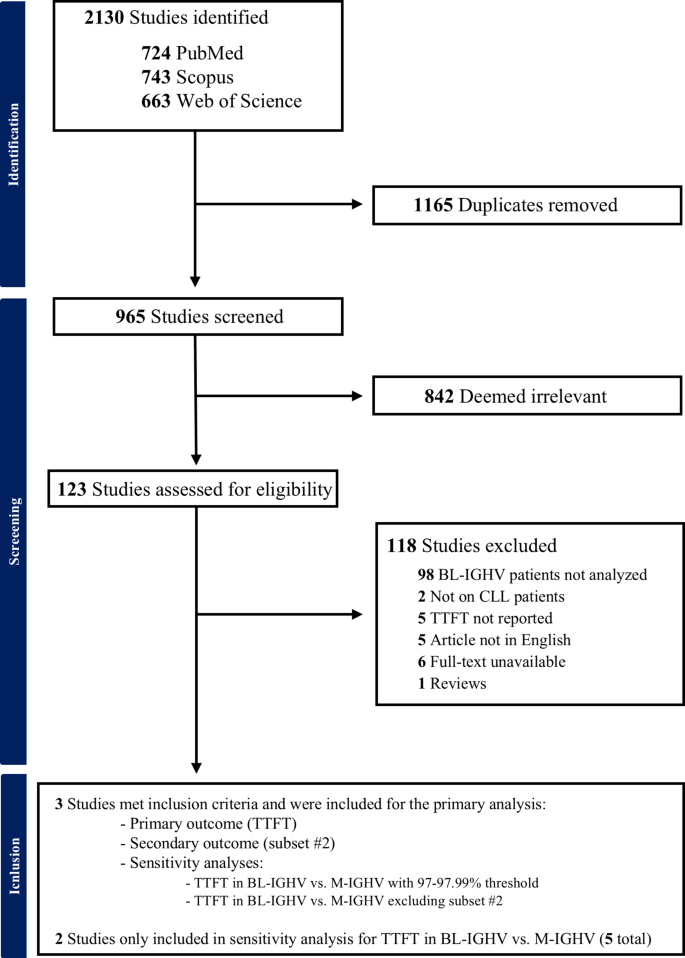
文献未提及具体实验产品,领域常规使用文献管理软件、核酸测序类试剂及生物信息学分析工具。
3.2 首次治疗时间的荟萃分析
实验目的是明确BL-IGHV与M-IGHV、U-IGHV患者的首次治疗时间(TTFT)差异,确定BL-IGHV的预后定位。方法细节为采用随机效应模型计算风险比(HR)评估不同IGHV突变状态患者的TTFT差异,同时按照DerSimonian-Laird方法重建合并Kaplan-Meier曲线分析中位TTFT。结果解读:森林图(Fig.2)显示,BL-IGHV患者的TTFT显著短于M-IGHV患者,风险比为2.28(95%置信区间1.20-4.35,n=1396,P<0.05);与U-IGHV患者相比,BL-IGHV患者的TTFT有更长的非显著趋势,风险比为0.55(95%置信区间0.30-1.03,n=882,P>0.05)。合并Kaplan-Meier曲线分析显示,BL-IGHV患者的中位TTFT为91.1个月,介于M-IGHV患者(中位TTFT未达到,n=1274,P=0.003)和U-IGHV患者(中位TTFT为41.1个月,n=760,P<0.001)之间,进一步验证了其中间预后特征。
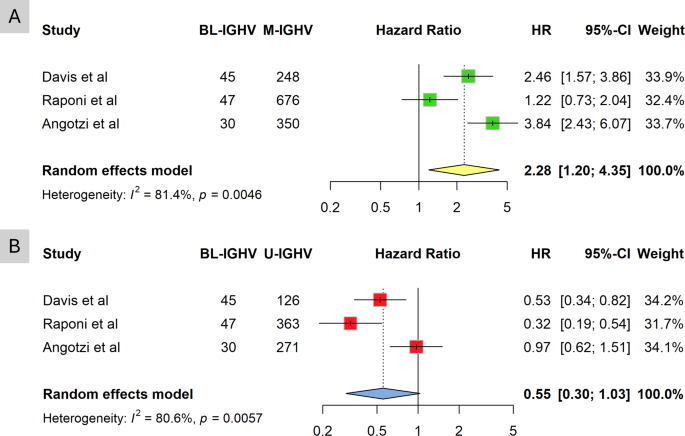
文献未提及具体实验产品,领域常规使用生存分析软件(如R语言survival包)、统计分析工具进行数据处理。
3.3 BCR定型亚群#2富集分析
实验目的是探索BL-IGHV患者中间预后特征的潜在生物学机制。方法细节为计算比值比(OR)分析BL-IGHV与M-IGHV、U-IGHV患者中BCR定型亚群#2的患病率差异,同时通过敏感性分析验证该亚群对预后的影响。结果解读:BL-IGHV患者中BCR定型亚群#2的患病率显著高于M-IGHV患者,比值比为8.56(95%置信区间3.79-19.33,n=1396,P<0.001);与U-IGHV患者相比,比值比为6.76(95%置信区间2.45-18.65,n=882,P<0.001)。在排除BCR定型亚群#2患者的敏感性分析中,BL-IGHV与M-IGHV患者的TTFT差异消失,提示BCR定型亚群#2是驱动BL-IGHV患者预后较差的关键因素。
文献未提及具体实验产品,领域常规使用免疫组化(IHC)、基因测序技术检测BCR定型亚群,使用统计软件进行比值比计算。
3.4 敏感性分析验证
实验目的是验证研究结果的稳定性与可靠性。方法细节为分别采用97-97.99%的BL-IGHV阈值、增加2项仅比较BL-IGHV与M-IGHV的研究、排除BCR定型亚群#2患者三种不同条件进行敏感性分析。结果解读:在采用97-97.99%阈值的分析中,BL-IGHV与M-IGHV的TTFT差异仍然显著;增加2项研究后,合并队列的结果也与主分析一致;排除BCR定型亚群#2后差异消失,进一步支持了研究结论的可靠性,同时明确了BCR定型亚群#2的驱动作用。
文献未提及具体实验产品,领域常规使用统计分析软件进行敏感性分析。
4. Biomarker研究及发现成果解析
本研究的核心Biomarker是临界免疫球蛋白重链可变区(BL-IGHV)突变状态,其筛选与验证逻辑为通过系统综述整合多中心临床队列数据,采用荟萃分析验证其与首次治疗时间(TTFT)的关联,结合BCR定型亚群#2的富集分析明确其预后价值及潜在机制。
该Biomarker的来源为临床CLL患者的IGHV基因测序数据,验证方法为通过荟萃分析比较不同IGHV突变状态患者的TTFT,计算风险比(HR)和比值比(OR)评估其预后相关性。特异性与敏感性方面,BL-IGHV作为预后标志物,区分M-IGHV和BL-IGHV的风险比为2.28(95%置信区间1.20-4.35),区分BL-IGHV和U-IGHV的风险比为0.55(95%置信区间0.30-1.03),能够有效识别具有中间预后的CLL亚群。
核心成果提炼:BL-IGHV是CLL中具有中间预后的独立亚群,其中位TTFT为91.1个月(n=122,P=0.003 vs M-IGHV,P<0.001 vs U-IGHV),其预后特征部分由BCR定型亚群#2的富集驱动。本研究的创新性在于首次通过荟萃分析明确了BL-IGHV的独立预后价值,解决了此前研究结论不一致的问题,为CLL的风险分层提供了新的依据,支持将BL-IGHV纳入常规临床报告,以优化CLL患者的个体化管理。