DMN-seq 利用 5-甲基胞嘧啶糖苷酶富集 DNA 低甲基化区域,用于生物标志物发现
DMN-seq enriches DNA hypomethylated regions for biomarker discovery using 5-methylcytosine glycosylase
1. 领域背景与文献引入
文献英文标题:DEMETER-assisted 5-Methylcytosine Nicking sequencing enables single-base resolution 5mC detection and hypomethylation profiling;发表期刊:Genome Biology;影响因子:17.9(2023年);研究领域:表观遗传学(DNA甲基化测序技术与肿瘤生物标志物研究)
DNA甲基化(5mC)是表观遗传学的核心调控机制之一,参与基因转录沉默、染色质结构维持等关键生物学过程,其异常与肿瘤发生发展密切相关。领域共识:亚硫酸氢盐测序(BS-seq)是5mC检测的金标准,但存在DNA损伤严重、测序成本高的局限性;后续发展的酶法测序技术如酶促甲基化测序(EM-seq)、TET辅助吡啶硼烷测序(TAPS)虽降低了DNA损伤,但存在碱基转换导致序列复杂度降低、不完全转换引发假阳性的问题;富集类方法如甲基化DNA免疫沉淀测序(MeDIP-seq)虽降低了测序成本,但仅能富集高甲基化区域,无单碱基分辨率,且需要大量起始样本。当前领域的核心未解决问题是:缺乏能同时实现单碱基分辨率检测、高效富集低甲基化区域、适配低输入临床样本的5mC测序技术,而低甲基化作为肿瘤早期发生的标志性事件,其精准分析对肿瘤早期诊断、生物标志物发现具有重要意义,但现有方法难以满足需求。本研究针对这一空白,开发了DEMETER辅助的5-甲基胞嘧啶切口测序(DMN-seq)技术,为5mC的全面分析及肿瘤低甲基化生物标志物研究提供了新工具。
2. 文献综述解析
作者对现有5mC测序方法按技术原理分为基于碱基转换(突变)和基于富集两类进行评述。基于碱基转换的方法以BS-seq为代表,通过化学脱氨基区分甲基化与未甲基化胞嘧啶,虽为金标准,但 harsh的亚硫酸氢盐处理会导致严重DNA损伤,且测序成本高;酶法如EM-seq、TAPS通过酶促反应实现碱基转换,减少了DNA损伤,但仍存在碱基转换导致序列复杂度降低、不完全转换引发假阳性的问题,且难以高效分析低甲基化区域。基于富集的方法包括MeDIP-seq和甲基化敏感限制性内切酶测序(MRE-seq),MeDIP-seq通过抗体富集高甲基化DNA,降低了测序成本,但偏向高甲基化区域,无单碱基分辨率,且抗体批次差异会影响结果稳定性;MRE-seq通过酶切未甲基化位点富集低甲基化区域,但酶切位点受限,无法覆盖全基因组低甲基化区域。
现有研究的核心局限性在于:无法同时兼顾单碱基分辨率、低样本量需求、高/低甲基化区域的全面分析,尤其是低甲基化区域的精准富集与检测技术存在明显空白。本研究的创新点在于首次利用植物来源的DNA糖基化酶DEMETER(DME)的特异性切割活性,开发了DMN-seq技术,分为DMN+(富集高甲基化区域,实现单碱基分辨率检测)和DMN-(富集低甲基化区域)两种实验模式,既解决了现有方法在低甲基化分析中的不足,又实现了单碱基分辨率的精准检测,同时适配低输入临床样本,为5mC测序技术的发展提供了新范式。
3. 研究思路总结与详细解析
本研究的整体目标是开发新型5mC测序技术,实现单碱基分辨率的5mC检测,并高效富集低甲基化区域,验证其在肿瘤样本及低输入游离DNA(cfDNA)中的临床应用价值;核心科学问题是如何利用DME酶对5mC的特异性切割活性构建测序文库,实现高甲基化与低甲基化区域的精准分析;技术路线遵循“酶活性验证→文库方法建立→细胞系样本验证→临床样本验证→低输入样本验证”的闭环逻辑,逐步验证技术的准确性、特异性与临床适用性。
3.1 DME酶活性与特异性验证
实验目的是验证DME酶对5mC的特异性切割能力,明确其能否区分5mC与5-羟甲基胞嘧啶(5hmC)。方法细节为:合成含单个5mC和单个5hmC的82bp双链DNA寡核苷酸(oligo),分别用0、125、250、500、750、1000ng的DME酶在37℃处理2h,经DNA纯化后进行尿素凝胶电泳检测。结果解读:凝胶电泳结果显示,DME酶对含5mC的oligo的切割呈剂量依赖性,酶量越高切割效率越高;而对含5hmC的oligo无切割活性(图1b),证明DME酶具有严格的5mC特异性,可有效区分5mC与5hmC,避免现有方法中无法区分两者导致的假阳性。实验所用关键产品:IDT的82bp dsDNA oligo、Zymo Research的DNA Clean & Concentrate kit、Invitrogen的Novex TBE-Urea Gel、Bio-Rad的ChemiDoc MP成像系统。
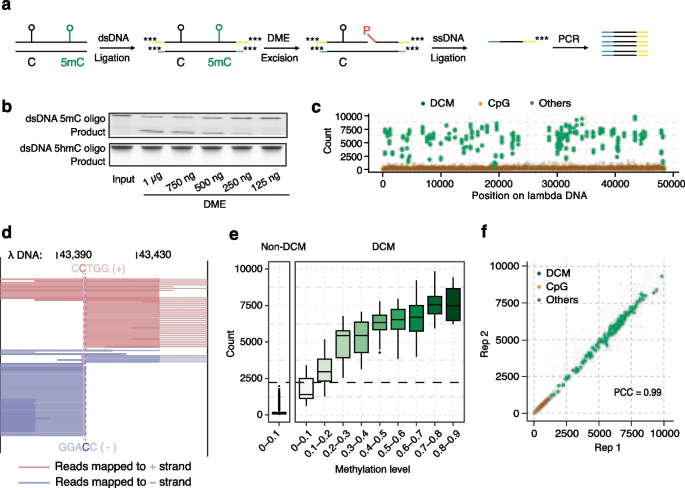
3.2 DMN+文库构建与单碱基分辨率验证
实验目的是验证DMN+方法能否实现单碱基分辨率的5mC检测。方法细节为:将λ-DNA或小鼠胚胎干细胞(mESC)基因组DNA(gDNA)片段化,连接含硫代磷酸酯修饰的定制接头,通过酶切去除未成功连接的片段及含游离5"-磷酸的片段,然后用DME酶处理,仅含5mC的片段会产生游离5"-磷酸,进而连接单链接头,最后通过PCR扩增构建测序文库。结果解读:DMN+文库能精准检测λ-DNA中部分甲基化的DCM基序位点,与超快速亚硫酸氢盐测序(UBS-seq)结果高度相关,技术重复的Pearson相关系数达0.99(图1f);在mESC样本中,97%以上检测到的5mC位点为CpG基序,与BS-seq结果一致(图2a),证明DMN+具有单碱基分辨率的5mC检测能力,且准确性高、重复性好。实验所用关键产品:NEB的NEBNext dsDNA Fragmentase、IDT的定制接头、Illumina的NovaSeqX测序平台。
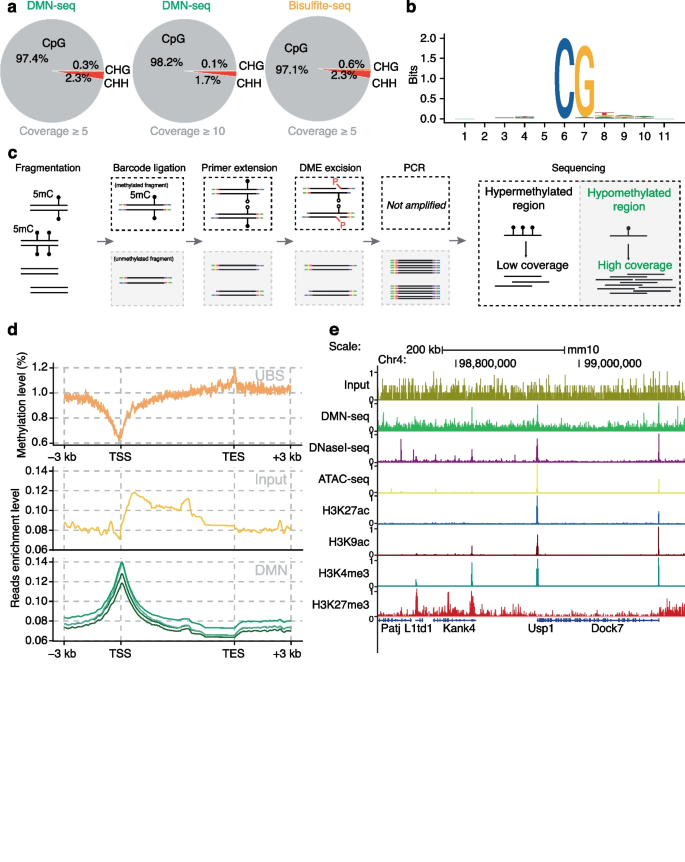
3.3 DMN-文库构建与低甲基化富集验证
实验目的是验证DMN-方法能否高效富集低甲基化区域。方法细节为:将DNA连接独特barcode,通过引物延伸合成互补链,然后用DME酶处理,含5mC的链会被切割去除,其互补链因缺乏P7接头序列无法在后续PCR中扩增,从而富集低甲基化片段。结果解读:在mESC样本中,DMN-处理后高甲基化的λ-DNA位点显著减少,低甲基化的转录起始位点(TSS)区域富集程度是转录终止位点(TES)的2倍(图2d),且富集的低甲基化区域与ATAC-seq、ChIP-seq检测的开放染色质区域、活性组蛋白标记区域高度重叠(图2e),证明DMN-能高效富集低甲基化区域,且特异性高。实验所用关键产品:Revvity的NEXTFLEX Unique Dual Index Barcodes、NEB的Q5 Hot Start High-Fidelity 2X Master Mix。
3.4 结直肠癌样本中低甲基化区域分析
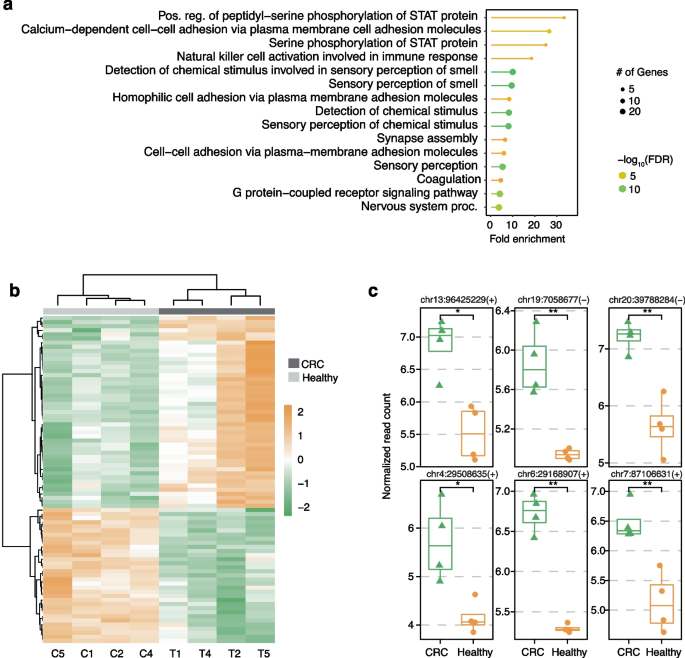
实验目的是验证DMN-在临床肿瘤样本中的应用价值,发现结直肠癌(CRC)相关的低甲基化生物标志物。方法细节为:收集6对CRC肿瘤与癌旁正常组织gDNA,构建DMN-文库,同时用简化代表性亚硫酸氢盐测序(RRBS)作为对照,分析差异甲基化区域(DMRs)及相关功能通路。结果解读:肿瘤样本中低甲基化区域显著多于癌旁组织(图3a),功能富集分析显示低甲基化区域关联的通路包括JAK-STAT信号通路(与肿瘤细胞增殖、免疫逃逸相关)、感觉感知通路(与CRC代谢异常相关)(图4a);进一步筛选出MBD3L3、OR2J2等潜在生物标志物,其中MBD3L3参与异染色质形成,是CRC的潜在预后标志物,OR2J2属于嗅觉受体家族,与CRC的预后及治疗相关(图4b、c)。实验所用关键产品:Qiagen的AllPrep DNA/RNA/miRNA Universal Kit、Zymo Research的Zymo-seq RRBS Library Kit。
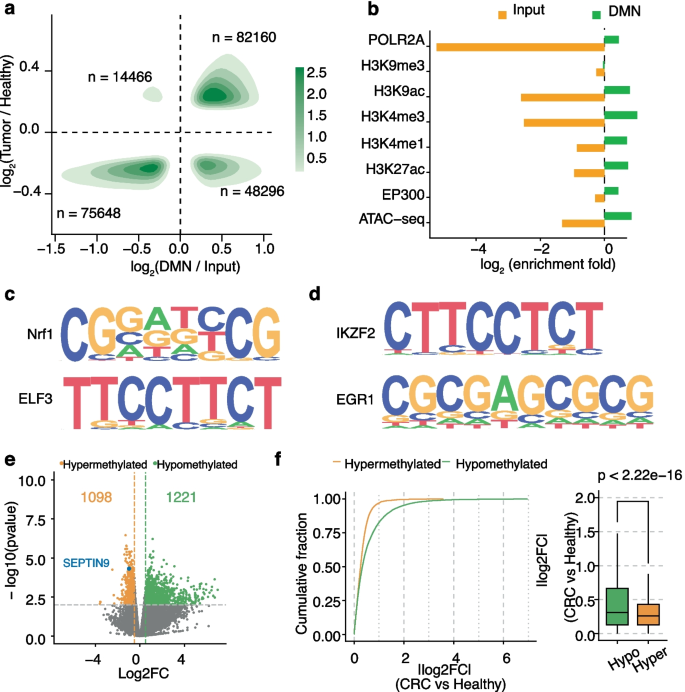
3.5 低输入cfDNA样本中的检测性能验证
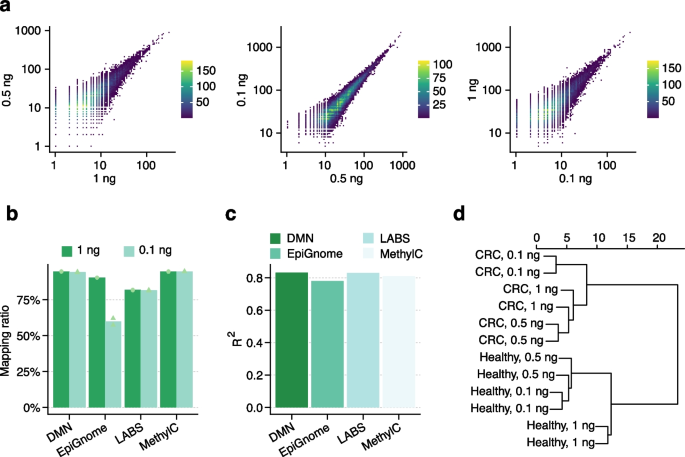
实验目的是验证DMN-在低输入cfDNA中的敏感性与可靠性。方法细节为:取1ng、0.5ng、0.1ng的CRC患者与健康对照cfDNA,构建DMN-文库,与现有低输入测序方法(LABS-seq、MethylC-seq、EpiGnome)的结果进行对比。结果解读:不同输入量的样本测序结果相关性高,即使在0.1ng低输入下仍能稳定检测低甲基化区域(图5a);DMN-的mapping率与现有方法相当,基因组范围内的相关性也与现有方法一致(图5b、c);样本聚类分析显示,样本按疾病状态聚类而非输入量,证明DMN-能有效捕获生物学信号,技术重复性好(图5d)。实验所用关键产品:Qiagen的QIAamp Circulating Nucleic Acid Kit、Illumina的NovaSeqX测序平台。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究中涉及的Biomarker包括CRC组织中的低甲基化基因(MBD3L3、OR2J2)、长散在核元件1(LINE-1)重复序列,筛选逻辑为:通过DMN-技术富集CRC肿瘤与癌旁组织的低甲基化区域→与RRBS结果对比验证差异甲基化区域→功能富集分析筛选与CRC发生发展相关的基因→结合现有研究验证其作为Biomarker的潜力;同时在低输入cfDNA中验证这些Biomarker的可检测性。
研究过程详述
Biomarker的来源为CRC患者的肿瘤组织gDNA与血浆cfDNA。验证方法包括:DMN-测序结合RRBS验证差异甲基化区域,功能富集分析明确基因功能,低输入cfDNA测序验证可检测性。特异性与敏感性数据:在CRC组织样本中,差异低甲基化区域的log2倍数变化(log2FC)绝对值显著高于高甲基化区域(图3f),样本量n=6对;在0.1ng低输入cfDNA中,DMN-仍能稳定检测到低甲基化区域,与高输入样本的相关性高(图5a)。
核心成果提炼
MBD3L3作为CRC的潜在预后Biomarker,其低甲基化与CRC的异染色质失调、肿瘤进展相关;OR2J2属于嗅觉受体家族,其低甲基化与CRC的代谢异常、预后相关;LINE-1重复序列的低甲基化作为CRC早期发生的标志性事件,可用于CRC的早期诊断与进展监测。这些Biomarker的创新性在于首次通过DMN-技术在CRC中系统分析低甲基化区域,发现了新的候选Biomarker,且这些Biomarker可在低输入cfDNA中稳定检测,为CRC的非侵入性诊断提供了新靶点。统计学结果显示,差异低甲基化区域的P值<0.0001(图4b),样本量n=6对组织样本,n=2例cfDNA样本(患者与对照)。