Characterization of novel interactions with membrane NEU1 highlights new regulatory functions for the Elastin Receptor Complex in monocyte interaction with endothelial cells.
对膜 NEU1 的新型相互作用的表征突显了弹性蛋白受体复合物在单核细胞与内皮细胞相互作用中的新调节功能
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2021 | 起止号: | 2021 Dec 13; 11(1):206 |
| doi: | 10.1186/s13578-021-00718-x | 研究方向: | 细胞生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:Characterization of novel interactions with membrane NEU1 highlights new regulatory functions for the Elastin Receptor Complex in monocyte interaction with endothelial cells;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:心血管生物学(血管重塑与炎症免疫调控)
血管重塑是多数心血管疾病的病理基础,涉及细胞外基质(ECM)的重组与降解。弹性蛋白作为血管壁ECM的主要成分,不仅维持血管的强度与弹性,其降解产生的弹性蛋白衍生肽(EDP)还通过弹性蛋白受体复合物(ERC)介导多种病理生理效应。领域共识:近十年研究表明,ERC的NEU1亚基(神经氨酸酶-1)在EDP介导的血管与代谢疾病中发挥关键作用,通过去唾液酸化调控膜糖蛋白功能,参与细胞迁移、黏附等过程。当前研究热点聚焦于NEU1的新相互作用靶点及其调控机制,但尚未明确NEU1如何通过ERC调控单核细胞与内皮细胞的相互作用,这是动脉粥样硬化等炎症性血管疾病早期阶段的关键事件,存在研究空白。因此,本研究旨在验证NEU1与β₂整合素、细胞间黏附分子-1(ICAM-1)的相互作用,并解析其对单核细胞-内皮细胞相互作用的调控机制,为血管重塑相关疾病的干预提供新靶点。
2. 文献综述解析
作者按“ECM重塑-EDP产生-ERC介导信号-NEU1功能”的时间线与分子通路维度,系统梳理了领域内现有研究。现有研究的关键结论包括:弹性蛋白降解产生的EDP主要通过ERC发挥生物学效应,NEU1作为ERC的信号转导亚基,通过去唾液酸化调控整合素、受体酪氨酸激酶等膜蛋白功能,参与心血管、代谢等疾病进程;技术方法上,已有研究采用蛋白质组学筛选NEU1的相互作用蛋白,如CD36,并验证了其对巨噬细胞摄取氧化低密度脂蛋白的调控作用,但这些研究多聚焦于单一细胞类型的单一靶点,缺乏对细胞间相互作用的系统研究;局限性在于,尚未阐明NEU1如何通过ERC调控单核细胞与内皮细胞的黏附及跨内皮迁移,而这是炎症性血管疾病早期单核细胞招募的核心环节。本研究的创新价值在于,首次在单核细胞中验证NEU1与β₂整合素的相互作用,在内皮细胞中验证NEU1与ICAM-1的相互作用,并揭示了EDP-ERC-NEU1轴通过去唾液酸化调控这两种膜蛋白,进而促进单核细胞黏附与跨内皮迁移的共同作用机制,填补了ERC在细胞间相互作用调控领域的研究空白。
3. 研究思路总结与详细解析
本研究的整体框架为:以“蛋白质组学筛选的NEU1候选相互作用蛋白”为切入点,核心目标是明确NEU1与β₂整合素、ICAM-1的相互作用及对单核细胞-内皮细胞相互作用的调控机制;核心科学问题是EDP结合ERC后,NEU1如何通过去唾液酸化调控β₂整合素和ICAM-1的功能;技术路线遵循“候选靶点验证→分子机制解析→功能效应验证→通路阻断确认”的闭环逻辑。
3.1 单核细胞中NEU1与β₂整合素的相互作用验证
实验目的:验证NEU1与β₂整合素在人单核细胞中的共定位及相互作用,并明确EDP对该相互作用的影响。
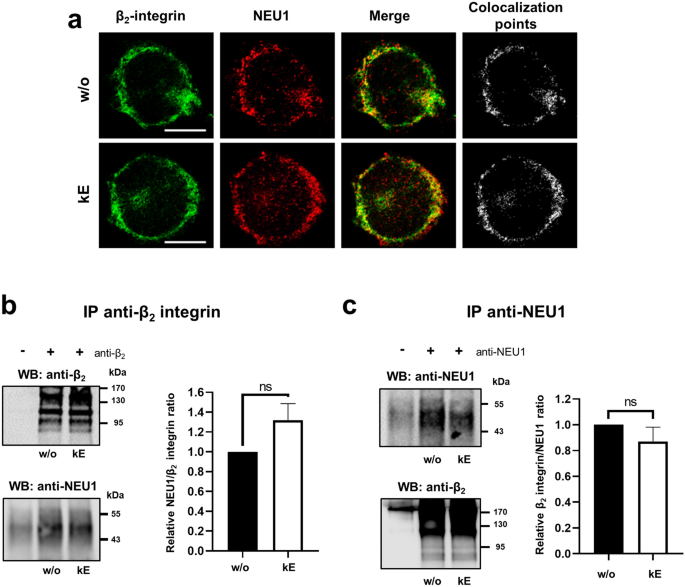
方法细节:采用人单核细胞系THP-1,通过免疫荧光共聚焦显微镜观察NEU1与β₂整合素的亚细胞定位;采用免疫共沉淀(co-immunoprecipitation)实验,分别以抗β₂整合素和抗NEU1抗体进行免疫沉淀,检测共沉淀的蛋白;实验中设置EDP(κE,50μg/mL)刺激组与对照组,刺激时间为1小时。
结果解读:共聚焦显微镜结果(图1)显示,β₂整合素主要定位于细胞膜,NEU1同时存在于细胞内与细胞膜,两者在细胞膜处共定位,EDP刺激不改变其共定位模式;免疫共沉淀结果显示,NEU1与β₂整合素在基础状态下即存在相互作用,EDP刺激后共沉淀的NEU1有增加趋势但无统计学显著性(p=0.0821,n=6)。
产品关联:实验所用关键产品:Santa Cruz Biotechnology的兔多克隆抗NEU1抗体(H-300)、小鼠单克隆抗NEU1抗体(F-8);Merck的小鼠单克隆抗β₂整合素抗体(MEM48);LI-COR的Odyssey Fc扫描仪用于蛋白条带可视化。
3.2 EDP通过NEU1调控β₂整合素的去唾液酸化
实验目的:明确EDP是否通过ERC-NEU1轴调控β₂整合素的唾液酸化水平。
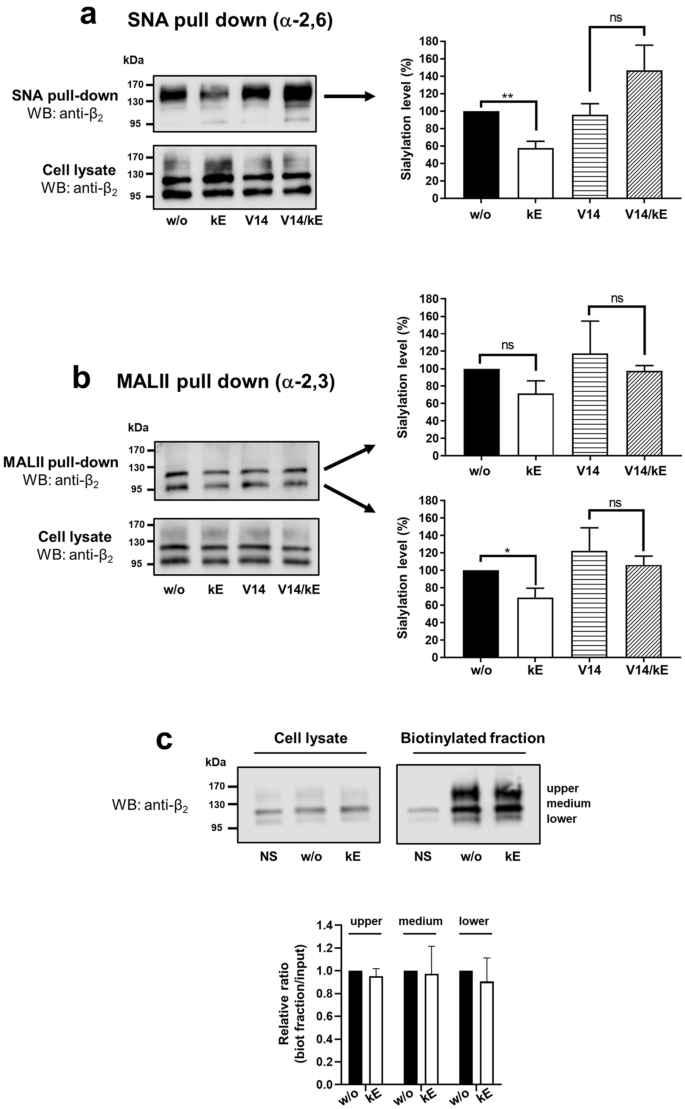
方法细节:采用凝集素下拉实验,分别用接骨木凝集素(SNA,识别α-2,6唾液酸)和马疫链球菌凝集素II(MALII,识别α-2,3唾液酸)富集唾液酸化的β₂整合素;设置κE刺激组、V14肽(阻断EDP与ERC结合)预处理组、DANA(广谱神经氨酸酶抑制剂)预处理组;通过蛋白质免疫印迹检测不同条带的唾液酸化水平,并用密度分析定量。
结果解读:结果(图2)显示,基础状态下β₂整合素的不同条带唾液酸化模式不同,~150kDa条带主要为α-2,6唾液酸化,~100kDa和~120kDa条带主要为α-2,3唾液酸化;κE刺激后,~150kDa条带的唾液酸化水平显著降低42.1±7.7%(n=4,P<0.01),~100kDa条带显著降低31.1±10.6%(n=4,P<0.05);V14肽预处理可完全阻断该效应,表明依赖于ERC;细胞表面蛋白生物素化实验显示,EDP刺激不改变β₂整合素的细胞膜表达水平。
产品关联:实验所用关键产品:Vector laboratories的生物素化SNA和MALII凝集素;ThermoScientific的EZLink® sulfo-NHS-LC-biotin用于细胞表面蛋白生物素化;Sigma的DANA(广谱神经氨酸酶抑制剂);Genecust合成的V14肽(纯度99%)。
3.3 单核细胞中NEU1调控β₂整合素对内皮细胞黏附的影响
实验目的:验证EDP-NEU1-β₂整合素轴对单核细胞黏附内皮细胞的调控作用。
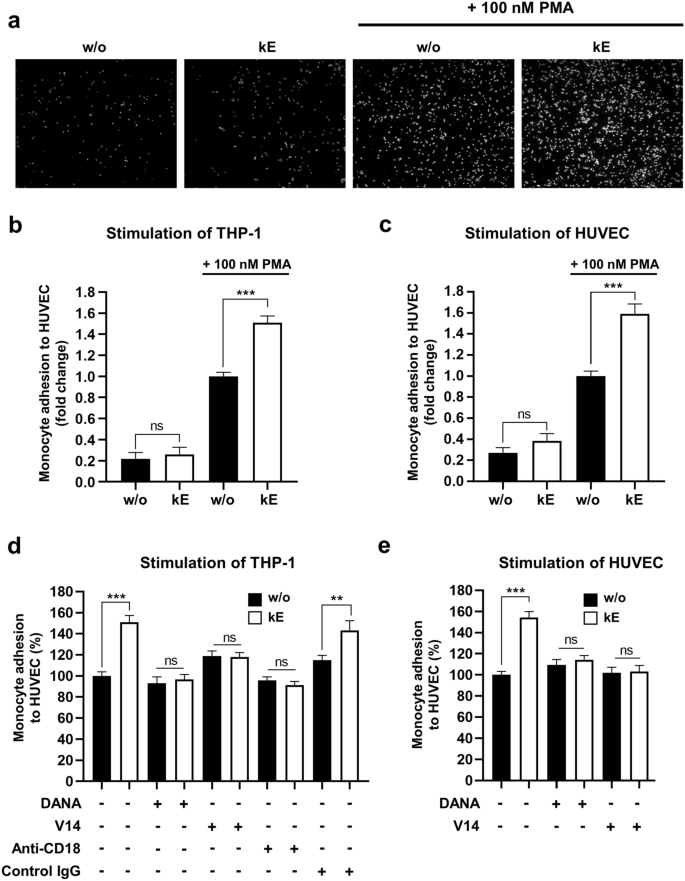
方法细节:采用人脐静脉内皮细胞(HUVEC),经佛波酯(PMA,100nM)过夜刺激诱导ICAM-1表达;THP-1单核细胞经κE刺激后,用钙黄绿素-AM标记,与HUVEC共孵育30分钟,通过荧光显微镜观察并定量黏附的单核细胞面积占比;设置V14肽、DANA、抗β₂整合素阻断抗体预处理组。
结果解读:结果(图3)显示,PMA刺激HUVEC后,单核细胞黏附率显著增加5倍(n=4-8,P<0.001);κE刺激单核细胞后,黏附率进一步显著增加50.8±6.5%(n=4-8,P<0.001);V14肽、DANA或抗β₂整合素阻断抗体可完全阻断该效应,表明依赖于ERC、NEU1的酶活性及β₂整合素。
产品关联:实验所用关键产品:Sigma的钙黄绿素-AM;Merck的抗β₂整合素阻断抗体及同型对照抗体;Zeiss的AXIO倒置荧光显微镜用于观察细胞黏附。
3.4 内皮细胞中NEU1与ICAM-1的相互作用及去唾液酸化调控
实验目的:验证NEU1与ICAM-1在人内皮细胞中的相互作用,及EDP对ICAM-1唾液酸化水平的调控。
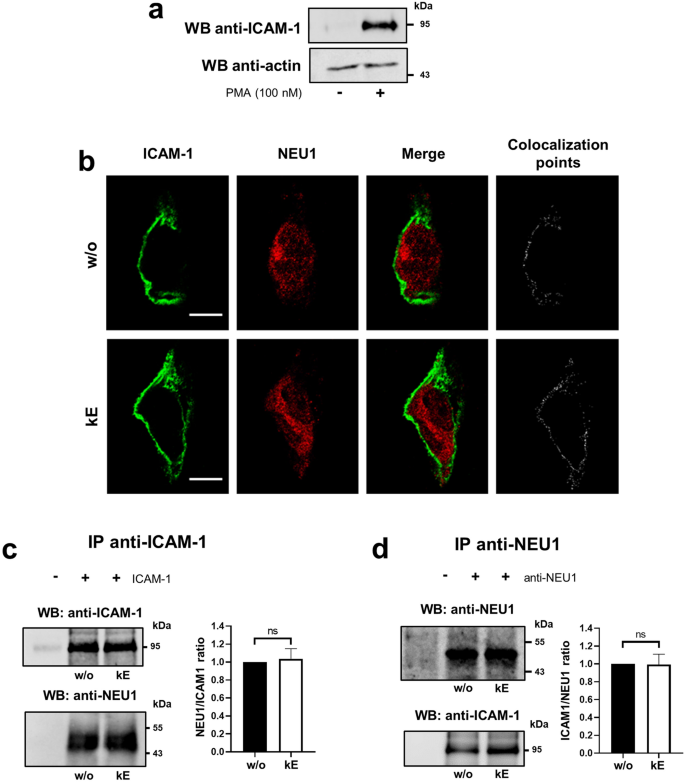
方法细节:采用PMA刺激的HUVEC,通过免疫荧光共聚焦显微镜观察NEU1与ICAM-1的共定位;采用免疫共沉淀实验验证两者的相互作用;采用SNA凝集素下拉实验检测ICAM-1的α-2,6唾液酸化水平;设置κE刺激组与V14肽预处理组。
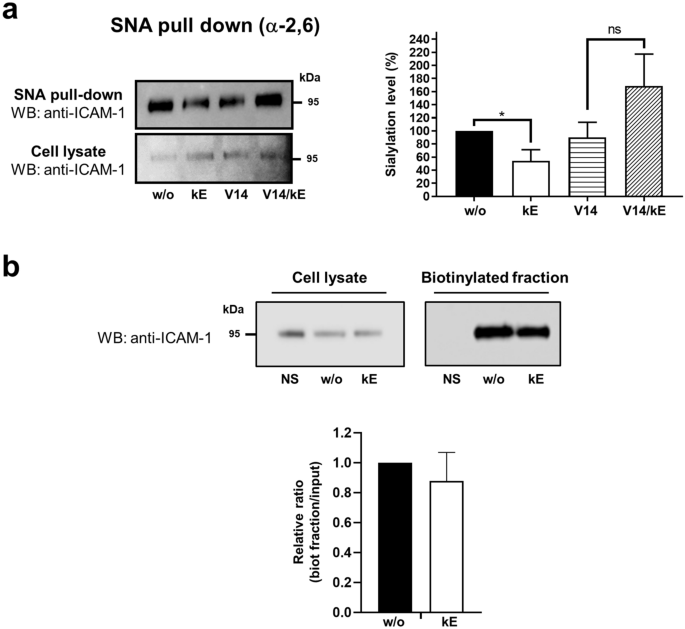
结果解读:共聚焦显微镜结果(图4)显示,ICAM-1主要定位于细胞膜,NEU1在细胞膜处与ICAM-1共定位,EDP刺激不改变其共定位;免疫共沉淀结果显示,NEU1与ICAM-1在基础状态下存在相互作用,EDP刺激无显著影响(n=3,P>0.05);凝集素下拉实验结果(图5)显示,κE刺激后ICAM-1的α-2,6唾液酸化水平显著降低46.0±17.5%(n=3,P<0.05),V14肽可阻断该效应;细胞表面蛋白生物素化实验显示,EDP刺激不改变ICAM-1的细胞膜表达水平。
产品关联:实验所用关键产品:Santa Cruz Biotechnology的小鼠单克隆抗ICAM-1抗体(6.5B5);Vector laboratories的生物素化SNA凝集素;Zeiss的LSM 710 NLO激光扫描显微镜用于共聚焦观察。
3.5 EDP-NEU1-ICAM-1轴对单核细胞黏附及跨内皮迁移的影响
实验目的:验证EDP-NEU1-ICAM-1轴对单核细胞黏附及跨内皮迁移的调控作用。
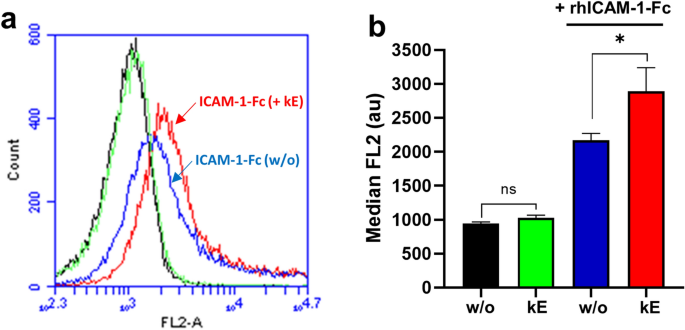
方法细节:采用Transwell小室构建HUVEC单层模型,检测单核细胞的跨内皮迁移能力;设置κE刺激HUVEC组、V14肽预处理组、DANA预处理组;通过荧光强度定量迁移的单核细胞数量;同时采用流式细胞术检测EDP刺激后单核细胞与ICAM-1的结合能力。
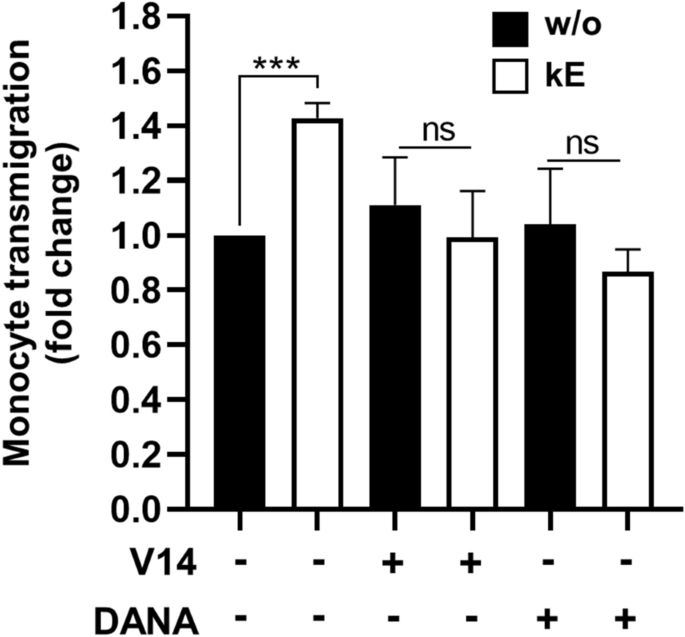
结果解读:流式细胞术结果(图6)显示,κE刺激单核细胞后,ICAM-1与单核细胞的结合能力显著增加(中位荧光强度从2168±102升至2893±347,n=5,P<0.05);Transwell实验结果(图7)显示,κE刺激HUVEC后,单核细胞跨内皮迁移能力显著增加42.8±5.6%(n=3-4,P<0.001),V14肽与DANA可完全阻断该效应;κE刺激单核细胞也可显著增加迁移能力32.6±7.9%(n=3-4,P<0.001)。
产品关联:实验所用关键产品:Greiner Bio-one的ThinCert™细胞培养小室(8μm孔径);BD Pharmingen的人Fc封闭试剂;BD Accuri C6流式细胞仪用于检测ICAM-1结合能力;TECAN infinite F200 Pro酶标仪用于定量荧光强度。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为膜蛋白β₂整合素(单核细胞)和ICAM-1(内皮细胞),属于功能型Biomarker,筛选逻辑为“蛋白质组学预筛选→细胞系共定位与免疫共沉淀验证→功能实验验证调控效应”的完整链条。
研究过程中,β₂整合素来源于人单核细胞系THP-1,ICAM-1来源于PMA刺激的人脐静脉内皮细胞;验证方法包括免疫共沉淀验证相互作用、凝集素下拉实验验证唾液酸化水平、细胞黏附与迁移实验验证功能效应;特异性与敏感性方面,β₂整合素的去唾液酸化效应在κE刺激后具有统计学显著性(P<0.05),ICAM-1的去唾液酸化效应同样具有统计学显著性(P<0.05),但未提供ROC曲线等诊断相关数据。
核心成果提炼:本研究首次发现,EDP通过ERC激活NEU1,分别使单核细胞β₂整合素和内皮细胞ICAM-1去唾液酸化,进而显著增强单核细胞与内皮细胞的黏附(增加50.8±6.5%,n=4-8,P<0.001)及跨内皮迁移(增加42.8±5.6%,n=3-4,P<0.001);该Biomarker的功能关联在于,作为单核细胞招募的关键调控分子,参与炎症性血管疾病的早期进程;创新性在于首次揭示了NEU1通过ERC调控两种细胞类型中不同膜蛋白的共同机制,为血管重塑相关疾病的干预提供了新的分子靶点。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。