Sex-biased transcriptome in in vitro produced bovine early embryos.
体外生产的牛早期胚胎的性别偏向转录组
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2025 | 起止号: | 2025 Aug 27; 15(1):123 |
| doi: | 10.1186/s13578-025-01459-x | 种属: | Bovine |
| 研究方向: | 其它 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Sex-specific transcriptomic differences in in vitro produced bovine blastocysts revealed by short- and long-read sequencing;发表期刊:BMC Bioinformatics;影响因子:未公开;研究领域:动物生殖生物学(早期胚胎性别特异性发育调控)
辅助生殖技术(如体外受精IVF)已成为畜禽遗传改良与繁殖效率提升的核心技术,早期胚胎性别特异性发育差异是该领域长期关注的热点问题。近几十年的研究显示,人、小鼠、牛、猪等多个物种的早期胚胎在性腺分化前已存在发育速率差异,雄性胚胎通常表现出更快的体外发育进程,但人类研究结果存在争议,部分研究未观察到显著性别偏差。现有研究已发现性别印记基因、X染色体剂量补偿、糖代谢活性、线粒体DNA拷贝数等层面的性别差异,但受培养条件、实验设计(如性别分选精液的使用)影响,结果一致性不足,且缺乏对转录组全层面(基因表达、可变剪接、异构体动态)的综合解析,导致性别特异性发育的分子机制仍不明确。
针对这一研究空白,本研究采用半囊胚PCR性别鉴定结合长短读长RNA测序技术,规避性别分选精液引入的变异,系统分析体外培养牛扩张囊胚的性别特异性转录组差异,从基因表达、可变剪接、异构体三个维度揭示雄性胚胎发育更快的分子基础,为早期胚胎性别调控机制提供新的见解。
2. 文献综述解析
作者对现有研究的分类维度主要包括物种(人、小鼠、牛、猪等)、研究层面(发育速率、基因表达、代谢特征、表观遗传调控)、实验条件(体内/体外培养体系、精液处理方式)三类。
现有研究的关键结论显示,多数哺乳动物体外培养早期胚胎存在雄性发育更快的现象,但人类研究因样本来源、培养体系差异结果不一致;已鉴定出性别印记基因、X连锁基因、代谢相关基因的表达差异,以及线粒体功能、端粒长度等层面的性别特异性特征。技术方法上,RNA测序等组学技术已能实现转录组层面的差异分析,但部分研究使用性别分选精液引入额外变异,且仅聚焦于基因表达层面,缺乏对可变剪接和异构体的综合解析,同时不同培养条件导致的结果争议尚未得到明确解释。
本研究的创新价值在于,首次结合长短读长RNA测序技术,全面解析体外培养牛囊胚的性别特异性转录组差异,涵盖基因表达、可变剪接、异构体动态三个核心层面;采用半囊胚PCR性别鉴定策略,避免性别分选精液的干扰,确保样本的随机性与可靠性;系统揭示X染色体剂量补偿机制在性别差异发育中的调控作用,明确代谢通路与雄性胚胎快速发育的直接关联,填补了早期胚胎性别调控机制研究中转录组全层面分析的空白。
3. 研究思路总结与详细解析
本研究的整体框架为:以揭示体外培养牛囊胚性别特异性发育的转录组机制为目标,聚焦“雄性胚胎发育更快的分子基础”这一核心科学问题,构建“体外胚胎培养→样本性别鉴定→转录组测序→生物信息学分析→实验验证”的完整技术闭环,综合解析基因表达、可变剪接、异构体及X染色体剂量补偿的调控作用。
3.1 体外胚胎培养与样本收集
实验目的:获取足量且发育同步的体外培养牛扩张囊胚,为后续转录组分析与性别鉴定提供可靠样本。
方法细节:从屠宰场获取牛卵巢,采集2-8mm卵泡中的卵母细胞,使用IVF Bioscience系列培养基依次进行卵母细胞成熟培养(22h)、体外受精(18h)、胚胎培养至第7-8天;选择扩张囊胚均分为两半,一半用于PCR性别鉴定,一半用于RNA测序;为增加统计效力,共收集444个囊胚进行性别鉴定,同时将同性别半囊胚2个混合为一个生物学重复,最终获得5个雄性样本、6个雌性样本。
结果解读:性别鉴定结果显示,第7天扩张囊胚中雄性占比69.03%(107/155,n=155,P<2.15e-06),第8天各发育阶段囊胚均呈现雄性偏多(非扩张80/99,P<8.75e-10;扩张91/112,P<3.73e-11;孵化29/34,P<3.86e-05),验证了雄性胚胎体外发育更快的现象;半囊胚样本同时包含内细胞团和滋养层,确保转录组数据能代表整个囊胚的特征。
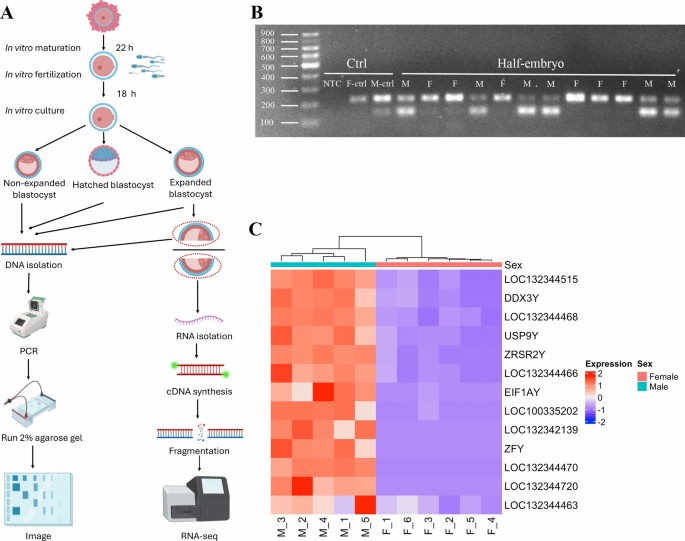
实验所用关键产品:IVF Bioscience的BO-IVM™、BO-IVF™、BO-IVC™培养基,New England Biolabs的OneTaq® Quick-Load® 2× Master Mix。
3.2 转录组文库构建与测序
实验目的:获取高质量的性别特异性转录组数据,涵盖基因表达、可变剪接及异构体信息。
方法细节:混合半囊胚样本采用SMART-Seq® HT PLUS Kit构建短读长cDNA文库,通过Novogene NovoSeq PE150平台测序;同时收集25个4细胞胚胎,采用PacBio ISO-Seq® express 2.0 kit、SMRTbell® prep kit 3.0构建长读长文库,在Revio平台进行HiFi测序。
结果解读:短读长测序共产生399,685,192条原始reads,平均每个样本36,335,017条,Q20≥89.94%、Q30≥83.16%,与牛参考基因组的唯一比对率平均达80.94%,数据质量满足后续分析要求;长读长测序鉴定出286,711个独特异构体,其中包含140,000多个新异构体,显著完善了牛早期胚胎的转录组注释。
实验所用关键产品:Taraka的SMART-Seq® HT PLUS Kit,PacBio的ISO-Seq® express 2.0 kit、SMRTbell® prep kit 3.0,Novogene的NovoSeq PE150测序服务。
3.3 差异基因表达与功能调控分析
实验目的:鉴定性别差异表达基因,解析其功能及上游调控机制。
方法细节:采用fastp进行测序数据质控,STAR软件比对至牛参考基因组,featureCounts进行基因计数,DESeq2鉴定差异基因(筛选标准:|Fold Change|>1.5,FDR<0.1);通过clusterProfiler进行GO和KEGG功能富集分析;从AnimalTFDB数据库筛选性别差异转录因子(TF),从人类RBP数据库转换得到牛同源RBP并筛选性别差异成员。
结果解读:共鉴定出837个性别差异表达基因,其中雄性上调231个、下调606个;GO功能富集显示,雄性差异基因主要富集于氨基酸生物合成、细胞代谢过程,雌性差异基因富集于雌性配子发生、性腺发育、细胞连接组装调控;KEGG通路分析显示,雄性差异基因富集于代谢与生物合成通路,雌性差异基因富集于炎症反应、TGF-β信号通路、紧密连接通路;进一步鉴定出68个性别差异TF(雄性19个、雌性49个)和52个性别差异RBP(雄性21个、雌性31个),其中雄性的HMGA2、SOX21、PRDM14为多能性调控关键因子,雌性的FMR1、HNRNPH2为可变剪接调控核心剪接因子。
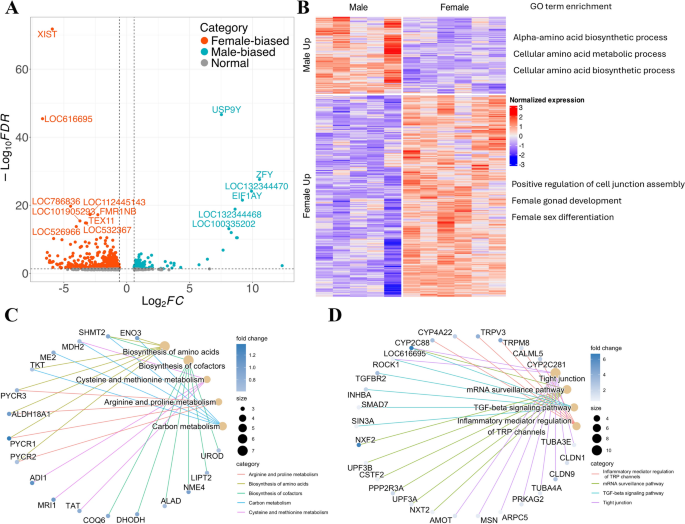
文献未提及具体实验产品,领域常规使用R语言的DESeq2、clusterProfiler等生物信息学工具。
3.4 X染色体剂量补偿机制分析
实验目的:解析X染色体剂量补偿在性别特异性发育中的调控作用。
方法细节:计算X染色体与常染色体的表达比率(X:A),分为表达基因、差异基因、非差异基因三类;排除同源基因后重新计算X:A比率,避免同源序列对表达定量的干扰;分析X染色体上差异基因与已知X染色体失活(XCI)逃逸基因的分布特征。
结果解读:雄性X:A比率在表达基因中约为1(完全剂量补偿),在差异基因中略低于1(不完全补偿);雌性X:A比率在表达基因中约为1.3,在差异基因中超过1.5,表明雌性X连锁差异基因是剂量补偿的主要驱动因素;17个已知XCI逃逸基因在雌性中呈现差异表达,且集中于X染色体的基因富集区域,但不与假常染色体区域(PAR)重叠,提示XCI逃逸基因参与雌性胚胎的性别特异性调控。
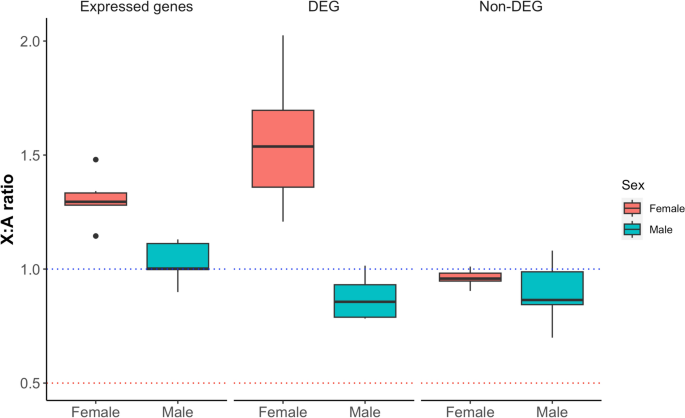
文献未提及具体实验产品,领域常规使用R语言的pairwiseCI、RIdeogram等分析工具。
3.5 可变剪接与异构体差异分析
实验目的:解析可变剪接与异构体动态在性别特异性发育中的调控作用。
方法细节:采用rMATS-turbo软件鉴定性别差异可变剪接事件(筛选标准:FDR≤0.01,|ΔPSI|≥0.05);将长读长鉴定的新异构体整合至牛参考基因组注释,采用Salmon定量异构体表达,通过fishpond的swish方法鉴定差异异构体(筛选标准:q-value<0.05);使用DEXSeq分析性别差异外显子使用情况。
结果解读:共鉴定出1555个性别差异可变剪接事件,其中跳过外显子(SE)为最主要类型(雄性475个、雌性281个);功能富集显示,雄性可变剪接相关基因富集于mRNA加工、代谢过程,雌性富集于酰胺与肽生物合成过程;共鉴定出1151个差异异构体(雄性637个、雌性514个),对应1017个基因,雄性异构体相关基因富集于肽代谢、ATP合成,雌性富集于转录负调控、RNA生物合成;进一步鉴定出5个存在差异外显子使用的基因(DENND1B、DIS3L2、DOCK11、IL1RAPL2、ZRSR2Y),提示其在早期胚胎中存在性别特异性调控。

文献未提及具体实验产品,领域常规使用rMATS-turbo、Salmon、fishpond等生物信息学工具。
3.6 实验结果验证
实验目的:验证转录组分析结果的可靠性。
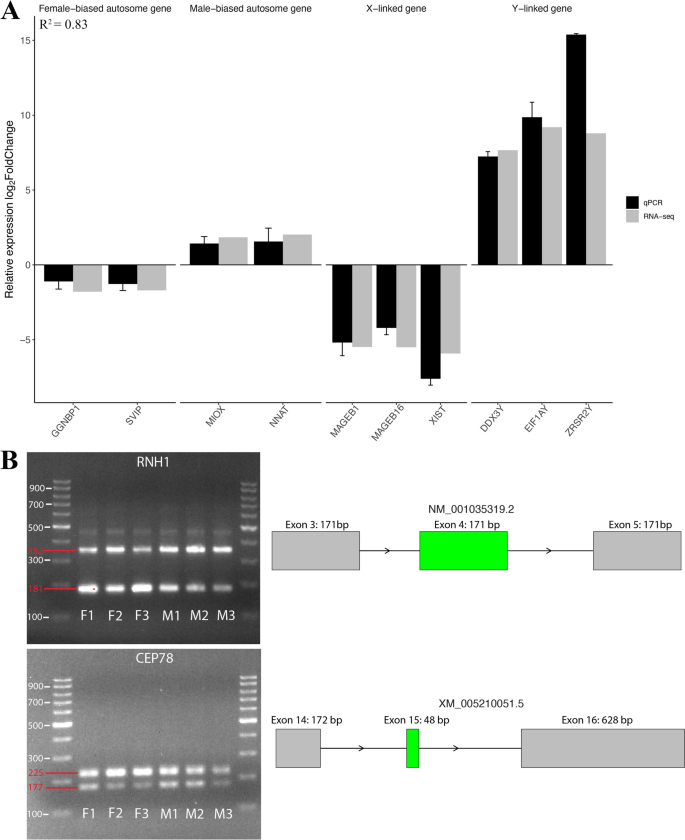
方法细节:选择10个差异表达基因(雌性上调5个、雄性上调5个)采用qPCR进行表达验证;选择5个差异跳过外显子事件设计特异性引物,通过PCR凝胶电泳验证外显子包含水平。
结果解读:qPCR结果与RNA测序的表达趋势高度一致(R²=0.83),证实差异基因分析的可靠性;PCR凝胶电泳显示,雄性胚胎中RNH1的外显子包含条带亮度显著高于外显子跳过条带,雌性胚胎中CEP78的外显子包含条带更丰富,与RNA测序计算的PSI值完全一致,验证了可变剪接分析结果的准确性。

实验所用关键产品:Bio-Rad的iTaq™ Universal SYBR® Green Supermix,New England Biolabs的OneTaq® Quick-Load® 2× Master Mix。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的Biomarker包括性别特异性差异表达基因、差异可变剪接事件、差异异构体三类,筛选与验证逻辑为:体外培养牛扩张囊胚→半囊胚PCR性别鉴定→长短读长RNA测序筛选差异分子→qPCR/PCR凝胶电泳验证→功能富集分析明确调控作用。
研究过程详述
Biomarker来源为体外培养牛扩张囊胚的转录组数据,涵盖基因、转录本、异构体三个层面;验证方法包括qPCR(基因表达)、PCR凝胶电泳(可变剪接);特异性与敏感性方面,差异基因的FDR<0.1,可变剪接事件的FDR≤0.01且|ΔPSI|≥0.05,差异异构体的q-value<0.05,确保结果的统计学可靠性。
核心成果提炼
- 性别差异基因Biomarker:雄性上调的代谢相关基因(如ENO3、PYCRs、SHMT2)可作为雄性胚胎快速发育的标志物,功能关联为参与氨基酸代谢、碳代谢通路,样本量n=5(雄性)、n=6(雌性);雌性上调的XCI逃逸基因(如MED12、SMARCA1)首次被证实与牛囊胚性别发育差异相关,样本量n=5(雄性)、n=6(雌性)。
- 性别差异可变剪接Biomarker:跳过外显子事件(如雄性的ZMYND11、雌性的CEP78)可作为性别特异性转录调控的标志物,首次揭示可变剪接在牛早期胚胎性别发育中的调控作用,样本量n=5(雄性)、n=6(雌性)。
- 性别差异异构体Biomarker:APOE的雄性高表达异构体、GOLM2的雄性特异性异构体首次被鉴定,功能关联为参与脂质代谢、高尔基体功能调控,为性别特异性发育提供新的分子靶点,样本量n=5(雄性)、n=6(雌性)。
本研究的核心成果明确了代谢通路激活是雄性胚胎快速发育的关键驱动因素,同时揭示X染色体剂量补偿、可变剪接、异构体动态在性别特异性发育中的协同调控作用,为早期胚胎性别调控机制研究提供了全面的转录组层面证据。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。