IgD in nucleus of pro-B cells promotes pro-B cells proliferation by regulating E2F3 expression
前B细胞核内的IgD通过调节E2F3表达促进前B细胞增殖。
| 期刊: | Cell and Bioscience | 影响因子: | 6.100 |
| 时间: | 2025 | 起止号: | 2025 Oct 29;15(1):149. |
| doi: | 10.1186/s13578-025-01490-y | 靶点: | E2F3 |
文献解析
1. 领域背景与文献
文献英文标题:未明确提供;发表期刊:未明确提供;影响因子:未公开;研究领域:B细胞发育与免疫球蛋白功能
免疫球蛋白家族是体液免疫应答的核心效应分子,根据重链恒定区结构分为IgM、IgD、IgG、IgA、IgE五类,其中IgM、IgG、IgA、IgE的功能已被广泛阐明,分别参与初次免疫应答、长期免疫保护、黏膜免疫及过敏反应等过程。IgD作为进化保守的免疫球蛋白亚型,长期以来仅被认为是成熟B细胞的表面标记分子,其生理功能一直是领域内未解决的核心问题。近年研究虽发现IgD可作为B细胞受体识别多价抗原、诱导自身反应性B细胞免疫耐受,但关于IgD缺失对B细胞数量的影响存在矛盾结论,且传统免疫学观点认为祖B细胞(pro-B细胞)阶段无IgD表达,IgD在B细胞发育早期的功能完全未知。当前领域研究热点集中于IgD在成熟B细胞中的免疫调控作用,而IgD在B细胞发育起始阶段的表达及功能是关键研究空白。本研究针对这一空白,通过构建IgD基因敲除小鼠模型,系统探究IgD在祖B细胞中的表达、定位及调控机制,填补了领域对IgD非经典功能的认知空白,为B细胞发育的分子调控网络提供了新视角。
2. 文献综述解析
作者对领域内现有研究按IgD的表达阶段(成熟B细胞vs早期B细胞)和功能方向(B细胞受体功能、免疫耐受、B细胞数量影响)进行分类评述,梳理了现有研究的核心结论、技术优势与局限性。现有研究证实,IgD作为成熟B细胞表面的B细胞受体,能有效识别复杂多价抗原并启动更强的钙信号通路,还可诱导自身反应性B细胞的免疫耐受;研究多采用基因敲除或转基因小鼠模型,能直接且特异性地探究IgD的功能。但现有研究存在明显局限性:一是研究范围集中于成熟B细胞,完全未关注B细胞发育早期阶段,传统观点认为祖B细胞阶段仅发生IgM重链重排,无其他免疫球蛋白表达;二是关于IgD缺失对B细胞数量的影响存在矛盾,Lutz等研究显示IgD缺失小鼠B细胞数量无显著变化,而Ubelhart等则发现B细胞数量显著减少;三是IgD的亚细胞定位及非受体功能完全未被揭示。本研究的创新价值在于突破了传统认知,首次发现IgD在祖B细胞阶段表达并定位于细胞核,作为转录因子调控细胞增殖相关基因的表达,明确了IgD缺失导致B细胞数量减少的具体阶段及分子机制,填补了IgD在B细胞发育早期功能的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是明确IgD在B细胞发育早期的表达及功能,解决的核心科学问题包括:IgD是否在祖B细胞中表达、IgD缺失导致B细胞数量减少的具体发育阶段是什么、IgD调控祖B细胞发育的分子机制是什么。技术路线遵循“模型构建→表型分析→功能验证→机制解析”的闭环逻辑:首先构建IgD基因敲除小鼠模型,验证模型有效性并初步分析免疫表型;随后通过流式细胞术定位B细胞发育异常的具体阶段;接着检测祖B细胞中IgD的表达与亚细胞定位;再通过体外细胞功能实验和转录组学分析探究IgD对祖B细胞增殖的影响;最后通过染色质免疫沉淀、电泳迁移率变动分析等技术验证IgD作为转录因子的分子机制。
3.1 IgD敲除小鼠模型构建与表型验证
实验目的是构建IgD功能完全缺失的小鼠模型,验证模型有效性并初步分析IgD缺失对免疫球蛋白分泌及B细胞数量的影响。方法细节:采用CRISPR-Cas9技术靶向敲除IgD恒定区的两个外显子,引入移码突变导致功能性IgD缺失,将 founder小鼠与C57BL/6J野生型小鼠回交6代以降低脱靶效应;通过免疫印迹(Western blot)和流式细胞术验证B细胞中IgD的缺失;检测血清中总IgG、IgM、IgA水平,并用胸腺依赖抗原NP偶联血蓝蛋白(NP-KLH)免疫小鼠,动态监测特异性抗体水平。结果解读:免疫印迹结果显示,IgD敲除小鼠脾脏B细胞中无IgD蛋白表达,IgM蛋白水平显著升高;流式细胞术分析显示,敲除小鼠脾脏和骨髓中B220+ B细胞的比例及绝对数量均显著减少(n=4,P<0.01);血清总IgG、IgM、IgA水平及NP特异性IgG、IgM、IgA水平与野生型小鼠无统计学差异,提示IgD缺失不影响体液免疫应答的整体能力。实验所用关键产品:CRISPR-Cas9基因编辑系统(上海邦耀生物科技有限公司)、抗CD19抗体(Biolegend, 115540)、抗B220抗体(BD, 103236)、抗IgD抗体(Santa, sc-53853)、抗IgM抗体(BD, 552867)。

3.2 B细胞发育阶段数量分析与IgD表达检测
实验目的是确定IgD缺失影响B细胞发育的具体阶段,并验证祖B细胞中是否存在IgD的表达与定位。方法细节:通过流式细胞术分选出pre-pro-B、pro-B、pre-B、未成熟B细胞,分析各阶段细胞的比例及绝对数量;采用RT-PCR、定量PCR(qRT-PCR)检测IgD重链和轻链的转录水平,通过DNA测序验证重排多样性;用免疫印迹检测非还原和还原条件下IgD蛋白的存在形式;通过免疫荧光染色结合共聚焦显微镜观察IgD的亚细胞定位。结果解读:流式细胞术结果显示,IgD敲除小鼠的pro-B、pre-B、未成熟B细胞数量均显著减少(n=4,P<0.01),而pre-pro-B细胞数量无变化,提示IgD缺失对B细胞发育的影响起始于pro-B细胞阶段;RT-PCR和qRT-PCR结果显示,祖B细胞中存在IgD重链和κ轻链的转录,且具有典型的V(D)J重排多样性;免疫印迹证实祖B细胞中存在完整的四聚体IgD蛋白;免疫荧光染色显示,IgD定位于祖B细胞的细胞核内,与组蛋白H3共定位,而在成熟B细胞中IgD主要分布于细胞膜表面。实验所用关键产品:TRIzol(Invitrogen)、RevertAid First Strand cDNA Synthesis Kit(Thermo Fisher Scientific)、抗组蛋白H3抗体(Proteintech)、Leica SP8共聚焦显微镜。

3.3 IgD缺失对祖B细胞增殖与细胞周期的影响
实验目的是探究IgD缺失对祖B细胞增殖功能的影响及相关分子变化。方法细节:分选野生型和IgD敲除小鼠的祖B细胞进行体外培养,加入IL-7刺激细胞增殖,每日计数活细胞;通过流式细胞术检测细胞周期分布、凋亡相关分子Fas及IL-7受体(IL-7R)的表达;对祖B细胞进行转录组测序(RNA-seq),分析差异表达基因及富集通路。结果解读:体外培养结果显示,IgD敲除祖B细胞的增殖能力显著降低(n=3,P<0.01),IL-7刺激后细胞体积增大不明显;细胞周期分析显示,敲除组祖B细胞在G0/G1期积累,S和G2/M期细胞比例显著减少;Fas分子表达显著升高(n=3,P<0.01),IL-7R表达显著降低(n=3,P<0.01);RNA-seq分析显示,敲除组有404个基因上调、492个基因下调,差异基因显著富集于细胞周期、染色体凝聚、染色体分离等通路,增殖相关基因如Mki67、Smc2、Smc4等表达显著下调。实验所用关键产品:IL-7(Biolegend)、碘化丙啶(PI)细胞周期检测试剂盒、Illumina NovaSeq 6000测序平台。

3.4 IgD作为转录因子调控E2f3a表达的机制验证
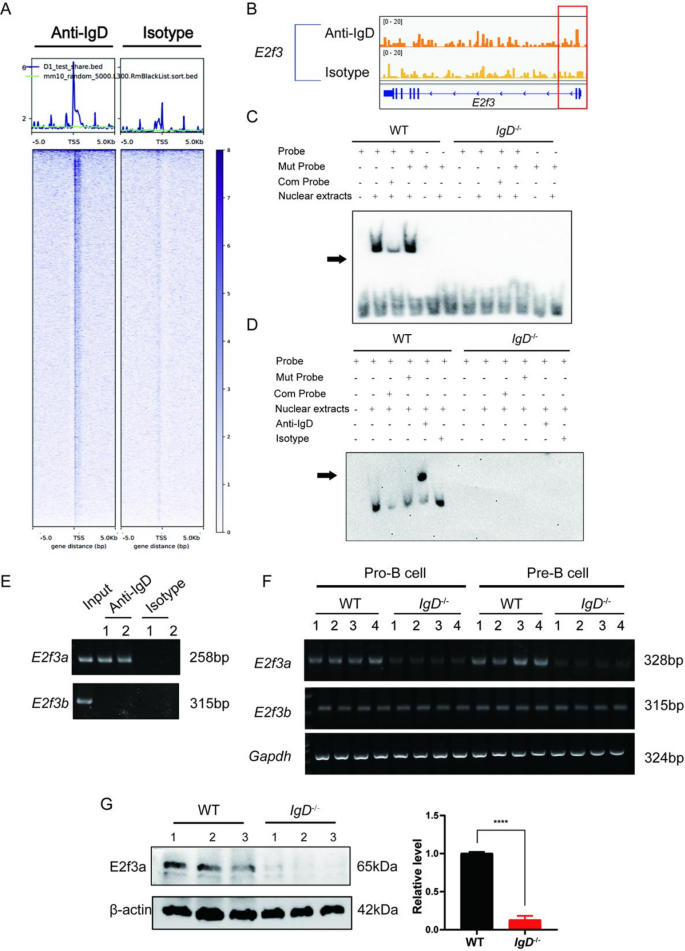
实验目的是验证IgD是否通过直接结合增殖相关转录因子E2f3的启动子区域调控其表达。方法细节:通过染色质免疫沉淀测序(ChIP-seq)和ChIP-PCR检测IgD与E2f3启动子的结合特异性;采用电泳迁移率变动分析(EMSA)验证IgD与E2f3启动子的直接结合;通过RT-PCR和免疫印迹检测E2f3两个亚型(E2f3a、E2f3b)的表达水平。结果解读:ChIP-seq结果显示,IgD在E2f3基因的启动子区域有明显的结合峰,ChIP-PCR证实IgD特异性结合E2f3a的启动子区域,而不结合E2f3b的启动子;EMSA结果显示,野生型祖B细胞的核提取物与E2f3a启动子探针结合形成特异性条带,未标记的竞争探针可消除该条带,突变探针则无结合信号,超迁移实验进一步证实结合条带包含IgD蛋白;IgD敲除祖B细胞中E2f3a的转录水平和蛋白水平均显著降低(n=3,P<0.0001),而E2f3b的表达无变化。实验所用关键产品:Pierce Magnetic ChIP Kit(Thermo Fisher, 26157)、EMSA生物素标记探针、抗E2f3抗体(CST, DF12390)。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker为核定位的IgD蛋白,筛选与验证逻辑为:通过IgD基因敲除小鼠模型发现B细胞发育异常起始于祖B细胞阶段,进而检测祖B细胞中IgD的表达与定位,通过体外功能实验和转录组学分析锁定其调控的靶基因,最终通过染色质免疫沉淀、EMSA等技术验证其转录调控功能。
该Biomarker来源于小鼠骨髓祖B细胞的细胞核,验证方法包括:免疫荧光染色结合共聚焦显微镜定位IgD的核分布;ChIP-seq和ChIP-PCR检测IgD与靶基因启动子的结合;EMSA验证直接结合特异性;RT-PCR和免疫印迹检测靶基因E2f3a的表达变化。特异性方面,IgD仅在祖B细胞、前B细胞和成熟B细胞中表达,pre-pro-B细胞中无表达,且IgD特异性结合E2f3a的启动子区域,不结合E2f3b;敏感性方面,ChIP-seq显示IgD在E2f3a启动子区域的结合信号显著高于IgG对照。
核心成果为:核定位的IgD作为转录因子,通过直接结合E2f3a的启动子区域促进其表达,进而调控祖B细胞的细胞周期进程与增殖能力;IgD缺失导致祖B细胞中E2f3a表达显著降低(n=3,P<0.0001),细胞增殖能力下降(n=3,P<0.01),细胞周期阻滞于G0/G1期。该成果首次揭示了IgD在B细胞发育早期的非经典功能,突破了传统认为IgD仅作为成熟B细胞表面标记的认知,为B细胞发育的分子调控机制提供了新的核心靶点,也为免疫球蛋白家族的功能多样性提供了新的研究方向。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。