Multi-omics analysis of the HMGB2(+) tumor epithelial cells in lactylation subgroups in colorectal cancer.
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2025 | 起止号: | 2025 Nov 19; 15(1):158 |
| doi: | 10.1186/s13578-025-01491-x | ||
文献解析
1. 领域背景与文献
文献英文标题:Multi-omics analysis of the HMGB2+ tumor epithelial cells in lactylation subgroups in colorectal cancer;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肿瘤学(结直肠癌代谢重编程与表观调控)。
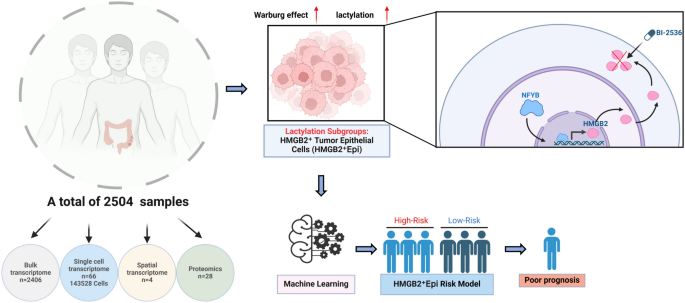
领域共识:结直肠癌是全球范围内发病率和死亡率最高的恶性肿瘤之一,近年来其发病呈年轻化趋势,严重威胁人类健康。目前结直肠癌的综合治疗方案包括手术、放疗、化疗、免疫治疗及靶向治疗,但肿瘤异质性导致的复发、远处转移和耐药问题仍是临床诊疗的主要瓶颈,深入解析结直肠癌进展的分子机制、挖掘新型诊疗靶点具有重要的临床价值。
肿瘤代谢重编程是恶性肿瘤的核心特征之一,其中糖酵解增强(Warburg效应)是结直肠癌的典型代谢表型,可导致肿瘤微环境中乳酸大量累积。2019年乳酸化被发现为一种新型蛋白质翻译后修饰,可通过调控染色质状态、基因转录等过程参与肿瘤发生发展、免疫逃逸等多个生物学过程,成为肿瘤代谢领域的研究热点。但目前结直肠癌中乳酸化的调控机制尚未完全阐明,尤其缺乏单细胞分辨率下的细胞亚群水平解析,无法明确乳酸化富集的特定肿瘤细胞亚群的功能及调控网络,同时缺乏基于乳酸化特征的预后评估模型和靶向干预策略,限制了其临床转化应用。
本研究针对上述领域空白,整合bulk转录组、单细胞RNA测序(scRNA-seq)、空间转录组、蛋白质组多组学数据,系统解析结直肠癌中的乳酸化景观,鉴定乳酸化富集的肿瘤上皮细胞亚群并阐明其调控机制,为结直肠癌的精准分层和靶向治疗提供新的理论依据和实践方案。
2. 文献综述解析
本研究的文献综述按研究方向划分为结直肠癌诊疗现状、肿瘤乳酸代谢与乳酸化修饰、HMGB2的肿瘤调控功能三大模块,系统梳理了领域内的研究进展与局限性。
现有研究在结直肠癌诊疗领域已取得显著进展:大规模筛查策略的推广显著提升了早期结直肠癌的诊断率,综合治疗方案的优化延长了中晚期患者的生存期,多组学技术的应用推动了结直肠癌分子分型的发展,为精准治疗奠定了基础。在乳酸化研究领域,现有研究已证实乳酸化在胰腺癌、肺癌、肝癌等多种肿瘤中通过调控细胞周期、免疫细胞功能等过程促进肿瘤进展,相关分子机制的揭示为肿瘤代谢干预提供了新的方向。在HMGB2研究领域,已明确HMGB2作为染色质结合蛋白参与DNA结构调控、基因转录、细胞周期调控等生物学过程,在多种肿瘤中高表达且与不良预后相关,可调控肿瘤细胞增殖、侵袭和耐药性。
现有研究仍存在多方面局限性:一是结直肠癌乳酸化研究多基于 bulk 水平分析,无法解析肿瘤异质性,缺乏对特定乳酸化富集细胞亚群的鉴定和功能研究;二是乳酸化在结直肠癌中的上游转录调控机制尚未阐明,代谢重编程与表观遗传修饰的耦合机制不明确;三是缺乏基于乳酸化特征的已验证预后评估模型和靶向干预药物,临床转化价值有限。
本研究的创新价值显著:首次在单细胞水平鉴定出结直肠癌中高乳酸化的HMGB2阳性肿瘤上皮细胞亚群,揭示了NFYB-HMGB2轴调控乳酸化和Warburg效应的全新分子机制,筛选出可靶向该轴的工具化合物BI-2536,构建的预后模型效能优于已发表的125种结直肠癌预后模型,填补了领域内的多项研究空白,为结直肠癌的精准诊疗提供了全新的靶点和策略。
3. 研究思路总结与详细解析
本研究的核心目标是解析结直肠癌中乳酸化相关肿瘤上皮细胞亚群的生物学功能及调控机制,核心科学问题为“HMGB2阳性肿瘤上皮细胞如何通过调控乳酸化和代谢重编程促进结直肠癌进展”,技术路线遵循“多组学数据整合→细胞亚群鉴定→功能验证→机制解析→药物筛选→模型构建”的闭环逻辑,研究结果严谨可靠。
3.1 结直肠癌乳酸化全景的多组学解析
实验目的:系统解析结直肠癌中乳酸化的表达特征、临床相关性及功能特征。
方法细节:整合TCGA结直肠癌队列(701例样本,含51例癌旁组织)和8个GEO结直肠癌bulk转录组队列(共1705例样本),采用sva R包进行批次校正后合并为统一分析队列;纳入4个GEO单细胞转录组队列(共66例样本,含47例肿瘤、19例癌旁),采用harmony R包进行批次整合,Seurat R包进行质量控制和细胞注释;纳入4个已发表的结直肠癌空间转录组队列用于空间定位验证。基于文献报道的332个乳酸化相关基因,采用单样本基因集富集分析(ssGSEA)计算每个样本/细胞的乳酸化评分,通过差异分析、生存分析、基因集变异分析(GSVA)解析乳酸化的临床意义和富集通路。
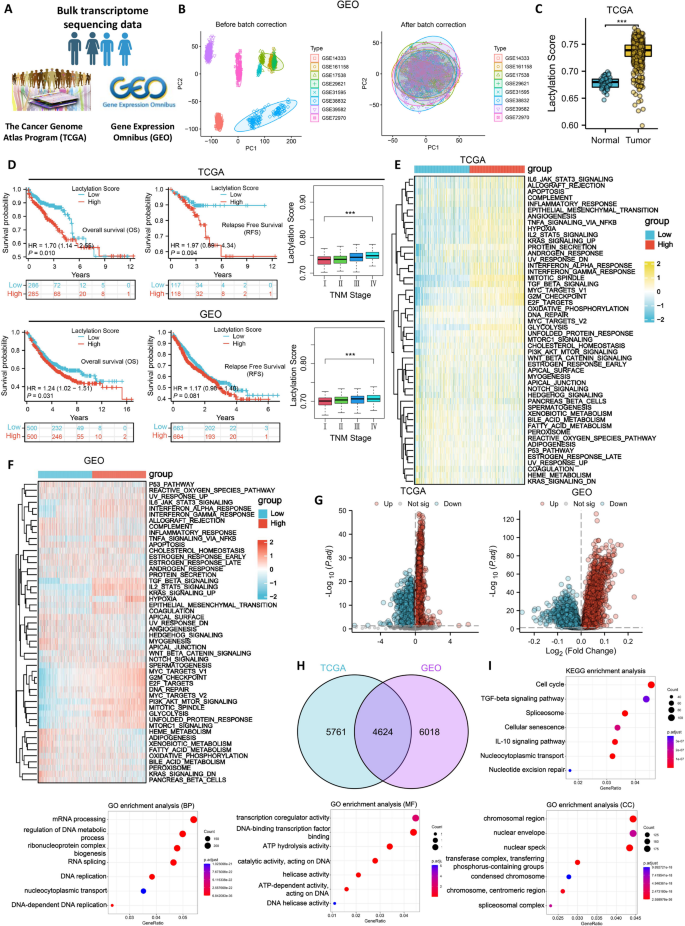
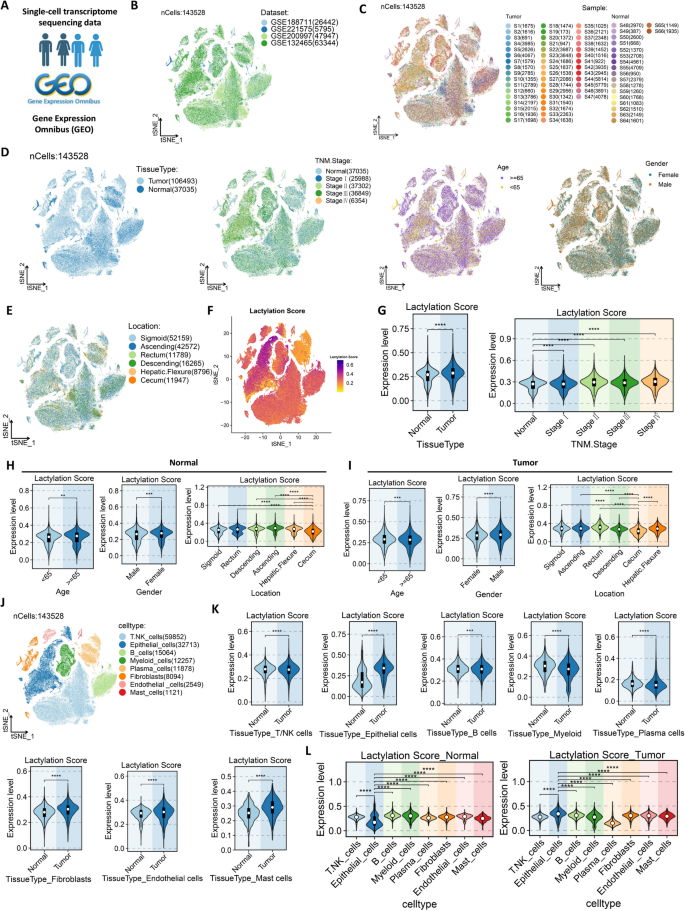
结果解读:bulk队列分析显示,肿瘤组织的乳酸化评分显著高于癌旁组织(P<0.01),高乳酸化评分患者的总生存期(OS)和无复发生存期(RFS)显著短于低评分患者(P<0.001),高乳酸化组显著富集于G2M检查点、MYC靶点、E2F靶点、IL6-JAK-STAT3信号、缺氧等与肿瘤恶性进展相关的通路。单细胞转录组分析显示,肿瘤组织的乳酸化评分显著高于癌旁组织,且随TNM分期升高而升高;8种主要细胞类型中,肿瘤上皮细胞的乳酸化评分最高,其中恶性上皮细胞的乳酸化水平显著高于非恶性上皮细胞(P<0.001)。
产品关联:文献未提及具体实验产品,领域常规使用转录组测序试剂盒、单细胞转录组测序平台、R语言分析软件包(sva、harmony、Seurat、GSVA等)。
3.2 乳酸化相关肿瘤上皮细胞亚群的鉴定
实验目的:在单细胞水平鉴定乳酸化富集的肿瘤上皮细胞亚群并分析其生物学特征。
方法细节:对单细胞转录组数据中的上皮细胞进行重聚类,获得11个上皮亚群(Epi_1至Epi_11);采用copycat算法推断拷贝数变异(CNV),区分恶性与非恶性上皮细胞;通过高维加权基因共表达网络分析(hdWGCNA)筛选各上皮亚群的核心基因集,进行GO/KEGG功能富集分析和基因集富集分析(GSEA);结合空间转录组数据验证目标亚群与乳酸化信号的空间共定位;采用ssGSEA计算bulk队列中目标亚群的浸润评分,分析其与患者预后的相关性。
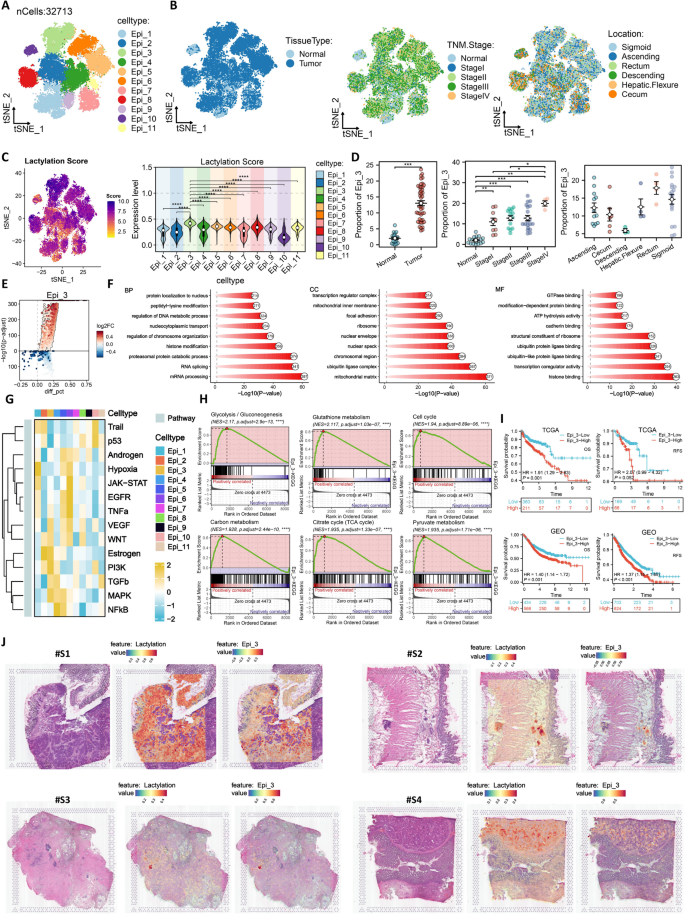
结果解读:11个上皮亚群中,Epi_3亚群的乳酸化评分最高(P<0.001),且在肿瘤组织、晚期TNM分期、直肠组织中的占比最高;CNV分析显示Epi_3亚群中90%以上为恶性上皮细胞,仅存在少量非恶性细胞,作者推测这些非恶性细胞可能处于正常向恶性转化的中间状态,或为受肿瘤旁分泌信号影响的正常上皮细胞。功能富集分析显示Epi_3亚群显著富集于糖酵解、氧化磷酸化、MAPK信号、PI3K信号等与代谢重编程和恶性进展相关的通路。生存分析显示,Epi_3浸润评分高的患者OS和RFS显著更短(P<0.01)。空间转录组数据证实Epi_3亚群与乳酸化信号存在显著的空间共定位。
产品关联:文献未提及具体实验产品,领域常规使用空间转录组测序平台、copycat、hdWGCNA等分析软件包。
3.3 HMGB2阳性上皮细胞(HMGB2+Epi)的定义与体外验证
实验目的:明确Epi_3亚群的核心标志物并验证其表达特征。
方法细节:取hdWGCNA筛选的Epi_3核心基因与Epi_3差异高表达基因(log2FC>1,P<0.05)的交集,获得候选标志物;通过TCGA、UALCAN、Human Protein Atlas(HPA)公共数据库验证候选标志物的表达差异及与乳酸化评分的相关性;收集28例结直肠癌患者的配对癌与癌旁组织,采用免疫组化(IHC)、蛋白免疫印迹(WB)验证标志物的表达水平和细胞定位;检测1株正常结肠上皮细胞系(NCM460)和8株结直肠癌细胞系的标志物表达和乳酸化水平,采用CRISPR-Cas9技术构建HMGB2敲除的DLD1稳定细胞系,采用慢病毒转染构建HMGB2过表达的SW620稳定细胞系,通过蛋白免疫印迹验证基因编辑效率。
结果解读:交集分析获得5个候选基因,其中HMGB2与Epi_3浸润评分的相关性最高(R>0.8,P<0.001),且在Epi_3亚群中特异性高表达(log2FC=1.9,P<0.001),因此将Epi_3亚群定义为HMGB2阳性上皮细胞(HMGB2+Epi)。公共数据库验证显示,HMGB2在结直肠癌组织的RNA和蛋白水平均显著高于癌旁组织(P<0.001),且与乳酸化评分呈显著正相关(R>0.6,P<0.01)。临床样本验证显示,HMGB2主要定位于肿瘤细胞核,在癌组织中的表达较癌旁组织上调2.7倍(n=28,P<0.001),且癌组织的乳酸化水平显著高于癌旁组织(n=28,P<0.001)。细胞系验证显示,DLD1细胞的HMGB2和乳酸化水平最高,SW620细胞最低,成功构建的HMGB2敲除/过表达细胞系的基因编辑效率符合后续实验要求。
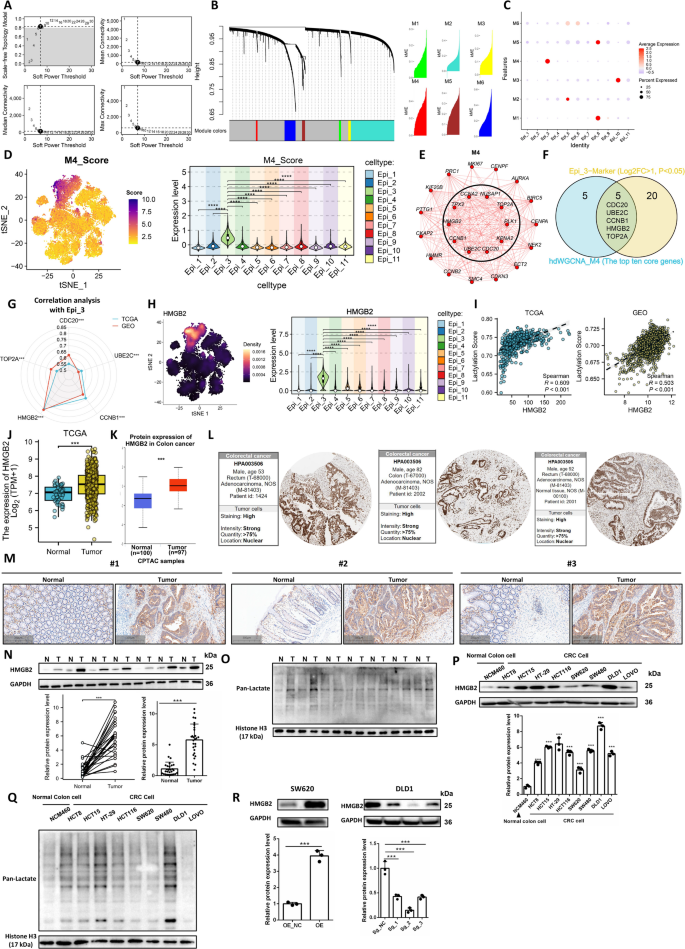
产品关联:实验所用关键产品:Abcam的HMGB2抗体(货号ab124670)、ABclonal的泛乳酸化抗体(货号A23004)、CRISPR-Cas9基因编辑试剂盒、慢病毒包装载体。
3.4 HMGB2调控结直肠癌恶性表型的功能验证
实验目的:明确HMGB2对结直肠癌细胞乳酸化、Warburg效应及恶性生物学行为的调控作用。
方法细节:在HMGB2过表达/敲除细胞系中,采用蛋白免疫印迹检测乳酸化水平和Warburg效应相关蛋白(FBP1、HK2、LDHA、PKM2)的表达;采用Transwell实验检测细胞的迁移和侵袭能力,采用CCK-8实验、克隆形成实验检测细胞增殖能力,采用Annexin V-FITC/PI双染流式细胞术检测细胞凋亡水平;采用裸鼠皮下成瘤实验验证HMGB2对体内肿瘤生长的调控作用,取瘤组织进行苏木精-伊红(H&E)染色和Ki67免疫组化分析增殖水平。
结果解读:HMGB2过表达可使细胞乳酸化水平显著升高,糖异生相关蛋白FBP1表达下调,糖酵解相关蛋白HK2、LDHA、PKM2表达上调(n=3,P<0.01),证实HMGB2可激活Warburg效应。功能实验显示,HMGB2敲除后细胞的迁移和侵袭能力下降42%(n=3,P<0.001),克隆形成能力下降36%(n=3,P<0.01),凋亡率升高2.1倍(n=3,P<0.001);HMGB2过表达可显著增强细胞的迁移、侵袭和增殖能力。裸鼠成瘤实验显示,HMGB2过表达组的肿瘤体积和重量为对照组的2.3倍(n=4,P<0.01),HMGB2敲除组的肿瘤体积和重量较对照组下降62%(n=4,P<0.001),Ki67免疫组化结果显示肿瘤增殖能力与HMGB2表达水平呈显著正相关。
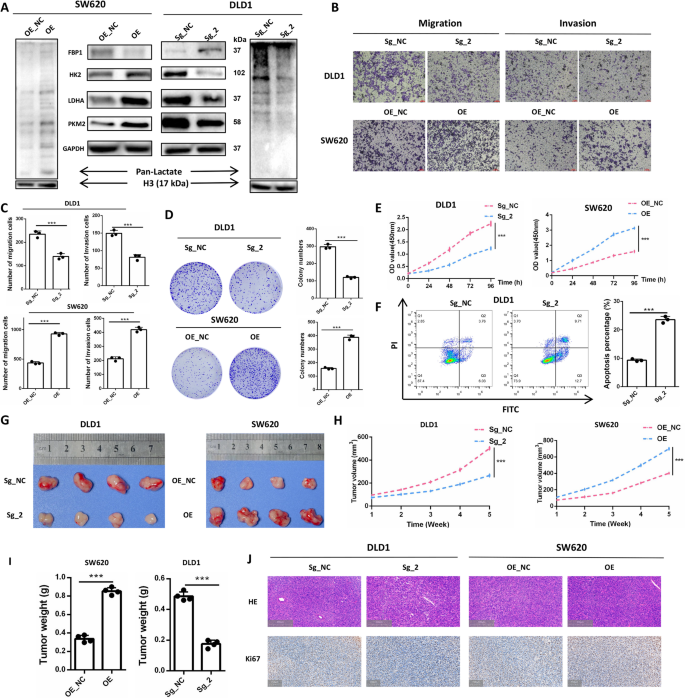
产品关联:实验所用关键产品:ABclonal的FBP1抗体(货号A11664)、HK2抗体(货号A22319)、LDHA抗体(货号A20991)、PKM2抗体(货号A20991)、Corning的Transwell小室(货号3422)、Dojindo的CCK-8试剂盒、碧云天的Annexin V-FITC/PI凋亡检测试剂盒。
3.5 NFYB-HMGB2调控轴的机制解析
实验目的:阐明HMGB2的上游转录调控机制及功能效应。
方法细节:采用SCENIC方法分析上皮亚群的转录因子调控网络,筛选HMGB2+Epi的核心转录因子;采用JASPAR数据库预测转录因子与HMGB2启动子的结合位点,通过染色质免疫共沉淀(ChIP)-qPCR验证结合作用;采用siRNA敲低NFYB表达,结合HMGB2回补实验,通过蛋白免疫印迹检测乳酸化和Warburg效应相关蛋白的表达,通过CCK-8、Transwell实验检测细胞增殖、迁移和侵袭能力的变化。
结果解读:SCENIC分析显示,NFYB是HMGB2+Epi中活性最高的转录因子,其表达水平与HMGB2表达、乳酸化评分均呈显著正相关(R>0.7,P<0.01)。JASPAR数据库预测NFYB在HMGB2启动子区存在结合基序TTATTGGTC,ChIP-qPCR验证显示NFYB可显著富集该区域(富集倍数为8.7,n=3,P<0.001),证实NFYB直接结合HMGB2启动子并调控其转录。功能回补实验显示,NFYB敲低可显著下调HMGB2表达,降低乳酸化水平,抑制Warburg效应,使细胞增殖、迁移和侵袭能力下降47%(n=3,P<0.001);回补HMGB2表达可逆转上述表型,证实NFYB-HMGB2轴是调控结直肠癌乳酸化和恶性进展的核心通路。
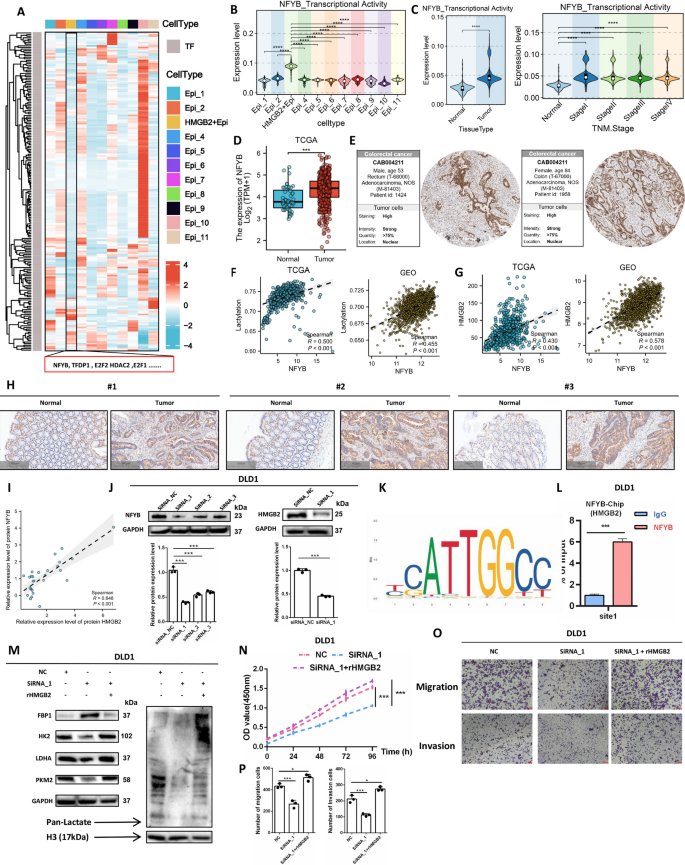
产品关联:实验所用关键产品:Abcam的NFYB抗体(货号ab6559)、Millipore的ChIP试剂盒、吉玛基因的NFYB siRNA。
3.6 HMGB2+Epi的细胞间通讯分析
实验目的:解析HMGB2+Epi与肿瘤微环境其他细胞的相互作用模式。
方法细节:采用CellChat R包分析11个上皮亚群与7种微环境细胞(肥大细胞、成纤维细胞、髓系细胞、B细胞、T/NK细胞、浆细胞、内皮细胞)的通讯网络,基于CellChatDB.human配体-受体数据库计算细胞间通讯概率,可视化互作网络和配体-受体对。
结果解读:与其他低乳酸化上皮亚群相比,HMGB2+Epi的信号发送和接收能力显著更强,与成纤维细胞、内皮细胞、T/NK细胞的互作强度最高,富集多种配体-受体对参与肿瘤微环境重塑、血管生成和免疫调控,提示HMGB2+Epi可通过与微环境细胞的互作促进结直肠癌进展。
产品关联:文献未提及具体实验产品,领域常规使用CellChat R软件包。
3.7 HMGB2潜在靶向药物筛选与验证
实验目的:筛选靶向HMGB2-乳酸化轴的小分子化合物并验证其作用效果。
方法细节:采用oncoPredict R包分析TCGA和GEO队列中198种药物的IC50与HMGB2表达的相关性,筛选呈显著负相关的候选药物(R<-0.3,P<0.05);采用CB-Dock2平台进行分子对接,计算药物与HMGB2的结合能,选择结合能最低的化合物进行100ns分子动力学模拟,通过均方根偏差(RMSD)、均方根波动(RMSF)、氢键分析等评估结合稳定性;采用细胞活力实验检测候选药物对DLD1细胞的IC50,通过蛋白免疫印迹检测药物处理后HMGB2和乳酸化水平的变化。
结果解读:共筛选出6种与HMGB2表达负相关的候选药物,其中BI-2536与HMGB2的结合能最低(Vina score=-9.2 kcal/mol)。分子动力学模拟显示,BI-2536与HMGB2的复合物在20ns后达到稳定结合状态,存在动态氢键相互作用,整体结构紧凑性良好。体外实验显示,BI-2536对DLD1细胞的IC50为68.16nmol,IC50浓度处理可使HMGB2蛋白水平下降65%(n=3,P<0.01),乳酸化水平显著降低,证实BI-2536可作为研究HMGB2-乳酸化轴的工具化合物,但其是否为HMGB2的直接抑制剂仍需进一步验证。
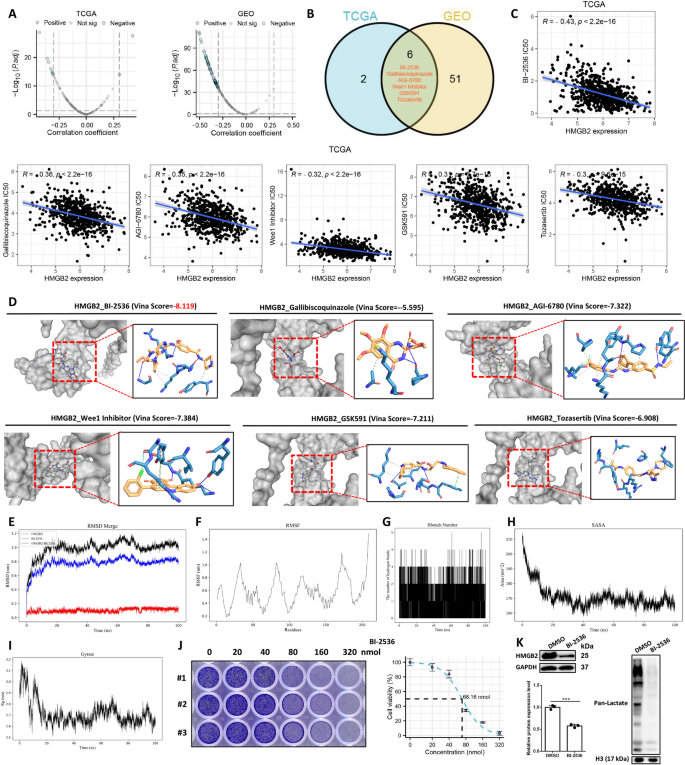
产品关联:实验所用关键产品:MCE的BI-2536(货号HY-50698)、分子对接与模拟软件(CB-Dock2、GROMACS 2022)。
3.8 HMGB2+Epi相关预后模型的构建与验证
实验目的:构建基于HMGB2+Epi特征的结直肠癌预后风险模型并验证其临床效能。
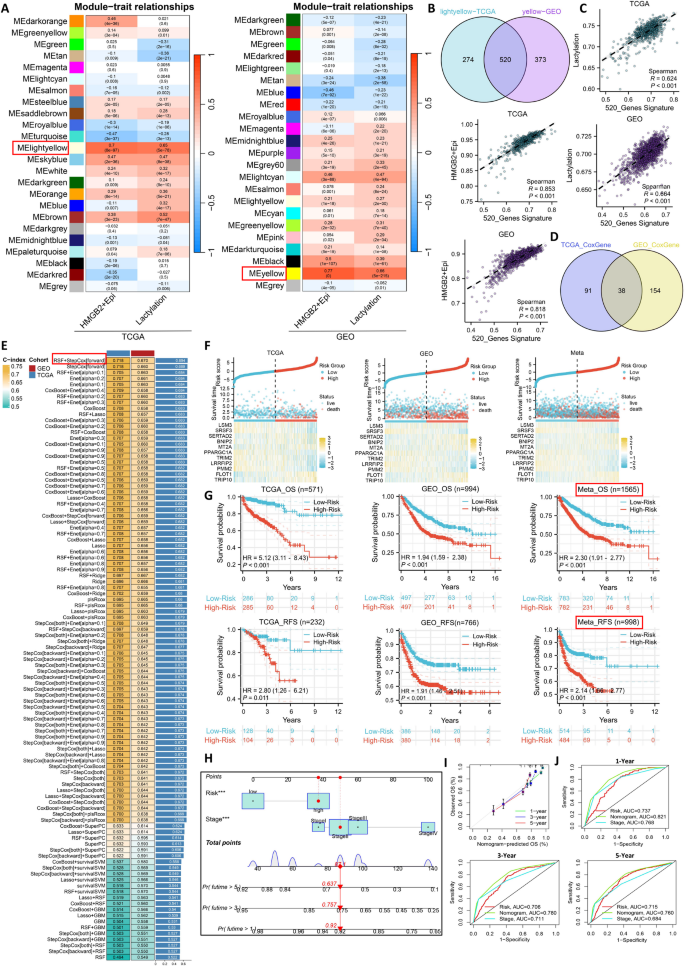
方法细节:采用加权基因共表达网络分析(WGCNA)筛选TCGA和GEO队列中与HMGB2+Epi浸润评分、乳酸化评分均显著相关的共表达基因模块,取交集基因进行单因素Cox回归分析,筛选与预后显著相关的基因作为特征集;采用10种机器学习方法的101种算法组合构建风险模型,以TCGA队列为训练集、GEO队列为验证集,选择C-index最高的算法组合构建最终模型;在TCGA、GEO及整合队列中验证模型的预后效能,与125种已发表的结直肠癌预后模型比较C-index;结合TNM分期构建列线图,通过校准曲线、时间依赖性ROC曲线评估模型的预测性能。
结果解读:最终采用RSF+StepCox算法构建的风险模型包含11个特征基因(TRIP10、FLOT1、PMM2、LRRFIP2、TRIM2、PPARGC1A、MT2A、BNIP2、SERTAD2、SRSF3、LSM3)。生存分析显示,高风险评分患者的OS和RFS显著低于低风险患者(P<0.001);该模型在TCGA、GEO、整合队列中的C-index分别为0.76、0.74、0.75,均优于125种已发表的结直肠癌预后模型。结合TNM分期构建的列线图预测1、3、5年OS的AUC分别为0.82、0.79、0.77,显著优于单独使用风险评分或TNM分期,校准曲线显示模型预测值与实际观测值一致性良好。
产品关联:文献未提及具体实验产品,领域常规使用机器学习相关R软件包(randomForestSRC、survival、rms等)。
4. Biomarker 研究及发现成果
本研究涉及两类核心生物标志物,分别为细胞亚群标志物HMGB2和预后风险标志物11基因特征集,两类标志物的筛选均遵循“多组学筛选→多水平验证→独立队列验证”的严谨逻辑,具有较高的可靠性和临床转化潜力。
HMGB2属于细胞亚群特异性标志物,为核定位蛋白,是HMGB2+Epi的核心特征分子,其筛选逻辑为:首先通过单细胞亚群差异分析筛选Epi_3的高表达基因,再通过hdWGCNA筛选Epi_3的核心共表达基因,取交集后通过多队列相关性验证确定HMGB2为最优标志物。HMGB2的验证来源包括公共数据库的转录组/蛋白组数据、28例临床配对组织样本、9株细胞系的蛋白表达数据,验证方法包括转录组差异分析、免疫组化、蛋白免疫印迹等。结果显示,HMGB2在结直肠癌组织中的表达较癌旁组织上调2.7倍(n=28,P<0.001),与乳酸化评分的相关系数为0.68(P<0.001),高表达患者的无复发生存期显著缩短(HR=1.89,P=0.002),可作为结直肠癌乳酸化状态和不良预后的指示标志物。
11基因预后模型属于预后风险标志物,其筛选逻辑为:通过WGCNA筛选与HMGB2+Epi和乳酸化均相关的共表达基因,经单因素Cox回归筛选预后相关基因后,通过机器学习算法优化特征组合,最终确定11个特征基因。该模型的验证基于TCGA、8个独立GEO队列共2406例样本,验证方法包括生存分析、C-index比较、ROC曲线分析、校准曲线分析等。结果显示,该模型预测5年总生存期的AUC为0.77(95%CI 0.72-0.82),在多独立队列中的C-index均高于125种已发表的结直肠癌预后模型,结合TNM分期的列线图可进一步提升预测效能,适用于结直肠癌患者的预后分层和个体化治疗决策。
此外,本研究筛选出的工具化合物BI-2536可显著下调HMGB2表达和乳酸化水平,对DLD1细胞的IC50为68.16nmol(n=3,P<0.01),为后续HMGB2-乳酸化轴的靶向药物研发提供了先导结构。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。
