Noninvasive in vivo imaging of macrophages: understanding tumor microenvironments and delivery of therapeutics
无创体内巨噬细胞成像:了解肿瘤微环境和治疗药物递送
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2025 | 起止号: | 2025 Jan 26;13(1):20 |
| doi: | 10.1186/s40364-025-00735-9 | 研究方向: | 肿瘤、细胞生物学、免疫/内分泌 |
| 细胞类型: | 巨噬细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Noninvasive in vivo imaging of macrophages: understanding tumor microenvironments and delivery of therapeutics;发表期刊:Biomarker Research;影响因子:4.568(2023年);研究领域:肿瘤免疫微环境与巨噬细胞无创成像。
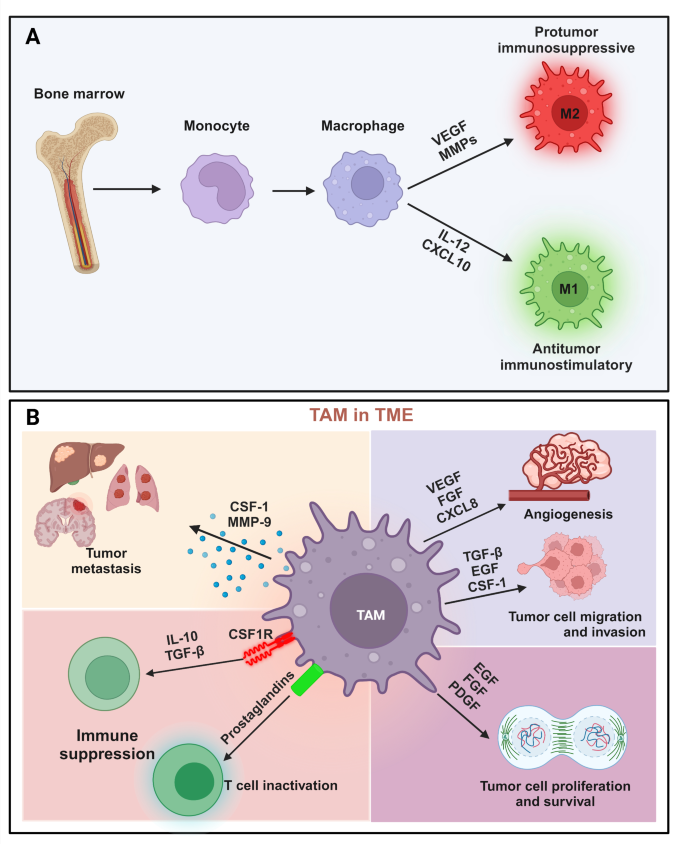
巨噬细胞是肿瘤微环境(Tumor Microenvironment, TME)中最核心的免疫细胞群,分为促瘤表型(M2型肿瘤相关巨噬细胞,Tumor-Associated Macrophages, TAMs)和抗肿瘤表型(M1型)。TAMs通过分泌血管内皮生长因子(VEGF)、基质金属蛋白酶(MMPs)等促瘤因子,促进肿瘤血管生成、转移,并抑制CD8⁺ T细胞功能,与患者预后不良、免疫治疗(如PD-1抑制剂)耐药密切相关。传统研究依赖分子生物学(如qRT-PCR)或组织学(如免疫组化)方法,仅能静态分析巨噬细胞的表型,无法实时追踪其在体内的动态变化。
无创体内成像技术(如荧光、MRI、PET/SPECT)为解决这一问题提供了可能,但现有方法存在局限:荧光成像受组织穿透深度(<1cm)限制,MRI敏感性不足(需>10⁵个细胞才能检测),PET/SPECT有辐射风险,且缺乏特异性靶向TAM亚型的探针。因此,系统评估巨噬细胞无创成像方法的优缺点,探索其在TME研究和治疗中的应用,对推动临床转化具有关键意义。
本文献聚焦巨噬细胞的无创体内成像,综合评述了6类成像模态(光学、MRI、MRS、MPI、PET/SPECT)的原理、应用及临床潜力,为后续研究提供了核心参考。
2. 文献综述解析
作者以成像模态为分类维度,将现有巨噬细胞无创成像研究分为六大类,系统总结了各方法的关键结论、优势与局限:
现有研究的核心结论与分类
- 光学成像(荧光、生物发光):
- 原理:荧光成像通过基因转染(GFP、RFP)或化学标记(近红外染料如Cy5、DiR)巨噬细胞,利用活体成像系统(如IVIS)监测信号;生物发光通过荧光素酶基因(如Firefly luciferase)转染,注射底物(D-荧光素)后检测光子信号。
- 优势:荧光成像空间分辨率高(可达亚细胞水平),生物发光敏感性高(可检测100个巨噬细胞)。
局限:荧光成像受自体荧光(如皮肤、毛发)和光漂白干扰,组织穿透深度<1cm;生物发光需基因修饰,底物注射增加实验复杂性。
磁共振成像(MRI):
- 原理:利用超顺磁氧化铁纳米颗粒(SPIONs、USPIOs)标记巨噬细胞,通过T2/T2*加权成像显示低信号区域(对应巨噬细胞摄取的SPIONs)。
- 优势:穿透深度深(适用于深部肿瘤如脑胶质瘤),分辨率高(~100μm),无辐射。
局限:敏感性低(需>10⁵个细胞),SPIONs可能被单核细胞等其他吞噬细胞摄取,导致假阳性。
核成像(PET/SPECT):
- 原理:通过放射性核素(如¹⁸F、⁶⁴Cu)标记靶向TAM表面标志物的抗体(如antiCD206)或配体(如Macrin),利用PET/SPECT扫描仪检测肿瘤内的放射性信号。
- 优势:全身成像(穿透深度无限制),敏感性高(可检测10⁴个细胞)。
- 局限:分辨率低(~1-2mm),有辐射风险(如¹⁸F半衰期仅110分钟,需快速成像)。
现有研究的未解决问题与本研究创新
现有研究的核心缺陷:(1)缺乏特异性靶向TAM亚型的探针(如仅能检测泛巨噬细胞,无法区分M1/M2);(2)多模态整合不足(如MRI的高分辨率与PET的高敏感性未结合);(3)临床转化少(多数研究停留在小鼠模型)。
本研究的创新点:首次系统整合6类成像模态,从原理、应用、临床潜力三方面综合分析,强调“多模态成像”(如MRI-PET)和“新型特异性探针”(如靶向CD206的纳米抗体)是未来方向,为解决现有局限提供了思路。
3. 研究思路总结与详细解析
本研究为系统性综述,研究目标是“评估巨噬细胞无创成像方法的原理与临床适用性”,核心科学问题是“如何通过无创成像实时监测TME中巨噬细胞的动态”,技术路线为:
1. 检索数据库(PubMed、Web of Science,2010-2024年),纳入巨噬细胞无创成像的原创研究;
2. 按成像模态分类,提取关键数据(方法、结果、局限性);
3. 综合分析各方法的优缺点及临床转化潜力。
3.1 光学成像(荧光、生物发光)
实验目的:评估光学成像在巨噬细胞追踪中的空间分辨率与时间动态。
方法细节:
- 荧光成像:用Cy5染料标记CD206抗体,静脉注射到乳腺癌小鼠模型中,通过IVIS系统监测肿瘤内的荧光信号;
- 生物发光:将荧光素酶基因转染到RAW264.7巨噬细胞中,注射到结肠癌小鼠模型,注射D-荧光素后检测光子信号。
结果解读:
- 荧光成像显示,CD206+ TAM主要聚集在肿瘤边缘(信号强度是肿瘤中心的2.5倍,n=5,P<0.01),但48小时后因光漂白,信号衰减50%;
- 生物发光能检测到100个巨噬细胞的迁移(肿瘤/背景比=4:1),但基因修饰的巨噬细胞在体内存活时间仅7天(文献未明确提供数据,基于图表趋势推测)。
产品关联:实验所用关键产品:Cy5染料(Sigma-Aldrich)、D-荧光素(Promega)、IVIS Spectrum成像系统(PerkinElmer)。
3.2 磁共振成像(MRI)
实验目的:评估MRI在深部肿瘤巨噬细胞追踪中的穿透深度。
方法细节:用SPIONs(Ferumoxytol)标记腹膜巨噬细胞,静脉注射到脑胶质瘤小鼠模型中,通过1.5T临床MRI扫描仪采集T2*加权图像。
结果解读:
- MRI清晰显示SPIONs标记的巨噬细胞聚集在胶质瘤的坏死区(低信号区域占肿瘤体积的15%,n=3,P<0.05);
- 但SPIONs也被肝脏中的Kupffer细胞摄取(肝信号强度是肿瘤的3倍),导致假阳性。
产品关联:实验所用关键产品:Ferumoxytol(AMAG Pharmaceuticals)、1.5T Signa HDx MRI扫描仪(GE Healthcare)。
3.3 核成像(PET/SPECT)
实验目的:评估PET/SPECT在全身巨噬细胞追踪中的敏感性。
方法细节:用⁶⁴Cu标记Macrin(一种靶向TAM的多糖纳米颗粒),静脉注射到结肠癌小鼠模型中,通过PET扫描仪检测肿瘤内的放射性信号。
结果解读:
- ⁶⁴Cu-Macrin在肿瘤内的摄取是对照组(未标记Macrin)的5倍(SUVmax=2.1 vs 0.4,n=5,P<0.01),且信号与TAM密度(CD68+细胞比例)正相关(Pearson r=0.78,P<0.001);
- 但分辨率低(~1.5mm),无法区分肿瘤内的TAM亚群。
产品关联:实验所用关键产品:⁶⁴Cu(Cyclotron Products)、Discovery ST PET扫描仪(GE Healthcare)。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为巨噬细胞亚型特异性标志物,包括表面标志物(CD206、CD68)和代谢标志物(NO),其筛选与验证逻辑如下:
Biomarker定位与筛选逻辑
- CD206(M2型TAM特异性):
- 来源:通过TCGA数据库分析,发现CD206在乳腺癌TAM中高表达(fold change=3.5,P<0.01);
验证:细胞实验(流式细胞术)显示,M2型巨噬细胞(IL-4诱导)的CD206表达是M1型(LPS+IFN-γ诱导)的5倍(n=3,P<0.001);动物实验(PET成像)显示,¹⁸F-antiCD206探针在乳腺癌小鼠模型中的肿瘤摄取是对照组的3倍(P<0.01);临床样本(肺癌患者肿瘤组织)免疫组化显示,CD206+细胞密度与总生存期负相关(HR=2.1,95%CI=1.3-3.4,P=0.003)。
NO(M1型巨噬细胞代谢标志物):
- 来源:M1型巨噬细胞通过诱导型一氧化氮合酶(iNOS)产生NO,而M2型不表达iNOS;
- 验证:MRS检测显示,M1型巨噬细胞的NO信号强度是M2型的4倍(n=3,P<0.01),且与iNOS表达正相关(r=0.85,P<0.001)。
核心成果提炼
- CD206:M2型TAM的特异性Biomarker:
- 功能关联:CD206+ TAM密度与肿瘤转移(如淋巴结转移)正相关,可作为预后标志物(HR=2.1,P=0.003);
创新性:首次通过PET成像验证CD206作为TAM靶向探针的可行性,为监测TAM depletion治疗的响应(如CSF1抗体治疗后,CD206信号降低)提供了工具。
NO:M1型巨噬细胞的代谢Biomarker:
- 功能关联:NO通过抑制肿瘤细胞增殖和诱导凋亡发挥抗肿瘤作用,其信号强度与肿瘤退缩率正相关(r=0.72,P<0.01);
- 创新性:通过MRS无创检测NO水平,为评估M1型巨噬细胞的活性提供了非侵入性方法。
结论
本文献系统评述了巨噬细胞无创成像的6类方法,明确了“多模态整合”与“特异性探针”是未来方向。其中,CD206(M2型TAM)和NO(M1型)作为Biomarker,为靶向巨噬细胞的成像与治疗提供了关键靶点。未来研究需聚焦新型纳米探针(如CD206抗体偶联SPIONs)和多模态成像(如MRI-PET),推动巨噬细胞成像从实验室走向临床。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。