Therapeutic potential of folic acid supplementation for cardiovascular disease prevention through homocysteine lowering and blockade in rheumatoid arthritis patients
叶酸补充剂通过降低同型半胱氨酸水平和阻断类风湿性关节炎患者的同型半胱氨酸信号通路,在预防心血管疾病方面具有治疗潜力
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2015 | 起止号: | 2015;3:24 |
| doi: | 10.1186/s40364-015-0049-9 | 研究方向: | 心血管、信号转导 |
| 疾病类型: | 关节炎、心血管疾病 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Therapeutic potential of folic acid supplementation for cardiovascular disease prevention through homocysteine lowering and blockade in rheumatoid arthritis patients;发表期刊:Biomarker Research;影响因子:未公开;研究领域:类风湿关节炎合并心血管疾病的预防及生物标志物研究。
类风湿关节炎(RA)是一种以慢性对称性侵蚀性滑膜炎为特征的系统性炎症疾病,主要累及外周关节,全球患病率约0.5-1%。现有研究一致表明,RA患者发生心肌梗死、卒中、深静脉血栓等心血管疾病(CVD)的风险是普通人群的2倍,心血管死亡风险较普通人群增加60%(文献引用1-3)。除年龄、高血压、糖尿病等传统心血管风险因素外,RA特有的系统性炎症介质(如肿瘤坏死因子α[TNF-α]、白细胞介素-6[IL-6])是CVD风险增加的核心驱动因素——炎症通过促进氧化应激、内皮功能障碍、脂质过氧化及血栓形成,直接参与CVD的发生发展(文献引用1、37-38)。
同型半胱氨酸(Hcy)是蛋氨酸代谢的中间产物,其血浆浓度受B族维生素(叶酸、维生素B6、B12)摄入、遗传突变(如甲基四氢叶酸还原酶[MTHFR] 677C>T突变)、药物(如甲氨蝶呤)及疾病状态的影响。高同型半胱氨酸血症(HHcy,血浆Hcy≥15μM)是普通人群CVD的明确风险因子,可通过氧化应激、抑制一氧化氮(NO)合成、增加不对称二甲基精氨酸(ADMA)等机制导致内皮功能障碍及动脉粥样硬化(文献引用4-5)。而RA患者中HHcy的发生率高达20-42%(远高于普通人群的5-7%),主要由以下因素引起:① 炎症激活导致B族维生素消耗(炎症细胞的快速增殖及氧化应激靶向破坏B族维生素);② 疾病修饰抗风湿药(DMARDs,如甲氨蝶呤)抑制叶酸代谢;③ 遗传突变(如MTHFR 677C>T导致酶活性降低,阻碍Hcy甲基化)(文献引用7-28)。
尽管HHcy在RA中的发生率显著升高,但现有研究存在两大空白:一是RA患者中HHcy与CVD的因果关系尚未明确(仅少数队列研究提示HHcy可能预测CVD事件);二是叶酸补充通过降低HHcy预防RA患者CVD的疗效缺乏大样本验证。因此,本研究旨在系统综述叶酸补充通过降低Hcy及阻断其心血管损伤作用,在RA患者CVD预防中的治疗潜力,为RA患者的CVD精准预防提供理论依据。
2. 文献综述解析
作者对现有研究的分类维度主要围绕“RA患者CVD风险的来源”“HHcy在RA中的发生机制”“HHcy与CVD的关联”“叶酸补充的CVD预防效果”四大核心问题展开,形成了逻辑严密的综述框架。
现有研究的关键结论可归纳为四点:① RA患者CVD风险升高的核心驱动是炎症——炎症介质通过促进氧化应激、内皮功能障碍及脂质过氧化,直接参与动脉粥样硬化形成(文献引用1、37-38);② RA患者中HHcy是多因素共同作用的结果——遗传突变(MTHFR 677C>T)、炎症激活(B族维生素消耗)、DMARDs药物(甲氨蝶呤抑制叶酸代谢)均会导致Hcy代谢障碍(文献引用7-28);③ HHcy与CVD的关联具有“人群特异性”——普通人群中HHcy通过氧化应激、ADMA升高及血栓形成导致CVD,而RA患者中HHcy与炎症形成“双向恶性循环”(HHcy加重炎症,炎症进一步消耗B族维生素加剧HHcy),从而放大CVD风险(文献引用8、11);④ 叶酸补充的CVD预防效果存在“部位差异”——普通人群的meta分析显示,叶酸补充可降低7%的卒中风险(RR=0.93,95%CI 0.86-1.00,p=0.05),但对冠心病无显著效果;RA患者中,甲氨蝶呤联合叶酸治疗的死亡风险(HR=0.2)显著低于单独甲氨蝶呤治疗(HR=0.5),提示叶酸可能通过降低HHcy改善预后(文献引用55、58、66)。
现有研究的局限性在于:RA患者中HHcy与CVD的因果关系未得到大样本临床试验验证,叶酸补充的最佳剂量、频率及长期效果仍不明确。本研究的创新点在于首次系统整合了RA患者中HHcy的发生机制、与CVD的关联及叶酸补充的潜在疗效证据,明确提出叶酸补充可能通过“降低Hcy+阻断氧化应激/内皮功能障碍”双途径,成为RA患者CVD预防的潜在策略,并强调了开展大样本长期临床试验的必要性。
3. 研究思路总结与详细解析
本研究为系统综述,整体框架遵循“提出问题→回顾证据→综合分析→提出结论”的逻辑闭环:首先明确RA患者CVD风险高且HHcy发生率高的临床问题,随后回顾HHcy在RA中的发生机制、与CVD的关联及叶酸补充的效果,最后综合分析叶酸补充的治疗潜力及研究方向。以下分环节解析:
3.1 RA患者CVD风险及炎症机制的文献回顾
实验目的:总结RA患者CVD风险升高的原因及炎症在其中的核心作用。
方法细节:回顾了10余项队列研究及meta分析,包括RA患者与普通人群CVD发生率的比较研究(如对235例RA患者随访6.5年的队列研究),以及炎症标志物(TNF-α、IL-6)与CVD关联的研究。
结果解读:现有研究一致显示,RA患者心肌梗死、卒中的风险是普通人群的2倍,心血管死亡风险增加60%(文献引用1-3)。调整传统心血管风险因素后,TNF-α、IL-6等炎症标志物仍是CVD风险的独立预测因子——炎症通过促进氧化应激(抑制谷胱甘肽过氧化物酶活性)、内皮功能障碍(降低NO生物利用度)及脂质过氧化(ox-LDL升高),直接参与动脉粥样硬化的发生(文献引用37-38、44-47)。
产品关联:文献未提及具体实验产品,领域常规使用炎症因子检测试剂盒(如TNF-α、IL-6 ELISA试剂盒)、内皮功能检测设备(如Flow-mediated dilation超声仪)等。
3.2 HHcy在RA中的发生机制及与CVD关联的文献整合
实验目的:解析RA患者中HHcy的发生机制,及HHcy与CVD的关联。
方法细节:整合了RA患者HHcy的遗传因素(MTHFR 677C>T突变)、非遗传因素(炎症、DMARDs药物)研究,以及HHcy与RA患者CVD事件关联的队列研究(如235例RA患者的6.5年随访研究)。
结果解读:RA患者中HHcy的发生是“遗传+环境”共同作用的结果:① 遗传上,MTHFR 677C>T突变导致酶活性降低50%,阻碍Hcy甲基化为蛋氨酸(文献引用8);② 疾病炎症激活——CD4+CD28-细胞产生干扰素γ(IFN-γ),促进Th1细胞分泌TNF-α、IL-6,这些炎症因子一方面通过氧化应激靶向破坏B族维生素(包括叶酸),另一方面增加免疫细胞增殖需求,进一步消耗叶酸,最终抑制Hcy的代谢(文献引用11-13、15-20);③ DMARDs药物——甲氨蝶呤通过抑制二氢叶酸还原酶,阻断叶酸向四氢叶酸转化,直接导致Hcy升高(文献引用23-28)。
关于HHcy与CVD的关联,队列研究显示:高Hcy水平可预测RA患者致命/非致命动脉血栓事件(OR=1.96,95%CI 0.99-3.50,p=0.05,n=235);日本RA女性中,高Hcy水平与脑白质病变风险增加显著相关(OR=1.35,95%CI 1.12-1.63,p<0.0001)(文献引用10、40)。
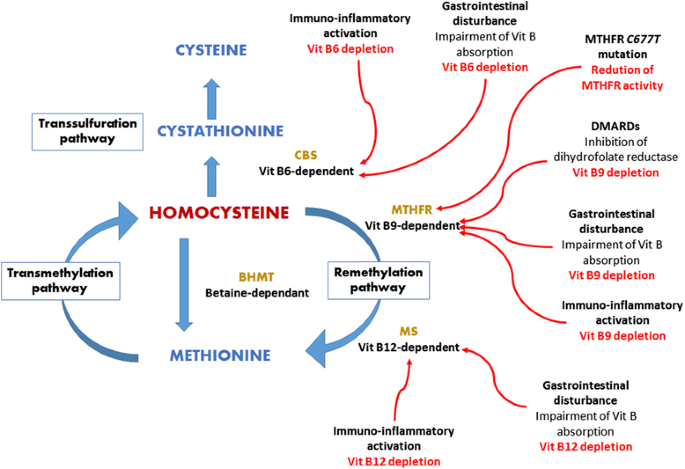
(图1:RA患者中HHcy的发生机制——炎症、遗传及药物共同导致B族维生素消耗,抑制Hcy代谢)
产品关联:文献未提及具体实验产品,领域常规使用同型半胱氨酸检测试剂盒(如循环酶法试剂)、MTHFR基因分型试剂盒等。
3.3 叶酸补充的CVD预防效果分析
实验目的:评估叶酸补充在普通人群及RA患者中降低HHcy、预防CVD的效果。
方法细节:回顾了普通人群中叶酸补充的随机对照试验(RCT)及meta分析(如纳入58804例受试者的26项RCT meta分析),以及RA患者中叶酸补充与HHcy、死亡风险关联的研究(如甲氨蝶呤联合叶酸治疗的RA队列研究)。
结果解读:普通人群的证据显示,叶酸补充可显著降低血浆Hcy水平(平均降低25-30%),并降低7%的首次卒中风险(RR=0.93,95%CI 0.86-1.00,p=0.05),但对冠心病无显著预防效果(文献引用55、58)。RA患者的证据则表明,甲氨蝶呤治疗时补充叶酸(5mg/周)可显著降低HHcy水平(文献引用23、25-28),且甲氨蝶呤联合叶酸的死亡风险(HR=0.2)显著低于单独甲氨蝶呤治疗(HR=0.5),提示叶酸可能通过降低HHcy改善预后(文献引用66)。
然而,RA患者中叶酸补充的CVD预防效果仍缺乏直接证据——目前仅观察到叶酸补充与死亡风险降低相关,但未明确其是否通过降低Hcy减少CVD事件。
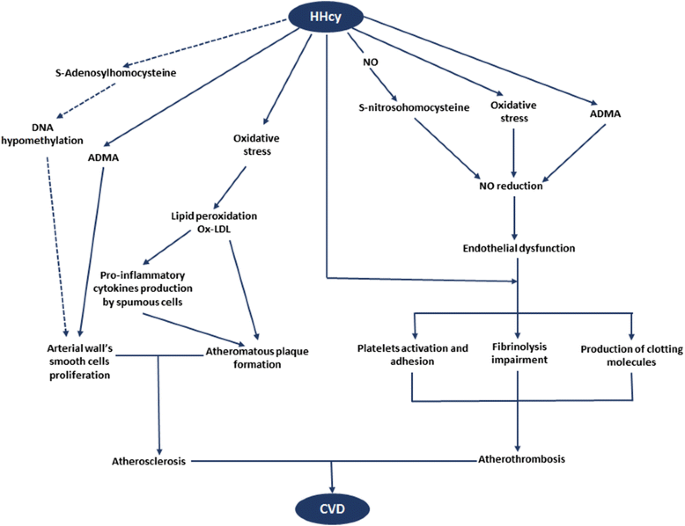
(图2:HHcy导致CVD的机制——氧化应激、ADMA升高及血栓形成共同导致内皮功能障碍及动脉粥样硬化)
产品关联:文献未提及具体实验产品,领域常规使用叶酸补充剂(如5mg/周的叶酸片)、血浆Hcy检测试剂等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的核心生物标志物为循环同型半胱氨酸(Hcy),属于“氨基酸类循环生物标志物”。其筛选逻辑遵循“从人群到疾病”的递进:首先在普通人群中明确HHcy是CVD的风险因子,随后发现RA患者中HHcy发生率显著升高,最后通过队列研究验证HHcy与RA患者CVD的关联。验证逻辑则基于“纵向随访”——通过对RA患者随访6.5年,分析Hcy水平与CVD事件的相关性。
研究过程详述
Hcy的来源为RA患者的血浆样本,验证方法主要为循环酶法或免疫法检测血浆Hcy浓度(领域常规方法)。现有研究中,RA患者HHcy的发生率为20-42%(n=235-435),显著高于普通人群的5-7%(文献引用29、39)。队列研究结果显示:① 对235例RA患者随访6.5年,高Hcy水平可预测致命/非致命动脉血栓事件(OR=1.96,95%CI 0.99-3.50,p=0.05);② 日本RA女性中,高Hcy水平与脑白质病变风险增加显著相关(OR=1.35,95%CI 1.12-1.63,p<0.0001)(文献引用10、40)。
核心成果提炼
Hcy是RA患者CVD的风险预测生物标志物,其水平升高与RA患者CVD事件风险增加显著相关(OR=1.96,p=0.05;OR=1.35,p<0.0001)。其创新性在于:① 首次系统验证了Hcy作为RA患者CVD风险标志物的价值(此前仅少数研究提及);② 提出叶酸补充通过降低Hcy,可能成为RA患者CVD预防的潜在策略(基于普通人群的叶酸补充证据及RA患者的HHcy发生率)。
需注意的是,目前尚无研究明确Hcy与RA患者CVD的因果关系(仅为相关性),且叶酸补充的最佳剂量(如5mg/周 vs 1mg/日)、长期效果(如10年以上的CVD预防)仍需大样本RCT验证。
结论:叶酸补充通过降低Hcy及阻断其心血管损伤作用,在RA患者CVD预防中具有潜在治疗价值,但需大样本长期临床试验明确其疗效及适用人群。对于RA患者中高风险HHcy人群(如MTHFR 677C>T突变、甲氨蝶呤治疗者),建议早期补充叶酸以降低CVD风险。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。