Extracellular vesicle-based liquid biopsy biomarkers and their application in precision immuno-oncology
基于细胞外囊泡的液体活检生物标志物及其在精准免疫肿瘤学中的应用
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2023 | 起止号: | 2023 Nov 17;11(1):99 |
| doi: | 10.1186/s40364-023-00540-2 | 研究方向: | 肿瘤、细胞生物学、免疫/内分泌 |
文献解析
1. 领域背景与文献引入
文献英文标题:Extracellular vesicle-based liquid biopsy biomarkers and their application in precision immuno-oncology;发表期刊:Biomarker Research;影响因子:5.8(2022年);研究领域:肿瘤免疫学、液体活检、细胞外囊泡(EVs)。
肿瘤免疫治疗(如免疫检查点抑制剂,ICI)已成为多种癌症的标准治疗,但原发性/适应性耐药仍是临床挑战——约60%患者对ICI无响应,响应者中约30%会出现获得性耐药。耐药的核心原因是肿瘤微环境(TME)的动态异质性:肿瘤细胞通过与基质细胞、免疫细胞的通讯重塑TME,诱导免疫逃逸。传统组织活检因侵入性、静态性无法实时反映TME变化,而液体活检(如循环肿瘤DNA、循环肿瘤细胞)因微创、实时的优势成为研究热点。其中,细胞外囊泡(EVs)作为细胞间通讯的关键介质,携带 parental细胞的蛋白质、RNA、代谢物等“ cargo ”,能全面反映TME的动态变化,是极具潜力的液体活检生物标志物。
尽管EVs的研究已取得进展,但仍存在分离与分析标准化不足、TME调控机制未完全阐明、临床转化证据分散等问题。本综述系统总结了EVs的生物学特性、分离分析技术、TME中的免疫调控机制,以及作为ICI响应生物标志物的临床证据,为EVs在精准免疫肿瘤学中的应用提供了全景式框架。
2. 文献综述解析
作者以“EVs从基础到临床的转化”为核心逻辑,将现有研究分为四大模块:EVs的生物学特性(亚型、生物发生、 cargo)、分离与分析技术、TME中的免疫调控机制、作为ICI生物标志物的临床研究。
2.1 现有研究的关键结论与局限
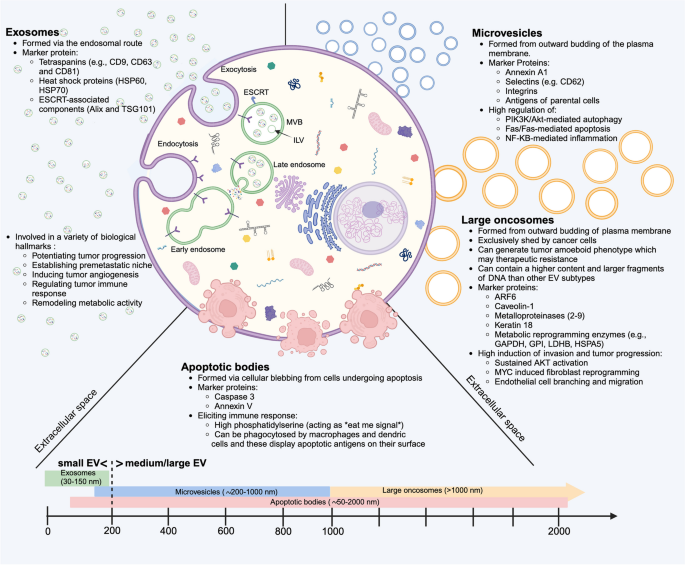
- EVs的生物学特性:EVs包括外泌体(30-150nm,内体途径,标志物CD9/CD63/CD81)、微囊泡(200-1000nm,质膜出芽,标志物Annexin V)、凋亡小体(50-2000nm,凋亡细胞碎片,标志物PS)、大肿瘤小体(>1000nm,癌细胞特有的,标志物TGF-β)。不同亚型的cargo和功能差异显著,如外泌体主要传递miRNAs调控基因表达,大肿瘤小体传递DNA反映肿瘤基因组特征。
- 分离与分析技术:传统方法(超速离心、尺寸排阻色谱)存在纯度低、EVs损伤的问题;新型技术(微流控、磁珠免疫捕获)通过靶向EVs表面标志物(如CD63、EpCAM)提高了分离效率(如微流控芯片捕获效率>90%)。分析技术方面,single EV分析(纳米流式细胞术)解决了EVs异质性问题,多组学整合(蛋白质组+转录组+机器学习)能挖掘高特异性生物标志物签名(如NSCLC中miR-200c-3p+miR-21-5p+miR-28-5p组合预测ICI响应的AUC=0.85)。
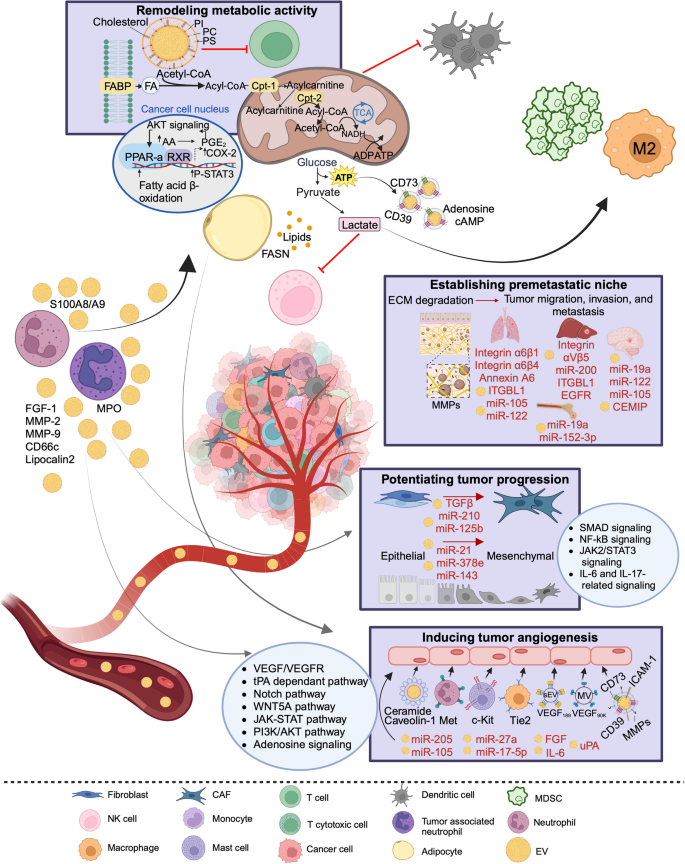
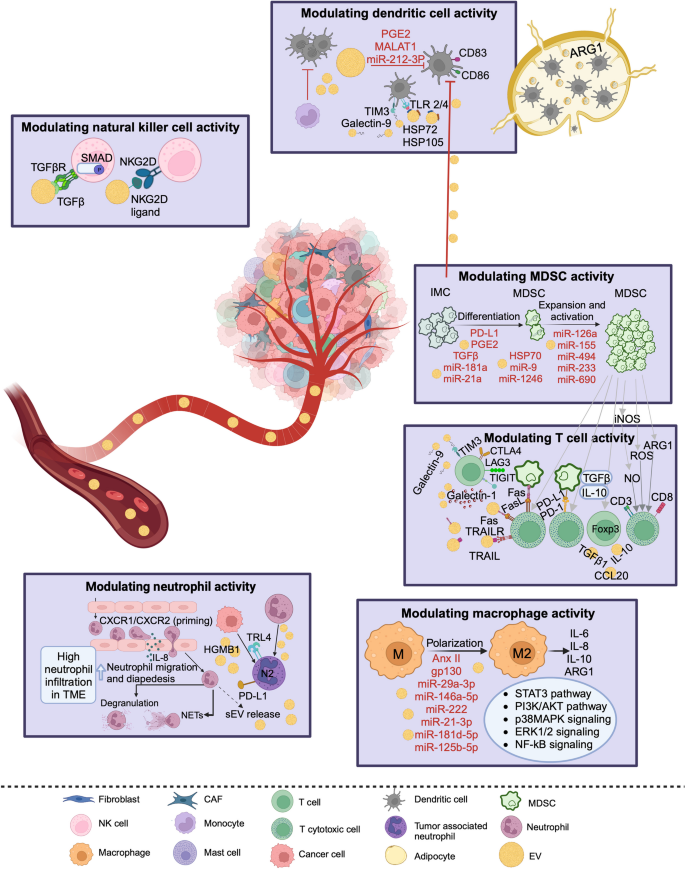
- TME中的免疫调控:EVs通过传递cargo调控免疫细胞功能:① 诱导巨噬细胞M2极化(如肿瘤来源EVs的miR-21激活STAT3通路);② 扩张髓源性抑制细胞(MDSCs,通过PD-L1、TGF-β);③ 抑制T细胞增殖(通过PD-L1直接结合T细胞PD-1);④ 下调NK细胞活性(通过NKG2D配体)。这些机制共同诱导免疫逃逸,促进肿瘤进展。
- 临床研究证据:EVs-PD-L1、miRNAs等生物标志物的动态变化与ICI响应密切相关:NSCLC患者治疗后EVs-PD-L1下降≥50%的客观缓解率(ORR)为60%,而无下降者仅20%;黑色素瘤患者基线EVs-PD-L1>100pg/mL的无进展生存期(PFS)更短(中位数3.5个月vs 12个月)。
现有研究的局限:① EVs分离与分析的标准化不足,不同研究结果可比性差;② single EV分析技术仍在发展,无法解析所有亚型的功能;③ 临床研究样本量小(多为单中心、n<100),缺乏多中心验证。
2.2 本综述的创新价值
本综述的核心创新在于“系统整合基础研究与临床证据”:① 首次从“精准免疫肿瘤学”视角,梳理EVs从生物学特性到临床应用的全链条;② 强调多组学结合机器学习在生物标志物发现中的作用(如通过机器学习整合EVs蛋白质组与转录组数据,筛选出预测ICI响应的miRNAs组合);③ 聚焦EVs的动态变化(如治疗前后EVs-PD-L1的波动),为临床实时监测提供依据。
3. 研究思路总结与详细解析
本综述以“EVs的基础研究→技术进展→机制研究→临床应用”为闭环逻辑,分四部分展开:
3.1 EVs的生物学特性解析
- 实验目的:阐明EVs的亚型、生物发生及cargo功能。
- 方法细节:基于国际细胞外囊泡学会(ISEV)的分类标准,综述了外泌体(内体途径:早期内体→多泡体→外泌体释放)、微囊泡(质膜出芽)、凋亡小体(凋亡细胞碎片)、大肿瘤小体(癌细胞特有的质膜出芽)的生物发生过程,以及各亚型的标志性蛋白质(如外泌体的tetraspanins家族、微囊泡的Annexin V)。
- 结果解读:不同EVs亚型的cargo和功能差异显著:① 外泌体富含miRNAs(如miR-21、miR-146a),主要调控基因表达;② 微囊泡携带蛋白质(如TGF-β),调控细胞信号通路;③ 大肿瘤小体携带DNA(如突变的KRAS),反映肿瘤基因组特征。
- 产品关联:文献提及外泌体分离常用ExoQuick(聚合物沉淀),微流控芯片(如ExoChip)用于高纯度分离。
3.2 EVs分离与分析技术的进展
- 实验目的:比较传统与新型技术的优缺点,推动技术标准化。
- 方法细节:① 分离技术:传统方法(超速离心)产量低(<30%)、易污染;新型方法(微流控、磁珠免疫捕获)通过靶向EVs表面标志物提高纯度(如磁珠捕获CD63+外泌体的纯度>95%)。② 分析技术:single EV分析(纳米流式细胞术,NanoFCM)能解析EVs的异质性(如不同亚型的蛋白质表达差异);多组学整合(蛋白质组+转录组)结合机器学习(如随机森林算法)能挖掘生物标志物签名。
- 结果解读:新型技术解决了传统方法的局限,如微流控芯片的分离时间从24小时缩短至1小时,且EVs完整性保留率>90%;single EV分析发现,NSCLC患者的外泌体中CD63+CD9+亚型占比(35%)显著高于健康人(15%),该亚型与ICI耐药相关。
- 产品关联:提到的分析技术包括NanoFCM(纳米流式细胞术)、Olink proximity extension assay(PEA,多蛋白检测)。
3.3 EVs在TME中的免疫调控机制
- 实验目的:阐明EVs如何介导TME中的细胞间通讯,诱导免疫逃逸。
- 方法细节:综述了EVs对不同免疫细胞的调控:① 巨噬细胞:肿瘤来源EVs的miR-21激活STAT3通路,诱导M2极化,分泌IL-10抑制T细胞;② MDSCs:EVs-PD-L1结合MDSCs的PD-1,诱导其扩张并分泌ARG1消耗L-精氨酸,抑制T细胞增殖;③ T细胞:EVs-PD-L1直接结合T细胞的PD-1,抑制其分泌IFN-γ和颗粒酶B;④ NK细胞:EVs携带的NKG2D配体下调NK细胞的NKG2D受体,降低细胞毒性。
- 结果解读:EVs通过“多免疫细胞调控网络”重塑TME:M2巨噬细胞与MDSCs协同抑制T细胞,NK细胞活性下降进一步削弱抗肿瘤免疫,最终诱导ICI耐药。例如,黑色素瘤患者的EVs-miR-125b能诱导Treg分化,Treg占比>10%的患者对ICI无响应。
- 产品关联:实验模型包括小鼠黑色素瘤B16异种移植模型(验证EVs对巨噬细胞的调控)、人外周血T细胞与癌细胞共培养模型(验证EVs-PD-L1对T细胞的抑制)。
3.4 EVs作为ICI生物标志物的临床研究
- 实验目的:总结EVs生物标志物与ICI响应的临床相关性。
- 方法细节:重点分析了NSCLC和黑色素瘤的临床研究:① NSCLC:治疗前EVs-miR-200c-3p/miR-21-5p高表达与耐药相关(ORR=15%),治疗后EVs-PD-L1下降≥50%的患者ORR=60%;② 黑色素瘤:基线EVs-PD-L1>100pg/mL的患者PFS更短(中位数3.5个月vs 12个月),治疗后EVs-PD-L1升高与响应相关(可能与T细胞再激活有关);③ EVs-CD73:黑色素瘤患者中,EVs-CD73高表达与ICI耐药相关(通过产生腺苷抑制T细胞)。
- 结果解读:EVs生物标志物的动态变化比静态指标(如组织PD-L1 IHC)更能反映TME的免疫状态。例如,NSCLC患者中,EVs-miRNAs组合(miR-200c-3p+miR-21-5p+miR-28-5p)预测ICI响应的AUC=0.85,显著高于组织PD-L1 IHC的AUC=0.72。
- 产品关联:临床检测常用ELISA(EVs-PD-L1)、qPCR(EVs-miRNAs)、流式细胞术(EVs-CD73)。
4. Biomarker研究及发现成果解析
4.1 Biomarker定位与筛选逻辑
本综述涉及的Biomarker主要为EVs携带的蛋白质、RNA,包括:
- 蛋白质:PD-L1(免疫检查点分子)、CD73(腺苷代谢酶);
- RNA:miR-200c-3p、miR-21-5p、miR-28-5p(调控免疫细胞功能的miRNAs)、PD-L1 mRNA。
筛选/验证逻辑:① 从临床样本(血浆/血清)中分离EVs;② 通过组学技术(蛋白质组学、转录组学)筛选差异表达的cargo;③ 功能实验验证其调控免疫细胞的机制(如EVs-PD-L1抑制T细胞增殖);④ 临床队列验证与ICI响应的相关性(如NSCLC患者的队列研究,n=100)。
4.2 研究过程与核心成果
- EVs-PD-L1:① 来源:血浆EVs;② 验证方法:ELISA定量检测;③ 临床数据:NSCLC患者治疗后EVs-PD-L1下降≥50%的ORR=60%(n=80,P<0.01),黑色素瘤患者基线EVs-PD-L1>100pg/mL的PFS中位数=3.5个月(n=60,P<0.05);④ 功能关联:EVs-PD-L1直接结合T细胞的PD-1,抑制其功能,是ICI耐药的关键介质。
- EVs-miRNAs组合:① 来源:血浆EVs;② 验证方法:qPCR检测;③ 临床数据:miR-200c-3p+miR-21-5p+miR-28-5p组合预测NSCLC患者ICI响应的AUC=0.85(95% CI 0.78-0.92),敏感性82%,特异性80%(n=100);④ 功能关联:这些miRNAs通过调控STAT3、JAK2通路,诱导巨噬细胞M2极化和MDSCs扩张。
- EVs-CD73:① 来源:血清EVs;② 验证方法:流式细胞术;③ 临床数据:黑色素瘤患者中,EVs-CD73高表达与ICI耐药相关(ORR=10% vs 50%,n=50,P<0.05);④ 功能关联:CD73催化AMP生成腺苷,抑制T细胞增殖。
4.3 创新性与临床价值
本综述的Biomarker研究突破了传统静态标志物的局限,强调动态变化的临床价值(如治疗前后EVs-PD-L1的波动),为临床实时监测ICI响应提供了依据。其中,EVs-miRNAs组合的预测准确性(AUC=0.85)显著高于组织PD-L1 IHC(AUC=0.72),有望成为临床实用的生物标志物。
总结
本综述系统总结了EVs在精准免疫肿瘤学中的应用,从基础研究(生物学特性、TME机制)到技术进展(分离分析),再到临床证据(ICI响应生物标志物),为EVs的临床转化提供了清晰框架。未来需要解决技术标准化、大样本多中心验证等问题,推动EVs成为精准免疫肿瘤学的“新一代液体活检生物标志物”。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。