A putative N-terminal nuclear export sequence is sufficient for Mps1 nuclear exclusion during interphase
假定的N端核输出序列足以使Mps1在间期被排除在细胞核外。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2015 | 起止号: | 2015 Feb 27;16:6 |
| doi: | 10.1186/s12860-015-0048-6 | 研究方向: | 细胞生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:A putative N-terminal nuclear export sequence is sufficient for Mps1 nuclear exclusion during interphase;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞周期调控(Mps1激酶核质转运机制)
Mps1(单极纺锤体1,人类中又称TTK)是一类关键的丝氨酸/苏氨酸激酶,在细胞周期调控网络中发挥多重核心功能。领域共识:在有丝分裂阶段,Mps1是纺锤体组装检查点(SAC)激活和染色体精准排列的必需分子,通过介导有丝分裂检查点复合物的组装调控细胞周期进程,同时还参与中心体复制的调控;在间期阶段,Mps1通过与p53、Chk2等分子互作,参与DNA损伤应答通路的激活。目前领域内已明确Mps1在间期主要定位于细胞质,在G2/M期会发生核质转运进入细胞核,但间期Mps1滞留在细胞质的具体调控机制尚未阐明,尤其是介导其核输出的分子基序和转运通路仍属研究空白。针对这一核心问题,本研究旨在鉴定Mps1上的功能性核输出序列,明确其核输出的调控机制,为细胞周期中Mps1的功能调控提供新的分子依据,具有重要的学术必要性。
2. 文献综述解析
作者对领域内现有研究的分类维度为Mps1的功能阶段(有丝分裂、间期)及亚细胞定位调控方向。现有研究已明确Mps1在有丝分裂中通过激活SAC通路抑制APC/C介导的蛋白水解,磷酸化Borealin参与染色体排列,还通过作用于Mortalin、Centrin 2等底物调控中心体复制;在间期则通过与p53、Chk2的相互作用参与DNA损伤应答的调控。技术方法上,已有研究通过免疫荧光、免疫共沉淀、蛋白激酶活性分析等技术,系统解析了Mps1的功能靶点和亚细胞定位动态变化,但现有研究的局限性在于未揭示间期Mps1滞留在细胞质的具体分子机制,尤其是介导其核输出的关键序列和转运分子尚未被鉴定。本研究通过对比现有研究的未解决问题,首次聚焦Mps1的核输出调控机制,鉴定出其N端的功能性推定核输出序列(pNES1),并明确该序列依赖Crm1介导Mps1的间期核输出,填补了Mps1核质转运调控机制的研究空白,为细胞周期调控的分子网络提供了新的节点。
3. 研究思路总结与详细解析
本研究的整体框架为:以“Mps1间期核输出的调控机制”为核心科学问题,首先验证Crm1对Mps1核输出的介导作用,然后通过生物信息学预测结合功能实验鉴定Mps1上的核输出序列,最后通过突变实验明确该序列的功能及关键位点,形成“假设-实验验证-机制解析”的完整研究闭环,研究目标是揭示Mps1间期核排除的分子基序及调控通路。
3.1 Crm1介导Mps1间期核输出的验证
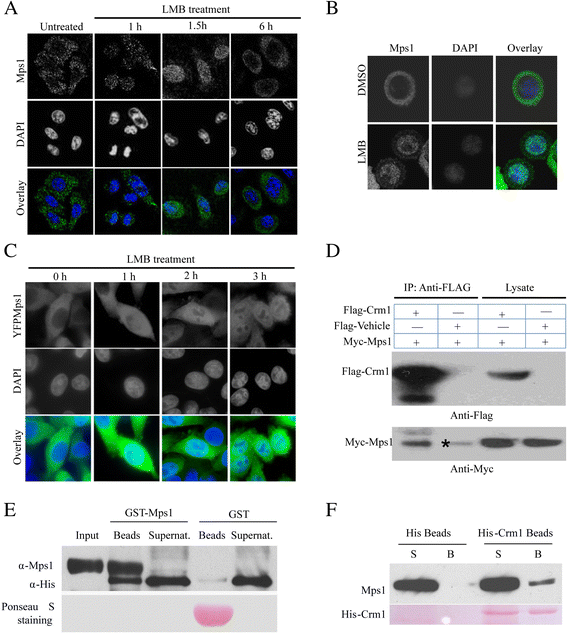
实验目的是明确Mps1的间期核输出是否依赖Crm1介导的转运通路。方法细节:采用结肠癌细胞系SW480,通过100 ng/ml诺考达唑处理使细胞停滞在前中期,释放后在不同时间点固定细胞进行免疫荧光染色,观察Mps1的亚细胞定位变化;同时用10 μM Crm1抑制剂雷帕霉素B(LMB)处理同步化及非同步化细胞,通过免疫荧光观察Mps1的定位变化;在293T细胞中进行免疫共沉淀实验,验证内源性及外源性Mps1与Crm1的相互作用;进一步通过体外蛋白pull-down实验,使用纯化的GST标签Mps1和His标签Crm1蛋白,验证两者的直接物理相互作用。结果解读:免疫荧光结果显示,有丝分裂完成后Mps1随核膜重建逐渐从细胞核排除到细胞质(图1A);LMB处理后,内源性及YFP融合的Mps1均在细胞核内积累(图1B、C),说明Mps1的核输出依赖Crm1;免疫共沉淀及pull-down实验证实Crm1与Mps1存在直接的物理相互作用(图1D-F),为Crm1介导Mps1核输出提供了直接证据。实验所用关键产品:文献未提及具体实验产品,领域常规使用免疫组化(IHC)抗体、免疫共沉淀试剂盒、蛋白纯化试剂等。
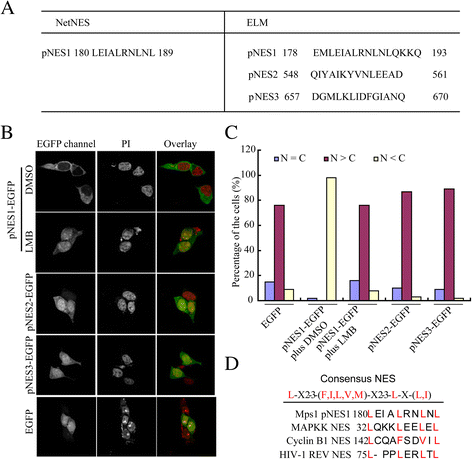
3.2 Mps1推定核输出序列(pNES1)的预测与功能验证
实验目的是鉴定Mps1上介导核输出的功能性序列。方法细节:通过NetNES和ELM在线生物信息学软件分析Mps1的氨基酸序列,预测潜在的核输出序列;将预测的推定核输出序列(pNES1)与增强型绿色荧光蛋白(EGFP)融合,构建重组表达载体并转染293T细胞,48小时后观察融合蛋白的亚细胞定位;同时用LMB处理转染细胞,验证融合蛋白的核输出是否依赖Crm1;进一步将pNES1与经典核输出序列(Cyclin B1、HIV Rev等)进行氨基酸序列比对,分析其同源性。结果解读:软件预测显示Mps1的N端仅存在1个符合经典核输出序列特征的pNES1(图2A);pNES1-EGFP融合蛋白主要定位于细胞质,LMB处理后融合蛋白显著进入细胞核(图2B、C),说明该序列具有核输出功能;序列比对显示pNES1与经典NES序列具有高度的疏水氨基酸同源性(图2D),符合Crm1识别的核输出序列特征。实验所用关键产品:文献未提及具体实验产品,领域常规使用基因克隆载体、荧光蛋白标签系统、定点突变试剂盒等。
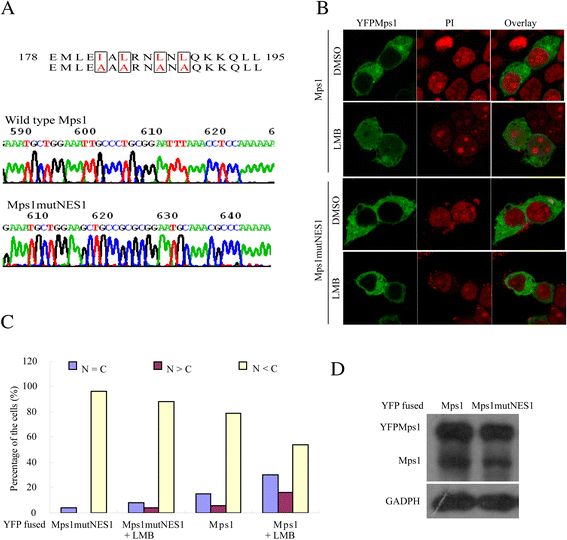
3.3 pNES1突变对Mps1亚细胞定位的影响
实验目的是明确pNES1的完整性对Mps1核质转运的具体作用。方法细节:通过定点突变技术,将pNES1中的1个异亮氨酸和3个亮氨酸突变为丙氨酸,构建Mps1突变体(Mps1mutNES1),并与YFP融合表达;将野生型YFP-Mps1及突变体转染293T和SW480细胞,通过免疫荧光观察其亚细胞定位;同时用LMB处理细胞,分析突变体的核输入能力;进一步构建单个亮氨酸突变的Mps1突变体,分析pNES1中不同氨基酸位点的功能差异。结果解读:Mps1mutNES1仍主要定位于细胞质,即使在LMB处理后也未出现明显的核积累(图3A-C),推测该突变同时影响了Mps1的核输入与核输出过程;单个亮氨酸突变实验显示,前两个疏水氨基酸(异亮氨酸、亮氨酸)突变体仍主要定位于细胞质,而后两个亮氨酸突变体则出现明显的核定位(图4D),说明pNES1的完整性对Mps1的核输出至关重要,且不同位点的疏水氨基酸发挥的功能存在差异。实验所用关键产品:文献未提及具体实验产品,领域常规使用细胞转染试剂、免疫荧光抗体、蛋白电泳试剂等。
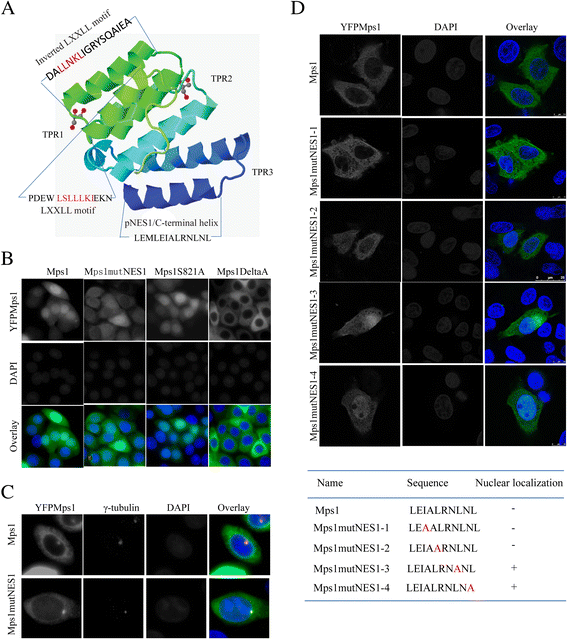
3.4 pNES1突变对G2/M期Mps1核转运的影响
实验目的是明确pNES1是否影响Mps1在G2/M期的核输入过程。方法细节:用2 mM胸腺嘧啶及CDK1抑制剂RO-3306依次处理SW480细胞,使其同步化停滞在G2期;通过免疫荧光观察野生型YFP-Mps1、Mps1mutNES1及其他对照突变体的核定位情况;同时观察突变体的中心体定位,分析突变是否影响Mps1的蛋白折叠。结果解读:G2期时,Mps1mutNES1的核定位能力显著受损,而缺失LXXLL核输入基序的突变体(Mps1deltaA)同样无法进入细胞核,作为对照的Mps1S821A突变体则正常进入细胞核(图4B);但Mps1mutNES1的中心体定位与野生型Mps1一致(图4C),说明pNES1突变未影响Mps1的整体蛋白折叠,而是通过影响相邻的TPR结构域的蛋白互作能力,间接影响了Mps1的G2/M期核输入。实验所用关键产品:文献未提及具体实验产品,领域常规使用细胞同步化试剂、免疫组化(IHC)抗体、荧光显微镜成像系统等。
4. Biomarker研究及发现成果
Biomarker定位
本研究鉴定的功能性Biomarker为Mps1的N端推定核输出序列(pNES1),属于蛋白功能调控基序。筛选与验证逻辑为:首先通过NetNES和ELM在线软件预测Mps1的潜在核输出序列,然后通过荧光融合蛋白实验验证其核输出功能,再通过LMB处理验证其Crm1依赖性,最后通过定点突变实验明确关键氨基酸位点的功能,形成完整的筛选-验证闭环。
研究过程详述
pNES1来源于Mps1的N端氨基酸序列,通过将其与EGFP融合构建重组载体,转染293T细胞后观察到融合蛋白主要定位于细胞质,LMB处理后融合蛋白进入细胞核,证实其具有核输出功能;通过定点突变实验,将pNES1中的疏水氨基酸突变为丙氨酸,发现单个亮氨酸位点的突变即可导致Mps1的核定位变化,其中后两个亮氨酸位点是核输出的关键功能位点。文献未提供定量的特异性与敏感性数据,基于图表趋势推测,pNES1-EGFP融合蛋白在细胞质的定位比例显著高于EGFP对照组,突变后核定位比例发生显著变化。
核心成果提炼
本研究的核心成果为:明确pNES1是Mps1间期核输出的功能性序列,依赖Crm1介导的转运通路;pNES1的完整性不仅影响Mps1的核输出,还通过影响相邻TPR结构域的蛋白互作,间接调控Mps1在G2/M期的核输入;该序列是首次被鉴定的Mps1核输出调控基序,为细胞周期中Mps1的亚细胞定位调控提供了分子机制,也为Crm1介导的核质转运通路增添了新的底物分子。文献未明确提供样本量及统计学显著性的具体数值,基于图表趋势推测实验结果具有统计学意义。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。