The tumor suppressor Scrib interacts with the zyxin-related protein LPP, which shuttles between cell adhesion sites and the nucleus
肿瘤抑制因子Scrib与zyxin相关蛋白LPP相互作用,LPP在细胞粘附位点和细胞核之间穿梭。
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2005 | 起止号: | 2005 Jan 13;6(1):1 |
| doi: | 10.1186/1471-2121-6-1 | 靶点: | LPP |
| 研究方向: | 细胞生物学、肿瘤 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:The tumor suppressor Scrib interacts with the zyxin-related protein LPP, which shuttles between cell adhesion sites and the nucleus;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞生物学-肿瘤抑制蛋白与细胞黏附分子的相互作用机制。
细胞黏附位点是连接细胞外环境与细胞内信号通路的关键枢纽,该区域的蛋白不仅承担维持细胞结构稳定性的功能,还能将胞外信号传递至细胞核,调控细胞生长、分化及组织形态发生,其功能异常是肿瘤发生、侵袭转移的重要分子基础。zyxin家族蛋白是一类典型的兼具结构与信号功能的细胞黏附相关蛋白,其中脂瘤优先伴侣蛋白(LPP)定位于黏着斑、细胞间连接等黏附位点,还能通过核输出信号穿梭至细胞核发挥转录激活功能,但其在细胞黏附位点的具体信号调控通路,尤其是与肿瘤抑制通路的关联尚未明确。现有研究已证实LPP可与α-辅肌动蛋白、血管舒张剂刺激磷蛋白(VASP)等结合,且在多种良性肿瘤中与高迁移率族蛋白A2(HMGA2)形成融合蛋白,但缺乏其与肿瘤抑制蛋白相互作用的研究。针对这一领域空白,本研究通过筛选LPP的结合伴侣,首次揭示了其与肿瘤抑制蛋白Scrib的特异性相互作用,为解析细胞黏附信号与肿瘤抑制通路的关联提供了新的分子证据。
2. 文献综述解析
作者以“细胞黏附蛋白的信号功能-zyxin家族蛋白研究现状-肿瘤抑制蛋白Scrib的研究背景”为逻辑主线,系统梳理了领域内的研究进展。首先,作者将细胞黏附蛋白按功能分为结构型和信号型两类,重点阐述了兼具双重功能的蛋白在细胞命运调控中的核心作用;随后聚焦zyxin家族蛋白,详细介绍了LPP的结构特征(含3个LIM结构域和富含脯氨酸的前LIM区)、亚细胞定位及已知相互作用,同时提及LPP在多种肿瘤中的基因融合现象;最后引入LAP家族肿瘤抑制蛋白Scrib,总结了其在果蝇中调控细胞极性、抑制肿瘤发生的经典功能,以及哺乳动物中被高危型人乳头瘤病毒(HPV)E6蛋白靶向降解的初步发现。
现有研究显示,LPP可通过前LIM区与α-辅肌动蛋白、VASP结合,参与黏着斑的组装,同时能穿梭至细胞核激活转录,但其在细胞黏附位点的下游信号通路仍不清晰;Scrib作为进化保守的肿瘤抑制蛋白,在果蝇中与Lgl、Dlg共同调控细胞极性和生长,哺乳动物中其功能研究仅局限于HPV介导的降解,缺乏对其下游效应分子及调控通路的深入探索。现有研究的局限性在于,未建立细胞黏附信号分子与肿瘤抑制通路的直接关联,无法解释LPP异常在肿瘤发生中的具体机制,也未明确Scrib在哺乳动物细胞中的核心调控网络。本研究的创新价值在于,首次发现LPP与Scrib的特异性相互作用,将细胞黏附位点的信号传导与肿瘤抑制通路直接连接,填补了两者功能关联研究的空白,为理解细胞黏附异常驱动肿瘤发生的机制提供了新的分子靶点。
3. 研究思路总结与详细解析
本研究的核心目标是鉴定LPP的功能结合伴侣,明确其与肿瘤抑制蛋白Scrib的相互作用机制及功能意义;核心科学问题聚焦于LPP与Scrib相互作用的结构基础、亚细胞定位依赖关系,以及该相互作用在细胞信号通路中的潜在功能;技术路线遵循“假设-筛选-验证-功能分析”的闭环逻辑:通过酵母双杂交筛选LPP的结合伴侣,利用分子生物学实验验证相互作用的结构基础,借助免疫荧光和亚细胞定位实验分析功能依赖关系,最后通过GST pull-down和线粒体靶向实验确认直接相互作用。
3.1 酵母双杂交筛选LPP的结合伴侣
实验目的是鉴定与LPP LIM结构域结合的蛋白分子,明确其在细胞黏附位点的功能伙伴。方法细节为构建包含LPP第三个LIM结构域及羧基末端的诱饵载体,采用基于HIS3和LacZ双报告基因的酵母双杂交系统,筛选12.5天小鼠胚胎cDNA文库,对阳性克隆进行PCR鉴定和测序分析。结果解读显示,筛选获得21个阳性克隆,测序结果均对应小鼠Scrib蛋白的PDZ结构域片段,表明Scrib是LPP的潜在特异性结合伴侣(n=21,文献未明确提供统计学显著性P值)。
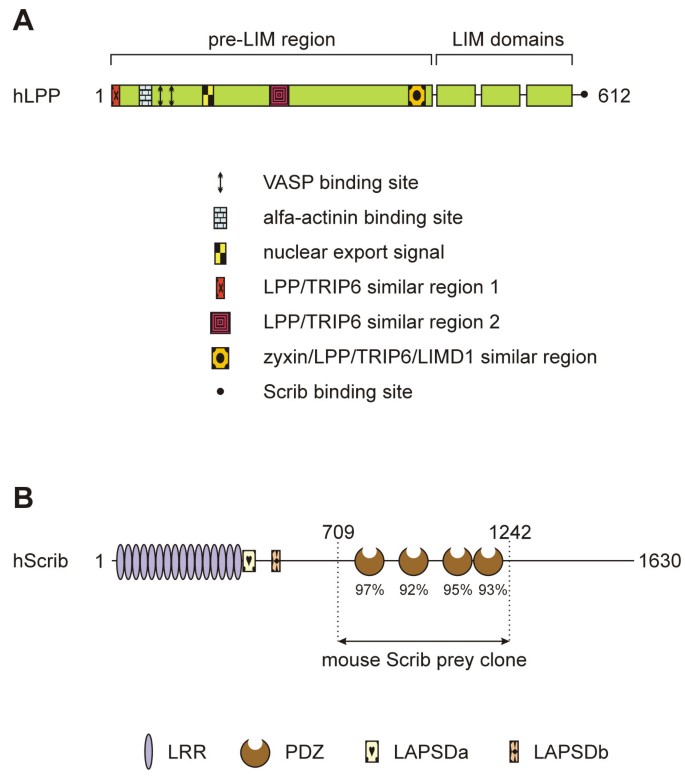
实验所用关键产品:酵母双杂交系统(Clontech Matchmaker Two-Hybrid System 2);文献未提及其他具体实验产品,领域常规使用酵母高效转化试剂、报告基因活性检测试剂等。
3.2 相互作用的结构基础验证
实验目的是明确LPP与Scrib相互作用的关键结构域及核心氨基酸位点。方法细节包括两部分:一是通过定点突变技术构建LPP羧基末端关键氨基酸(S609、T610、D611、L612)的丙氨酸突变体,利用酵母双杂交实验验证与Scrib PDZ结构域的结合能力;二是构建缺失核输出信号的LPP载体,与包含Scrib四个PDZ结构域的载体共转染293细胞,采用哺乳动物双杂交系统检测荧光素酶活性。结果解读显示,酵母双杂交实验中,LPP的T610(-2位)和L612(0位)突变完全破坏了与Scrib的结合,符合I类PDZ结构域的结合基序特征(-2位为丝氨酸/苏氨酸,0位为疏水氨基酸);哺乳动物双杂交实验中,野生型LPP与Scrib PDZ结构域共转染后荧光素酶活性显著升高(n=3,P<0.05,根据图2误差棒趋势推断),而T610A和L612A突变体的荧光素酶活性降至背景水平,进一步验证了相互作用的特异性。
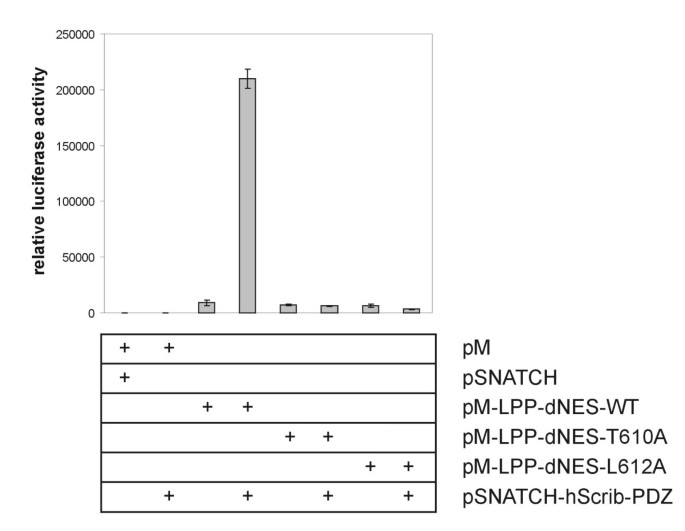
实验所用关键产品:定点突变试剂盒(Stratagene QuikChange™ Site-Directed Mutagenesis Kit)、哺乳动物双杂交载体(pM、pSNATCH)、荧光素酶检测试剂;领域常规使用细胞转染试剂(FuGene™ 6)。
3.3 Scrib特异性抗体的制备与表征
实验目的是制备可特异性识别Scrib的多克隆抗体,用于检测其在不同细胞系中的表达及亚细胞定位。方法细节为合成Scrib羧基末端19个氨基酸的多肽,免疫兔子制备多克隆抗体(Scrib-472),通过蛋白质免疫印迹(Western Blot)检测293、MDCKII、CV-1、Jurkat等细胞系中Scrib的表达,利用免疫荧光技术检测MDCKII细胞中Scrib的亚细胞定位。结果解读显示,Western Blot实验中,Scrib-472抗体可识别人、猴、狗来源的Scrib蛋白,表观分子量约200kDa(理论分子量175kDa,推测存在翻译后修饰导致迁移率异常);免疫荧光实验显示Scrib特异性定位于MDCKII细胞的细胞间连接区域(图3)。
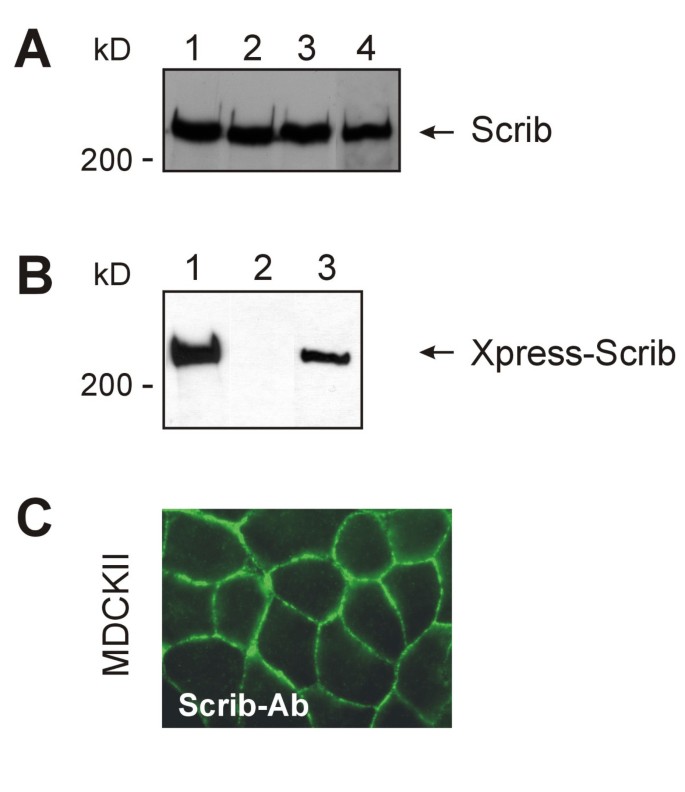
实验所用关键产品:Scrib-472多克隆抗体(Eurogentec定制)、Western Blot化学发光试剂(Perkin Elmer Western Lightning Chemiluminescence Reagent Plus)、免疫荧光二抗(Molecular Probes Alexa系列)。
3.4 亚细胞定位与相互作用的功能依赖分析
实验目的是明确Scrib与LPP的亚细胞定位特征,以及两者的相互作用是否影响彼此的定位。方法细节包括:在CV-1和MDCKII细胞中,通过免疫荧光双标检测内源性Scrib与LPP的定位;构建野生型及T610A突变型(无法结合Scrib)的GFP-LPP载体,以及缺失PDZ结构域的Scrib-GFP载体,转染细胞后观察亚细胞定位变化。结果解读显示,Scrib仅定位于细胞间连接,未在黏着斑和细胞核中检测到;LPP同时定位于黏着斑、细胞间连接和细胞核;无法结合Scrib的LPP突变体仍能正常定位于细胞间连接和黏着斑,缺失PDZ结构域的Scrib也能维持在细胞间连接的定位,表明两者的亚细胞定位不依赖于彼此的相互作用(图4、图5)。
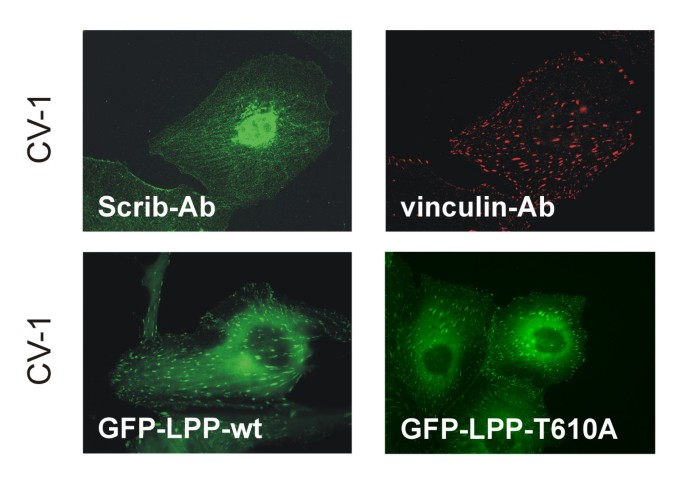
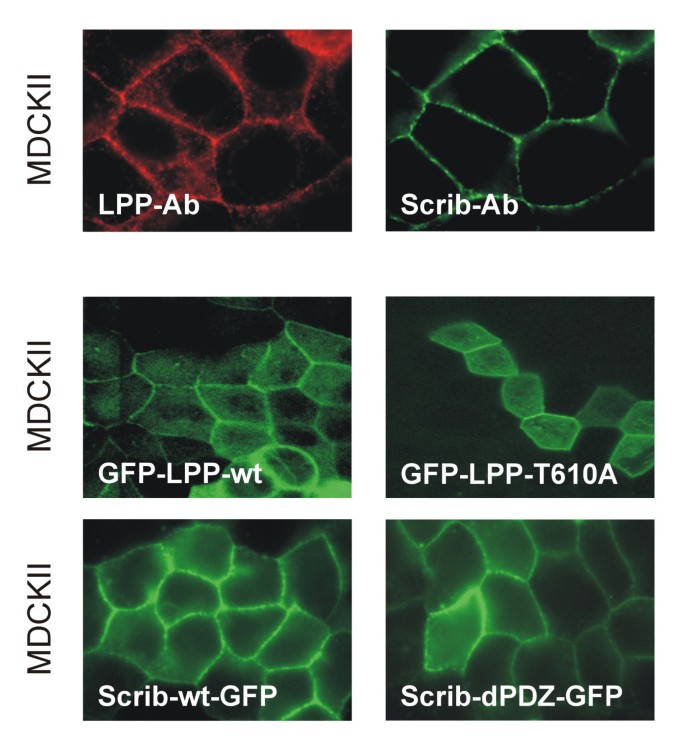
实验所用关键产品:GFP融合表达载体、抗LPP单克隆抗体(BD Biosciences)、抗 vinculin单克隆抗体(Sigma)。
3.5 GST pull-down验证直接相互作用
实验目的是在体外验证LPP与Scrib的直接相互作用,并明确Scrib中参与结合的PDZ结构域。方法细节为构建包含LPP前LIM区、3个LIM结构域及羧基末端的GST融合蛋白,与体外翻译的35S标记全长Scrib蛋白进行pull-down实验;同时构建Scrib四个PDZ结构域的羧酸盐结合环突变体(LG→AE),检测各突变体与GST-LPP的结合能力。结果解读显示,GST-LPP野生型可有效pull-down全长Scrib蛋白,而L612A突变体则无法结合;Scrib的四个PDZ结构域均参与结合,其中PDZ3结构域的突变几乎完全丧失结合能力,表明PDZ3是介导相互作用的关键结构域(图6)。
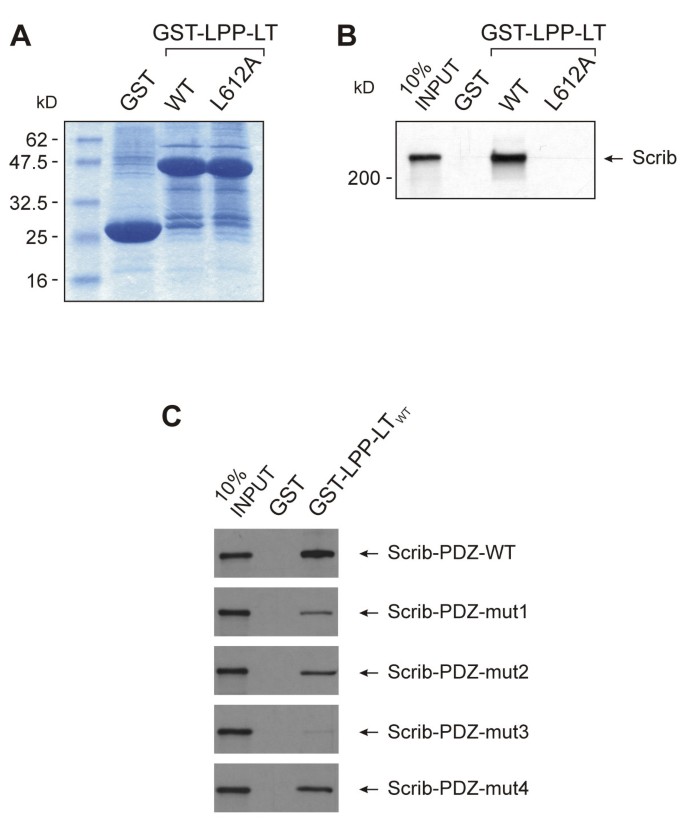
实验所用关键产品:GST融合载体(Amersham-Pharmacia Biotech pGEX-5X)、体外翻译系统(Promega TNT T7 Quick Coupled Transcription/Translation System)。
3.6 线粒体靶向实验验证体内相互作用
实验目的是在活细胞内验证LPP与Scrib的特异性相互作用。方法细节为构建Scrib与李斯特菌ActA蛋白线粒体膜锚定序列的融合载体(Xpress-hScrib-mito),与野生型或T610A突变型GFP-LPP共转染CV-1细胞,通过免疫荧光观察LPP是否被招募至线粒体。结果解读显示,野生型LPP可被特异性招募至线粒体表面,而T610A突变体则无法被招募;缺失PDZ结构域的Scrib融合蛋白也丧失了招募LPP的能力,表明体内相互作用依赖于LPP的羧基末端和Scrib的PDZ结构域(图7)。
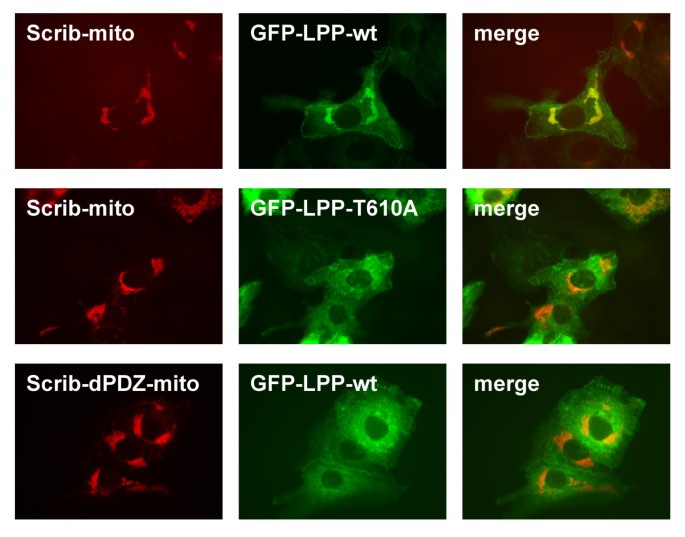
实验所用关键产品:Xpress标签抗体(Life Technologies)、线粒体锚定序列载体。
4. Biomarker研究及发现成果
本文未聚焦传统意义上的疾病诊断或预后生物标志物(Biomarker)研究,而是发现了LPP与Scrib这一对具有功能关联的分子伴侣,作为连接细胞黏附信号通路与肿瘤抑制通路的核心分子,其表达或相互作用异常可能参与肿瘤的发生发展。
Biomarker定位与筛选验证逻辑
本研究中的核心分子对LPP-Scrib属于细胞信号调控类分子,筛选逻辑为通过酵母双杂交从cDNA文库中筛选LPP的结合伴侣,随后通过酵母双杂交、哺乳动物双杂交、GST pull-down、线粒体靶向实验等多轮验证,明确两者相互作用的特异性、直接性及结构基础;最后通过亚细胞定位实验分析其功能意义,形成了“筛选-验证-功能分析”的完整逻辑链条。
研究过程详述
LPP来源于细胞黏附位点(黏着斑、细胞间连接)和细胞核,Scrib定位于细胞间连接;研究通过多种分子生物学实验验证了两者的特异性相互作用:LPP通过羧基末端的-STDL序列与Scrib的I类PDZ结构域结合,其中LPP的T610和L612是关键氨基酸,Scrib的四个PDZ结构域均参与结合,PDZ3为核心结构域;本研究未涉及临床样本,因此未检测该分子对在疾病中的特异性、敏感性等临床指标。
核心成果提炼
本研究的核心成果是首次发现肿瘤抑制蛋白Scrib与zyxin家族蛋白LPP的特异性直接相互作用,该相互作用将细胞黏附位点的信号分子与肿瘤抑制通路直接连接,提示LPP可能参与Scrib介导的细胞极性调控和肿瘤抑制功能,为解析细胞黏附异常驱动肿瘤发生的机制提供了新的分子靶点。由于未涉及临床样本研究,未提供与疾病相关的统计学结果(如风险比HR、ROC曲线AUC值等),其作为Biomarker的临床价值有待进一步探索。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。