Integrating pathology, chromosomal instability and mutations for risk stratification in early-stage endometrioid endometrial carcinoma
整合病理学、染色体不稳定性及突变信息,对早期子宫内膜样癌进行风险分层
| 期刊: | Cell and Bioscience | 影响因子: | |
| 时间: | 2020 | 起止号: | 2020;10:122 |
| doi: | 10.1186/s13578-020-00486-0 | 研究方向: | 肿瘤 |
文献解析
1. 领域背景与文献引入
文献英文标题:Integrating pathology, chromosomal instability and mutations for risk stratification in early-stage endometrioid endometrial carcinoma;发表期刊:Cell Bioscience;影响因子:5.681(2020年);研究领域:妇科肿瘤学-子宫内膜癌风险分层
子宫内膜癌是全球女性第六大常见恶性肿瘤,风险分层是精准预后评估与治疗方案优化的核心前提。当前临床应用的风险分层系统主要分为两类:一是指南推荐的病理分层,依赖组织学类型、肿瘤分级、肌层浸润深度等指标,但存在病理学家诊断共识不足导致的重复性差问题,且同一临床病理特征患者的预后异质性被严重忽略,同时多数病理预后因素需术后获取,对术前手术决策指导价值有限;二是The Cancer Genome Atlas(TCGA)提出的分子分层,将子宫内膜癌分为POLE突变型、微卫星不稳定型(MSI)、低拷贝数变异型(CNV-L)和高拷贝数变异型(CNV-H),还纳入CTNNB1突变等独立预后因素,虽弥补了病理分层的部分缺陷,但仅对“中高危”患者有预后细化价值,在低危或高危患者中效果有限,且多平台分子检测成本高、流程复杂,还存在“多重分类”无法精准分层的难题,同时无法直接指导术后辅助放疗方案选择。
染色体不稳定性(CIN)作为染色体分离错误导致的染色体数目与结构异常,是病理和分子预后因素演化的内在生物学机制,可能成为整合两种分层系统的关键桥梁。本研究即围绕这一核心假设展开,旨在明确CIN与子宫内膜癌病理、分子预后因素的关联,构建更优的早期子宫内膜样子宫内膜癌风险分层模型,解决现有分层系统的局限性。
2. 文献综述解析
本文综述部分围绕子宫内膜癌现有风险分层系统的核心缺陷展开,提出以CIN为桥梁整合病理与分子分层的创新研究思路。
作者首先按病理与分子两个维度对现有风险分层系统进行分类评述:病理分层系统的核心优势在于基于临床广泛应用的病理指标,可直接对接现有治疗指南,但局限性显著,包括病理诊断的主观性导致的重复性差,无法覆盖肿瘤内在异质性,以及对手术决策的指导不足;分子分层系统的优势在于检测结果客观精准,能有效区分不同预后的患者群体,但存在适用人群受限、无法直接指导放疗方案选择、检测成本高昂及多重分类难题。
作者进一步指出,现有分层系统的核心缺陷在于未能整合病理与分子层面的预后信息,而CIN作为病理和分子预后因素的共同生物学基础,可能解决这一关键问题。原文研究显示,CIN与病理中的不良预后因素(如高分级、晚期、深肌层浸润)及分子中的部分不良预后因素(如CNV-H、MSI)均存在显著关联,仅POLE突变(良好预后因素)和CTNNB1突变(不良预后因素)表现出特殊的CIN特征,这为整合病理与分子分层系统提供了可行的切入点。
3. 研究思路总结与详细解析
本研究的核心目标是明确CIN与子宫内膜癌病理、分子预后因素的关联,构建整合病理、CIN基因签名及POLE/CTNNB1突变的早期子宫内膜样子宫内膜癌风险分层模型,技术路线遵循“公共数据挖掘-关联特征分析-特殊因素排除-模型构建验证”的闭环逻辑。
3.1 CIN与病理预后因素的关联分析
实验目的:验证CIN在子宫内膜癌组织中的异常表达特征,并明确其与病理预后因素的相关性。
方法细节:利用TCGA Uterine Corpus Endometrial Carcinoma(UCEC)队列、GSE63678、GSE17025等多个公共数据集,分析CIN25和CIN70两个经泛癌研究验证的CIN基因表达签名的水平差异,通过配对t检验、Mann-Whitney检验、单因素方差分析(ANOVA)及荟萃分析(STATA 12.0)比较良性与恶性组织、不同病理特征患者的CIN签名表达水平。
结果解读:在TCGA队列中,23例癌组织的CIN25和CIN70表达显著高于配对正常组织(CIN25:p<0.001;CIN70:p<0.001);GSE63678和GSE17025数据集也验证了恶性组织CIN签名的特异性高表达。进一步分析显示,病理分级越高(3级vs1-2级,CIN25标准化均数差SMD=0.985,95%CI 0.85-1.13,p=0.000)、非子宫内膜样组织类型、临床分期越晚(III-IV期vsI-II期,CIN25 SMD=0.602,95%CI 0.43-0.78,p=0.000)、肌层浸润越深(>50%vs<50%,p<0.05)、年龄越大(>60岁vs<60岁,p=0.0050)的患者,CIN签名表达水平越高,提示CIN与病理不良预后因素显著相关。
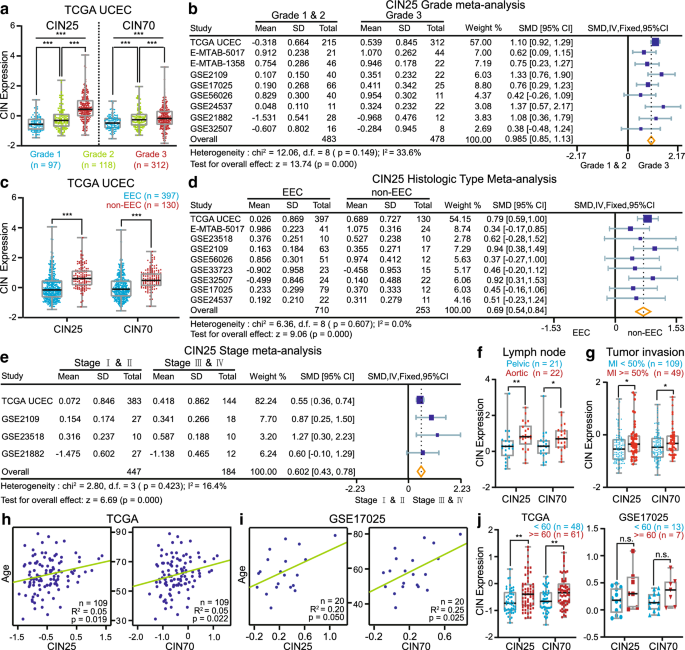
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析工具如R语言、SPSS、GraphPad Prism等进行数据挖掘与统计分析。
3.2 CIN与分子预后因素的关联分析
实验目的:探究CIN与子宫内膜癌分子预后因素的关系,明确特殊突变对CIN预后价值的干扰作用。
方法细节:分析TCGA分子亚型(POLE突变型、MSI、CNV-L、CNV-H)及POLE、CTNNB1等常见突变患者的CIN签名表达水平,通过Kaplan-Meier生存分析、Cox比例风险模型评估突变状态与CIN签名的预后价值。
结果解读:TCGA分子亚型中,CNV-H亚型的CIN签名表达最高,CNV-L亚型最低,MSI亚型居中,而预后最佳的POLE突变型CIN签名表达与CNV-H亚型相当(p>0.05);预后不良的CTNNB1突变型CIN签名表达显著低于野生型(p<0.05)。生存分析显示,POLE突变患者预后极佳(无复发或死亡事件),但CIN签名呈高表达;CTNNB1突变患者预后显著较差,但CIN签名呈低表达,这两种突变会干扰CIN签名的预后评估效能。
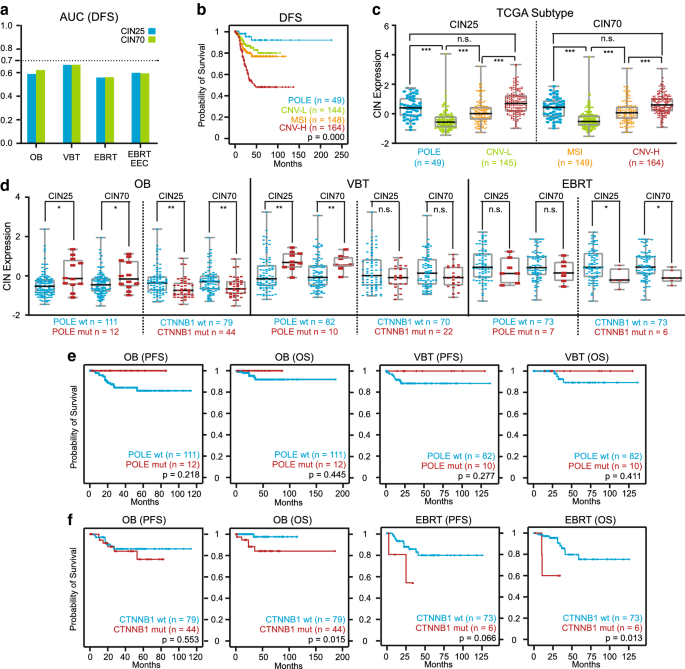
产品关联:文献未提及具体实验产品,领域常规使用cBioPortal、TCGA数据门户等公共数据库获取分子特征数据,利用生物信息学工具进行生存分析。
3.3 排除特殊突变后CIN的预后价值验证
实验目的:验证排除POLE/CTNNB1突变后,CIN签名在不同辅助放疗亚组中的独立预后价值。
方法细节:将TCGA I期子宫内膜样子宫内膜癌患者分为观察(OB)、阴道近距离放疗(VBT)、外照射放疗(EBRT)三个亚组,排除POLE/CTNNB1突变后,通过时间依赖ROC曲线确定CIN签名的最佳截断值,采用Kaplan-Meier分析、log-rank检验评估不同CIN分组的预后差异。
结果解读:排除POLE/CTNNB1突变后,OB亚组中CIN70的5年无病生存(DFS)AUC为0.76,CIN70高表达组预后显著差于低表达组;VBT亚组排除POLE突变后,CIN25的5年DFS AUC为0.71,高表达组5年DFS率显著更低;EBRT亚组排除CTNNB1突变后,CIN25的5年DFS AUC为0.62(整体)和0.72(子宫内膜样亚型),高表达组预后更差。此外,CIN签名的预后价值显著优于仅评估染色体内容的FGA(基因组改变比例)和非整倍体评分。
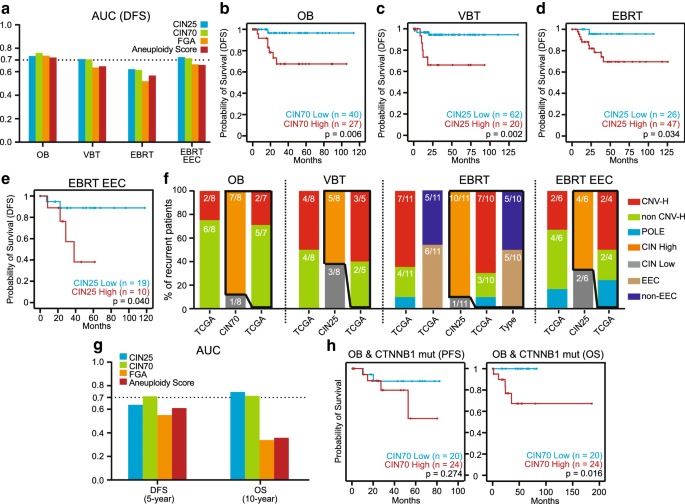
产品关联:文献未提及具体实验产品,领域常规使用R语言survivalROC包进行ROC曲线分析,采用Cox比例风险模型评估预后因素的独立价值。
3.4 整合风险分层模型的构建与验证
实验目的:构建整合病理、CIN基因签名及POLE/CTNNB1突变的风险分层模型,并验证其预后效能。
方法细节:基于病理特征、CIN基因签名表达水平及POLE/CTNNB1突变状态,将I期子宫内膜样子宫内膜癌患者分为低、中、高、极高危四个风险组,通过ROC曲线、Kaplan-Meier分析比较该模型与现有分层系统的预后效能。
结果解读:整合模型的5年DFS AUC为0.75,10年总生存(OS)AUC为0.76,显著高于指南病理分层、FGA、非整倍体评分及TCGA分子分层系统;Kaplan-Meier分析显示,四个风险组的DFS和OS均存在显著差异(p<0.001),可分别对应观察、VBT、EBRT、放疗联合系统治疗的术后辅助治疗推荐方案。
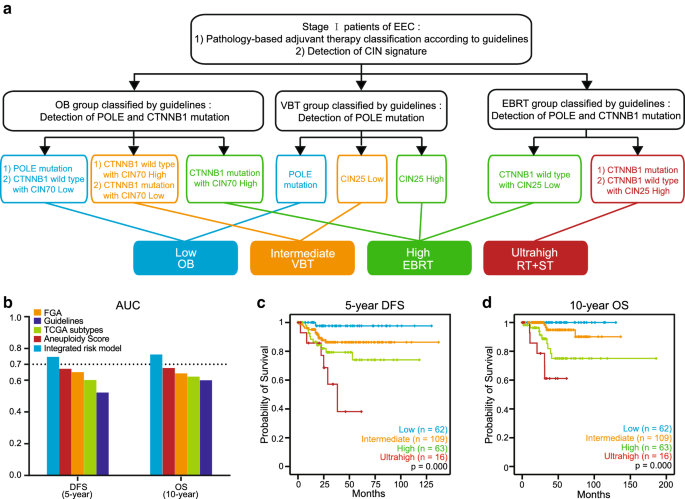
产品关联:文献未提及具体实验产品,领域常规使用生物信息学工具进行模型构建与验证,后续临床验证需采用实时荧光定量PCR(qRT-PCR)等方法检测CIN签名基因的表达水平。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究的核心Biomarker为CIN25和CIN70基因表达签名,属于基于基因表达的染色体不稳定性特征。筛选逻辑为采用已在泛癌研究中验证的CIN基因集,验证逻辑遵循“公共数据集验证-病理/分子关联分析-特殊突变排除-亚组预后验证-整合模型构建”的完整链条,确保Biomarker的特异性与预后价值。
研究过程详述
Biomarker来源为TCGA、GSE等公共数据库的子宫内膜癌组织基因表达数据,验证方法包括:1)通过多个独立数据集比较良性与恶性组织的CIN签名表达水平,确认其在肿瘤组织中的特异性升高;2)分析CIN签名与病理、分子预后因素的关联,明确其与不良预后因素的显著相关性;3)排除POLE/CTNNB1突变后,在不同辅助放疗亚组中验证其预后价值,其中OB亚组排除双突变后CIN70的5年DFS AUC为0.76,VBT亚组排除POLE突变后CIN25的5年DFS AUC为0.71;4)整合病理特征、CIN签名及突变状态构建风险分层模型,验证其对DFS和OS的预后效能。
核心成果提炼
该Biomarker的功能关联在于可有效区分不同风险的子宫内膜癌患者,整合模型将患者分为四个风险组,各组DFS和OS存在显著差异(p<0.001);创新性在于首次以CIN为桥梁整合病理与分子分层系统,解决了现有分层系统的局限性;统计学结果显示,整合模型的AUC显著高于现有分层系统,且对DFS和OS均有独立预后价值。该模型可为临床治疗方案选择提供更精准的依据,有望减少过度治疗与治疗不足,值得进一步的临床验证与优化。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。