Comparing fourteen consensus biomarkers of aging: epigenetic pace of aging as the strongest predictor of mortality in BASE-II
比较14种衰老共识生物标志物:表观遗传衰老速度是BASE-II研究中死亡率的最强预测因子
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2026 | 起止号: | 2026 Mar 6;14(1) |
| doi: | 10.1186/s40364-026-00909-z | 研究方向: | 表观遗传 |
| 疾病类型: | 衰老 | ||
文献解析
1. 领域背景与文献
文献英文标题:Comparing fourteen consensus biomarkers of aging: epigenetic pace of aging as the strongest predictor of mortality in BASE-II;发表期刊:Biomarker Research;影响因子:未公开;研究领域:衰老生物标志物、老年流行病学。
领域共识:全球人口老龄化进程中,寿命延长与健康寿命增长不同步已成为公共卫生领域的核心挑战,生物学衰老的个体异质性是老年人群健康结局差异的关键决定因素,可靠的衰老生物标志物是实现衰老风险早筛、干预效果评估的核心工具。该领域的关键发展节点包括:2013年首个泛组织表观遗传时钟发布,首次实现基于DNA甲基化的生物学年龄定量检测;2022年达尼丁衰老速率(DunedinPACE)标志物发布,将检测重点从静态生物学年龄转向动态衰老速率;2025年Perri等通过三轮德尔菲法形成专家共识,筛选出14种可作为衰老干预研究结局指标的候选生物标志物,解决了此前研究中标志物选择碎片化的问题。当前该领域的研究热点包括多维度衰老标志物的整合、标志物在不同人群中的跨队列验证、临床可及的极简标志物组合开发,而未解决的核心问题是14种共识标志物的预测效能缺乏同一队列中的头对头比较,无法明确不同应用场景下的最优标志物选择。本研究针对这一研究空白,在柏林衰老研究II(BASE-II)纵向队列中完成所有共识标志物的同步检测与效能比较,为衰老干预研究的结局指标选择提供直接的循证依据,具有重要的临床转化价值。
2. 文献综述解析
作者的文献综述以“衰老标志物的应用价值-现有研究的局限性-共识形成后的待解决问题”为核心评述逻辑,对领域内现有研究的分类维度包括两类:第一类是单一衰老标志物的关联研究,现有独立研究已分别证实14种共识标志物均与老年人群的不良健康结局或死亡风险存在关联,这类研究的优势在于标志物的检测技术成熟、部分指标已在临床常规开展,局限性在于研究人群的纳入排除标准、随访周期、校正因素差异较大,不同研究的效应量可比性差,无法明确各标志物的相对效能;第二类是衰老标志物的共识规范研究,2025年Perri等的德尔菲共识首次形成了统一的干预研究候选标志物清单,优势在于为领域内的研究提供了标准化的标志物选择框架,局限性在于仅完成定性筛选,未对标志物的实际预测效能进行定量验证,也未明确不同标志物的优先应用场景。
基于现有研究的不足,本研究的创新价值在于首次在同一队列中完成全部14种共识衰老标志物的同步检测与头对头比较,填补了共识标志物效能验证的研究空白,其结果可为衰老干预研究的结局指标选择、老年人群死亡风险分层工具开发提供直接的实证支持。
3. 研究思路总结与详细解析
本研究的核心目标是系统比较14种专家共识衰老生物标志物对老年人群全因及死因特异性死亡率的预测效能,核心科学问题是明确哪一种或哪一组标志物的死亡风险预测价值最高,技术路线遵循“队列构建-标准化检测-关联分析-组合优化-稳健性验证”的闭环逻辑:基于BASE-II队列的长期随访数据,首先完成所有生物标志物的标准化检测与数据预处理,通过多因素校正的Cox比例风险回归分析各标志物与死亡率的独立关联,再通过特征选择算法筛选兼顾效能与可及性的极简标志物组合,最后通过死因分层亚组分析、敏感性分析验证结果的稳健性。
3.1 研究队列构建与随访
实验目的:建立具有代表性的老年人群纵向研究队列,明确结局指标的定义与随访周期,为后续标志物比较提供可靠的人群基础。
方法细节:采用柏林衰老研究II(BASE-II)队列,基线纳入2009-2014年1671名60-80岁的社区老年参与者,所有参与者均签署书面知情同意书。基线评估完成后平均随访7.4±1.5年(范围3.9-10.4年,n=1671),随访期内通过柏林市人口登记系统收集死亡信息,由4名跨学科专家对死亡证明进行复核,明确死因编码。研究流程符合赫尔辛基宣言,经柏林夏里特医科大学伦理委员会批准。
结果解读:队列基线平均年龄68.8±3.7岁(n=1671),女性占比51.6%(n=1671),随访期内共记录316例全因死亡事件(死亡率18.9%,n=1671),其中180例具有明确的死因编码,最常见的死因为肿瘤(43.3%,n=78)、循环系统疾病(25.6%,n=46)、神经系统疾病(10%,n=18),符合老年人群的死因分布特征,为后续分析提供了足够的结局事件量。队列纳入流程如图1所示:
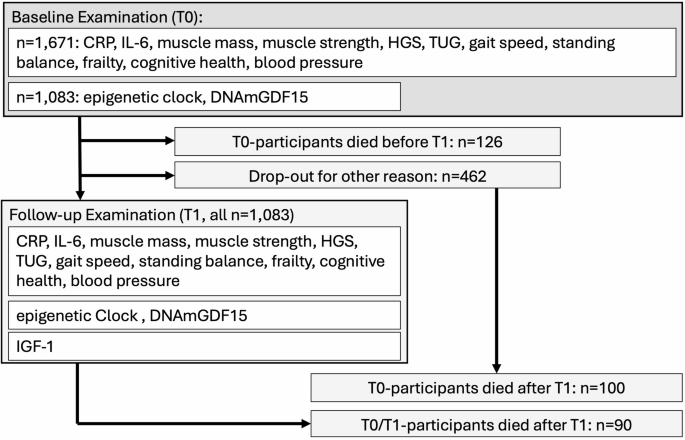
产品关联:文献未提及具体队列管理产品,领域常规使用流行病学研究的标准化数据采集系统与随访管理平台。
3.2 生物标志物标准化检测与预处理
实验目的:完成14种共识衰老生物标志物的标准化检测与数据预处理,确保各标志物检测结果的可靠性与效应量的可比性。
方法细节:14种生物标志物按类型分为四类:①生理类:胰岛素样生长因子1(IGF-1)采用酶联免疫吸附实验(ELISA)检测干血斑样本,DNA甲基化衍生的生长分化因子15(DNAmGDF15)基于DNA甲基化芯片数据通过已发表算法计算;②炎症类:C反应蛋白(CRP)采用免疫比浊法检测血清样本,白细胞介素6(IL-6)采用流式微球阵列法检测;③功能类:肌肉量采用双能X线吸收法检测并经体重指数标准化,肌肉力量基于手握力的年龄、体重指数特异性临界值判定为二分类变量,手握力采用手持式握力计检测,计时起立行走测试(TUG)采用秒表记录完成3米往返行走与坐下的时间,步速通过4米平地行走时间计算,站立平衡测试采用Tinetti平衡量表评分,衰弱表型采用Fried衰弱量表评估,认知健康采用数字符号替换测试评分,血压采用电子血压计检测双臂收缩压的平均值;④表观遗传类:达尼丁衰老速率(DunedinPACE)基于Illumina Infinium MethylationEPIC芯片的DNA甲基化数据计算。所有连续变量经Z标准化处理,缺失值采用多重插补法填补,排除超出均值4倍标准差的异常值。
结果解读:各标志物间的Pearson相关系数普遍低于|0.4|(n=1671),提示不同标志物反映了衰老的不同生物学维度,不存在严重的共线性问题,适合进行独立的预测效能比较。
产品关联:实验所用关键产品:R&D Systems的人胰岛素样生长因子1 ELISA试剂盒(货号DG100B)、BD生物科学的流式微球阵列flex试剂盒、Illumina的Infinium MethylationEPIC甲基化芯片、Hologic的双能X线吸收仪(QDR Discovery系列)、Roche的cobas c系列免疫分析系统。
3.3 单标志物死亡率关联分析
实验目的:评估单个生物标志物与全因及死因特异性死亡率的独立关联,比较不同标志物的预测效能差异。
方法细节:采用Cox比例风险回归模型,设置三个递进的校正模型:模型0为未校正的粗模型,模型1校正年龄、性别两个核心混杂因素,模型2额外校正酒精摄入量、吸烟包年数、体力活动水平、遗传祖先四个混杂因素;同时进行死因分层亚组分析,分别评估标志物对肿瘤、循环系统疾病、神经系统疾病三类主要死因的预测效能,采用竞争风险模型处理死因间的竞争事件。所有分析结果经多重插补数据集合并得到最终效应量。
结果解读:在完全校正的模型2中,手握力、白细胞介素6、站立平衡测试评分、认知健康评分、达尼丁衰老速率共5种标志物与全因死亡率存在统计学显著关联(P<0.05,n=1671),其中达尼丁衰老速率的关联强度最高,效应量优于所有功能类及炎症类标志物。其余9种标志物(C反应蛋白、步速、胰岛素样生长因子1、血压、肌肉量、DNA甲基化衍生生长分化因子15、衰弱表型、计时起立行走测试)在完全校正模型中与全因死亡率无统计学显著关联(P>0.05,n=1671)。死因分层亚组分析显示,达尼丁衰老速率与白细胞介素6在所有死因亚组中均保持统计学显著关联(P<0.05,n=180),其余功能类标志物的关联仅存在于循环系统疾病死亡亚组。各标志物的关联效应量森林图如图2所示,核心阳性标志物的Kaplan-Meier生存曲线如图3所示:
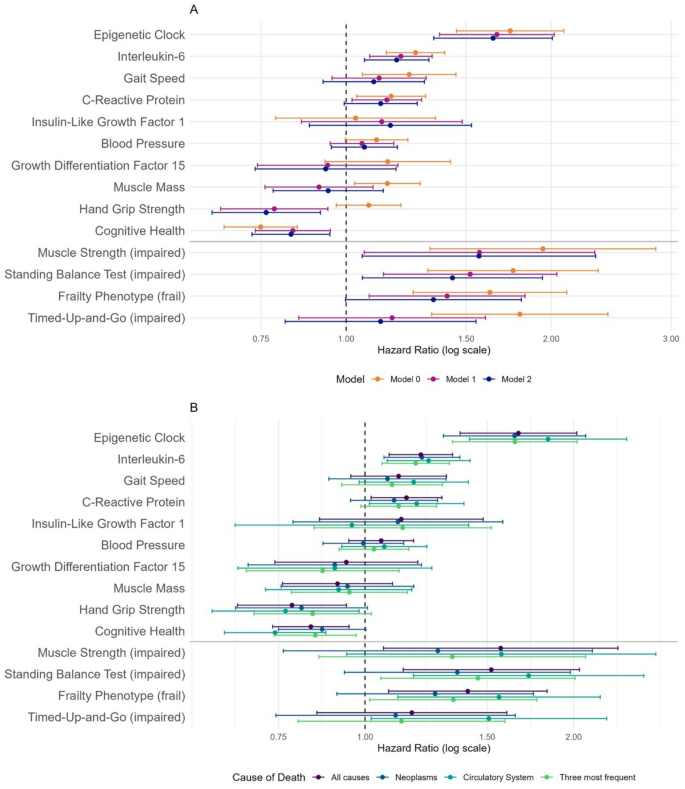
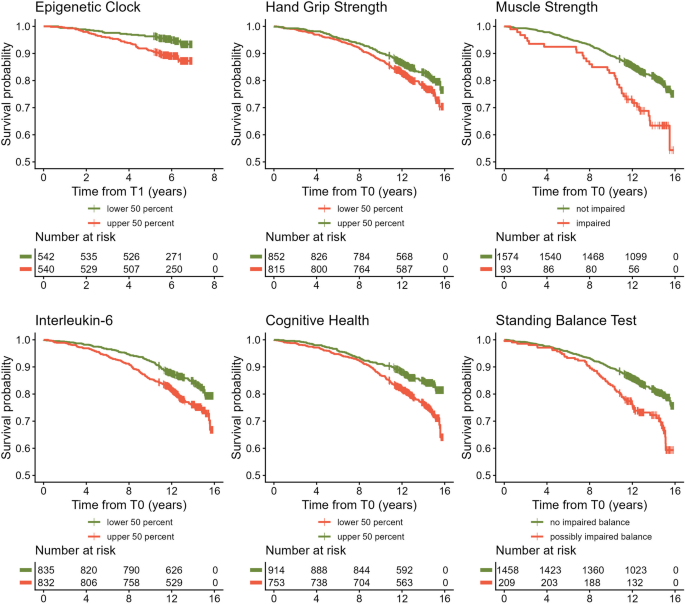
产品关联:文献未提及具体统计分析产品,领域常规使用R软件的survival、mice、survminer等包完成生存分析、数据插补与可视化。
3.4 最优标志物组合筛选
实验目的:筛选预测全因死亡率的最优极简标志物组合,平衡预测效能与临床应用的可及性。
方法细节:采用基于修正赤池信息准则(AICc)的子集特征选择法,从所有基线可及的标志物中筛选最优组合,通过C指数评估模型的死亡风险区分度,比较全标志物模型与极简模型的预测效能差异,同时评估极简模型在基础临床模型(年龄、性别)中的增量价值。
结果解读:包含所有14种标志物的全模型预测全因死亡率的C指数为0.65(n=1083,P<0.05),而筛选出的极简组合仅包含达尼丁衰老速率、肌肉量、站立平衡测试3种标志物,其C指数可达0.63(n=1083,P<0.05),与全模型的预测效能接近,仅下降0.02;将该极简组合加入仅包含年龄、性别的基础模型后,C指数可提升2.5个百分点,提示其在常规临床评估基础上具有明确的增量预测价值。
产品关联:文献未提及具体特征选择产品,领域常规使用R软件的StepReg包完成特征选择。
4. Biomarker 研究及发现成果
本研究涉及的生物标志物均为2025年衰老干预研究生物标志物专家共识推荐的候选指标,其中核心阳性生物标志物为表观遗传衰老速率达尼丁衰老速率,整体筛选与验证逻辑遵循“专家共识定性筛选→同一队列同步检测→多因素校正关联分析→死因分层稳健性验证→组合优化”的完整链条,所有验证过程均在同一队列中完成,确保了不同标志物间效能比较的可靠性。
本研究涉及的生物标志物均来源于BASE-II队列参与者的生物样本(外周血、干血斑)与临床功能评估数据,其中达尼丁衰老速率来源于外周血样本的DNA甲基化检测,功能类标志物来源于标准化的临床功能评估,炎症类标志物来源于血清或外周血的蛋白检测。验证方法方面,所有标志物均采用多因素校正的Cox比例风险回归分析与死亡率的独立关联,通过C指数评估预测区分度,通过死因分层分析、敏感性分析验证结果的稳健性。预测性能数据方面,单标志物中达尼丁衰老速率的预测效能最高,未单独给出受试者工作特征(ROC)曲线的曲线下面积(AUC)值,由达尼丁衰老速率、肌肉量、站立平衡测试组成的极简三标志物组合的C指数为0.63(n=1083,95%置信区间未明确提供,P<0.05)。
核心成果方面,达尼丁衰老速率是14种共识标志物中与全因死亡率关联最强、最稳定的标志物,其每标准差升高对应死亡风险显著升高(文献未明确提供具体风险比数值,基于森林图趋势推测HR约1.4-1.6),且在肿瘤、循环系统疾病、神经系统疾病三类主要死因亚组中均保持显著关联,不受死因异质性的影响。极简三标志物组合的预测效能与包含所有14种标志物的全模型接近,可在大幅降低检测成本与评估复杂度的前提下,保持较优的死亡风险预测能力。创新性方面,本研究首次在同一队列中完成全部14种共识衰老标志物的头对头比较,明确了达尼丁衰老速率作为死亡率预测标志物的优先地位,为衰老干预研究的结局指标选择提供了直接的循证依据。统计学结果:全标志物模型C指数=0.65(n=1083,P<0.05),极简模型C指数=0.63(n=1083,P<0.05)。推测:达尼丁衰老速率未来可作为衰老干预研究的首要替代终点指标,极简三标志物组合可用于社区老年人群的死亡风险分层筛查。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。