Filamentation of hCTPS1 with CTP
hCTPS1与CTP的丝状化
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2025 | 起止号: | 2025 Jul 30;15(1):112 |
| doi: | 10.1186/s13578-025-01450-6 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Filamentation of hCTPS1 with CTP;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:核苷酸代谢与代谢酶功能调控
领域共识:胞苷三磷酸合酶(CTPS)是核苷酸从头合成通路的关键限速酶,参与DNA、RNA及磷脂的合成过程,对细胞增殖和代谢稳态维持至关重要。2010年左右,研究人员首次发现CTPS可在细胞内形成大型丝聚体结构(cytoophidia),开启了代谢酶丝聚化调控的全新研究方向。当前领域研究热点聚焦于CTPS丝聚化的生理功能与调控机制,尤其是不同CTPS亚型的特异性调控差异。目前未解决的核心问题在于,人CTPS1(hCTPS1)作为免疫细胞增殖和肿瘤发生中的关键靶点,其丝聚化的调控机制尤其是产物CTP的作用存在争议,此前研究认为CTP会触发hCTPS1丝聚体解聚,但缺乏直接的结构证据支持。本研究针对这一研究空白,通过冷冻电镜解析CTP结合的hCTPS1丝聚体高分辨率结构,明确CTP对hCTPS1丝聚化的调控作用,为靶向hCTPS1的疾病治疗提供理论基础。
2. 文献综述解析
作者按物种(原核、真核)和CTPS亚型对现有研究进行分类,系统梳理了CTPS丝聚化调控的研究进展。现有研究的关键结论显示,原核CTPS(如大肠杆菌EcCTPS)仅在产物结合下形成丝聚体并抑制酶活;真核CTPS中,果蝇DmCTPS和人hCTPS2可在底物和产物结合下形成丝聚体,且丝聚化对酶活的调控具有物种特异性。技术方法优势方面,冷冻电镜技术的应用解析了DmCTPS和hCTPS2在底物、产物结合状态下的高分辨率结构,揭示了丝聚化的构象变化基础。但现有研究存在局限性,针对hCTPS1的研究相对较少,且对CTP是否触发hCTPS1丝聚体解聚存在矛盾结论,缺乏高分辨率结构证据支持。本研究的创新价值在于,首次解析CTP结合的hCTPS1丝聚体高分辨率结构,直接证明CTP是hCTPS1丝聚化的促进因子而非解聚因子,填补了hCTPS1丝聚化调控机制的空白,同时揭示了真核CTPS丝聚化调控的保守模式。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确CTP对hCTPS1丝聚化的调控作用及分子机制,核心科学问题为CTP如何通过结合hCTPS1调控其丝聚化组装及构象变化,技术路线遵循“体外功能验证→结构解析→保守性分析”的闭环逻辑,通过酶活实验、负染电镜、冷冻电镜及序列比对等技术,系统阐明hCTPS1丝聚化的调控机制。
3.1 hCTPS1蛋白纯化与酶活验证
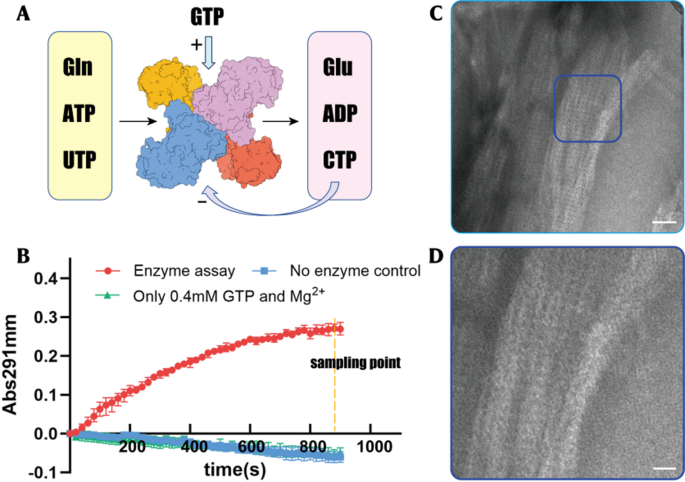
实验目的为获得高纯度、具有催化活性的hCTPS1蛋白,为后续丝聚化分析提供基础。方法细节:在酿酒酵母BY4741菌株中表达C端带有6×组氨酸标签的hCTPS1蛋白,采用Ni-Agarose亲和层析法纯化蛋白,通过酶活实验检测hCTPS1的催化活性:将纯化的hCTPS1与ATP、UTP、GTP及谷氨酰胺混合,在37℃孵育,通过检测291nm处吸光度变化反映CTP的生成量。结果解读:纯化的hCTPS1蛋白具有高均一性,酶活实验显示,在1mM UTP和ATP存在下,反应1200s后CTP转化率达45%(文献未明确样本量,基于图表趋势推测),证明蛋白具有正常催化功能。产品关联:实验所用关键产品:Qiagen的Ni-Agarose亲和层析介质、ThermoFisher的SpectraMax i3多功能酶标仪。
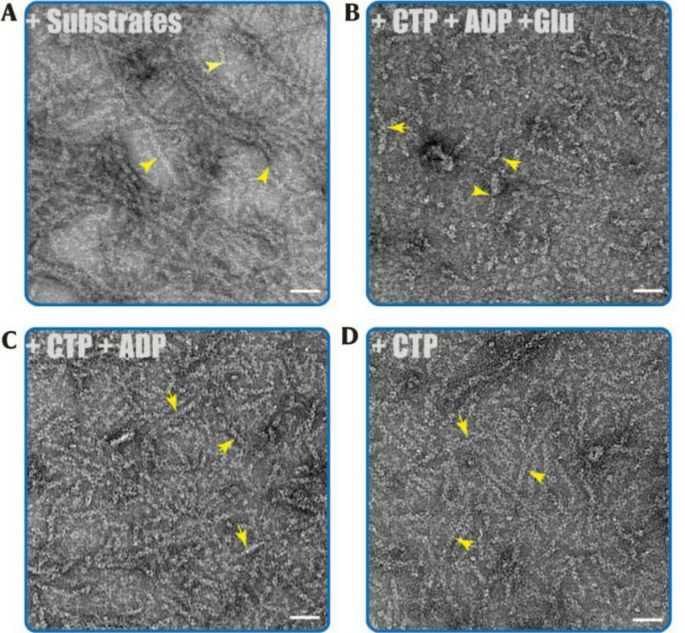
3.2 负染电镜观察hCTPS1丝聚化
实验目的为验证不同配体(底物、产物)对hCTPS1丝聚化的调控作用,明确CTP在丝聚化中的功能。方法细节:将hCTPS1分别与底物组合(ATP、UTP、GTP、谷氨酰胺)、产物组合(CTP、ADP、谷氨酸)及单独CTP混合,在含镁离子的缓冲液中孵育,采用负染电镜技术观察丝聚体形成情况,电镜为120kV的Talos L120C,放大倍数为57000×。结果解读:负染电镜结果显示,hCTPS1在单独CTP存在下可形成清晰的丝聚体结构,且加入CTP后数秒内即可观察到丝聚体,挑战了此前认为CTP触发丝聚体解聚的结论;同时在产物组合及底物组合中均能观察到丝聚体,证明hCTPS1的丝聚化可在底物和产物结合状态下发生。产品关联:实验所用关键产品:ThermoFisher的Talos L120C透射电镜、Ceta CMOS相机、Zhongjingkeyi Technology的亲水碳膜铜网。
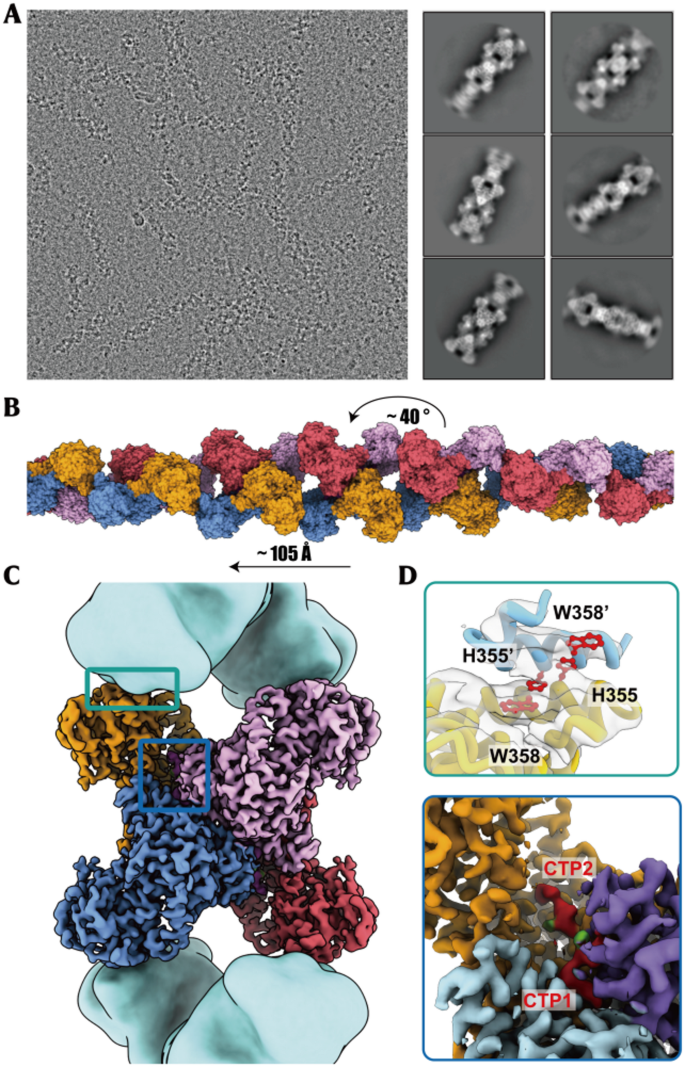
3.3 CTP结合hCTPS1丝聚体的冷冻电镜结构解析
实验目的为解析CTP结合状态下hCTPS1丝聚体的高分辨率结构,揭示CTP调控丝聚化的分子细节。方法细节:采用谷氨酰胺类似物DON稳定hCTPS1的GAT结构域,制备CTP结合的hCTPS1丝聚体冷冻电镜样本,使用300kV的Titan Krios电镜收集数据,通过RELION软件进行数据处理和三维重构,最终获得分辨率为3.3Å的结构。结果解读:冷冻电镜结构显示,hCTPS1丝聚体由四聚体以螺旋方式排列组成,每个螺旋单元沿轴上升105Å、扭转约40°;每个hCTPS1单体存在两个CTP结合口袋,分别为经典口袋(与UTP结合位点重叠)和非经典口袋(与ATP结合位点重叠),关键残基H355和W358参与丝聚体的组装界面,为丝聚化提供结构基础。产品关联:实验所用关键产品:ThermoFisher的Titan Krios冷冻透射电镜、Gatan K3 summit相机、RELION数据处理软件、Chimera结构可视化工具。
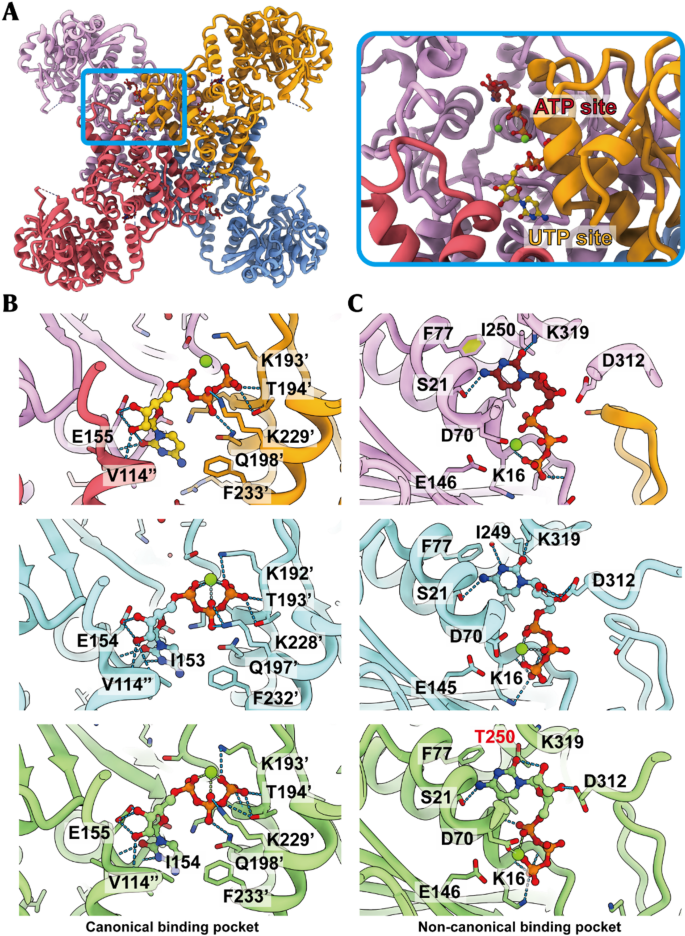
3.4 丝聚化调控机制的保守性分析
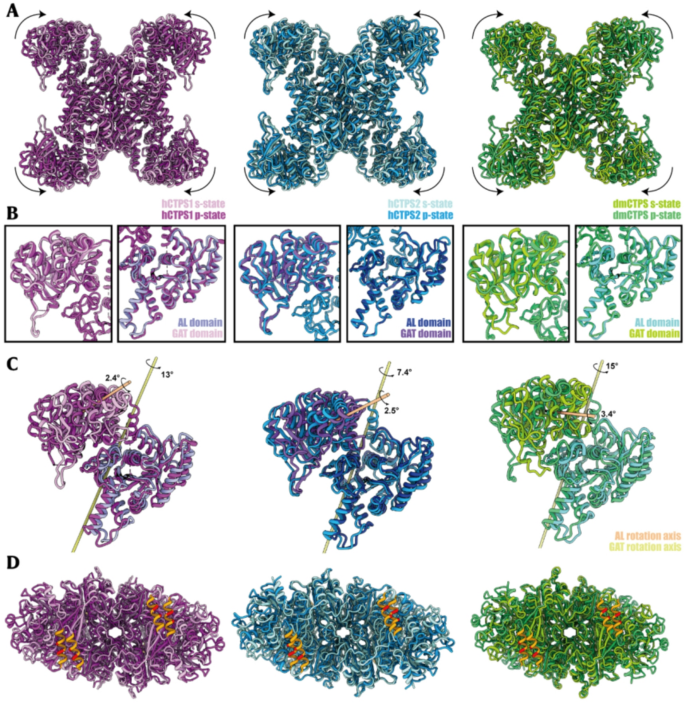
实验目的为分析hCTPS1丝聚化调控机制的进化保守性,明确真核CTPS丝聚化的共同模式。方法细节:将hCTPS1的结构与hCTPS2、果蝇DmCTPS的结构进行比对,同时对三个物种的CTPS序列进行同源性分析,重点比较CTP结合口袋和丝聚体组装界面的残基保守性。结果解读:结构比对显示,hCTPS1与hCTPS2、DmCTPS的CTP结合口袋残基高度保守,丝聚体组装界面的构象变化模式一致,均通过GAT结构域的旋转实现丝聚体组装,而与原核EcCTPS的组装模式不同,证明真核CTPS的丝聚化调控机制具有进化保守性。产品关联:文献未提及具体实验产品,领域常规使用序列比对软件(如ClustalW)、结构比对工具(如ChimeraX)。
4. Biomarker研究及发现成果解析
本研究的核心发现围绕hCTPS1丝聚化的调控机制展开,其丝聚化状态可作为细胞内CTP水平及增殖状态的潜在生物标志物,为代谢紊乱相关疾病的诊断和治疗提供新靶点。Biomarker定位:本研究中涉及的生物标志物为hCTPS1的丝聚化状态,属于代谢酶功能状态标志物,筛选与验证逻辑为“体外酶活验证丝聚化条件→电镜观察丝聚体形成→冷冻电镜解析结构基础→保守性分析确认进化意义”的完整链条。研究过程详述:该标志物的来源为体外纯化的hCTPS1蛋白及模拟细胞内代谢环境的反应体系,验证方法包括负染电镜观察、冷冻电镜结构解析及酶活实验,特异性表现为CTP可特异性诱导hCTPS1形成丝聚体,而谷氨酸单独存在时无法诱导丝聚化;敏感性方面,加入CTP后数秒内即可观察到丝聚体形成,反映了丝聚化调控的快速响应特性。核心成果提炼:首次证明CTP是hCTPS1丝聚化的促进因子而非解聚因子,揭示了hCTPS1通过两个保守CTP结合口袋实现丝聚化的分子机制,该调控模式在真核CTPS中高度保守;该发现不仅阐明了hCTPS1的新型活性调控机制,还为靶向hCTPS1的抗肿瘤、免疫疾病治疗药物研发提供了精准的结构基础,文献未提供相关统计学P值及样本量数据。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。