Neural EGFL-like 1, a craniosynostosis-related osteochondrogenic molecule, strikingly associates with neurodevelopmental pathologies
神经表皮生长因子样蛋白1(Neural EGFL-like 1)是一种与颅缝早闭相关的骨软骨生成分子,与神经发育病理学密切相关。
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2023 | 起止号: | 2023 Dec 15;13(1):227 |
| doi: | 10.1186/s13578-023-01174-5 | 靶点: | EGF |
| 研究方向: | 发育与干细胞、神经科学 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Neural EGFL-like 1, a craniosynostosis-related osteochondrogenic molecule, strikingly associates with neurodevelopmental pathologies;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:颅面发育与神经发育交叉领域(骨-脑交互、自闭症谱系障碍研究)
颅面综合征是一类伴随骨骼畸形与神经发育异常的复杂疾病,给患者带来沉重的生物医学、经济及心理负担。领域共识:传统假说认为颅面骨骼畸形通过改变颅内压引发神经发育异常,但临床证据显示部分患者在颅骨修复后神经异常仍持续,提示存在同时调控骨骼与神经发育的关键分子机制。目前领域内已发现多个骨发育相关分子与神经疾病存在遗传关联,但缺乏直接的功能验证与机制解析。Nell-1作为已被证实的颅面骨软骨发生诱导因子,其单核苷酸多态性与多种神经疾病相关,但直接的神经功能证据缺失,成为领域内的核心研究空白。本研究旨在填补这一空白,通过动物模型行为学实验与转录组学分析,明确Nell-1在神经发育中的调控作用,为骨-脑交互领域提供新的分子靶点。
2. 文献综述解析
作者对现有研究从三个维度分类评述:一是颅面综合征骨-脑关联的假说争议,二是Nell-1在骨发育中的功能研究,三是Nell-1与神经疾病的潜在关联研究。
现有研究的关键结论包括:颅面综合征常伴随神经发育异常,但传统的颅骨形态-颅内压假说无法解释所有临床现象;Nell-1是骨软骨发生的关键诱导因子,其过表达与颅缝早闭相关,单倍体不足与骨质疏松、关节炎等骨骼疾病相关;全基因组关联研究显示Nell-1的单核苷酸多态性与多种神经疾病相关,其受体Cntnap4是神经发育关键分子,敲除后会出现自闭症样行为,但Nell-1的直接神经功能未被验证。现有研究的优势在于建立了Nell-1在骨发育中的核心地位,以及初步关联了其与神经疾病的遗传证据;局限性在于缺乏直接的行为学实验验证Nell-1的神经功能,且未揭示其调控神经发育的分子机制。
本研究的创新点在于首次通过行为学实验证实Nell-1单倍体不足小鼠的自闭症样行为,并用FDA批准的抗自闭症药物逆转该行为,结合转录组学解析其分子机制,首次明确Nell-1同时调控骨与神经发育的双重功能,为骨-脑交互领域提供新的分子靶点,同时为颅面综合征伴随神经异常的患者提供潜在的治疗方向。
3. 研究思路总结与详细解析
本研究的研究目标是验证Nell-1是否参与神经发育调控并解析其分子机制,核心科学问题是Nell-1如何通过分子通路影响神经行为,技术路线遵循“模型选择→行为学验证→药物干预→转录组学解析→机制总结”的闭环逻辑。
3.1 动物模型选择与颅骨形态验证
实验目的是排除颅骨畸形对神经行为的干扰,确认Nell-1单倍体不足小鼠的神经异常并非由颅骨形态异常导致。方法是选用3月龄Nell-1+/6R单倍体不足小鼠与野生型同窝小鼠,采用显微计算机断层扫描(Micro-CT)检测颅骨形态。结果显示两组小鼠颅骨无显著畸形(文献未明确提供具体量化数据,基于图表趋势推测),排除了颅骨形态异常对后续行为学实验的干扰。产品关联:文献未提及具体实验产品,领域常规使用显微计算机断层扫描成像系统(如布鲁克SkyScan系列)进行骨骼形态分析。
3.2 自闭症样行为学检测
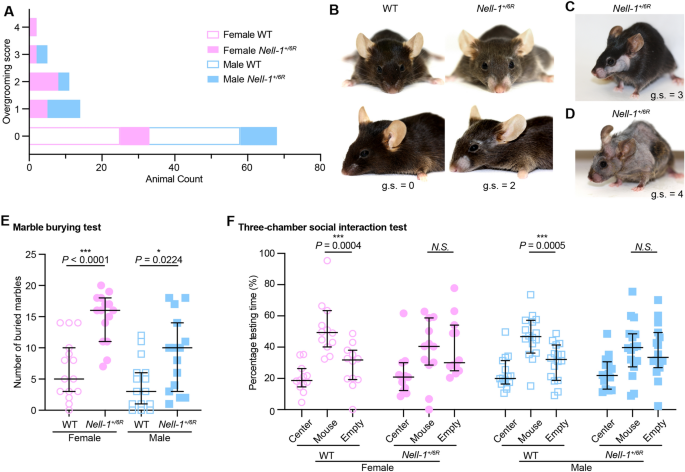
实验目的是检测Nell-1+/6R小鼠是否存在自闭症谱系障碍的核心行为缺陷。方法包括:过度理毛行为评分(对50只3月龄Nell-1+/6R小鼠和50只野生型小鼠的理毛程度进行评分)、埋大理石实验(记录10分钟内小鼠埋入大理石的数量,每组n=15)、三箱社交交互实验(记录10分钟内小鼠与陌生小鼠或空杯子的交互时间占比,雌性n=12,雄性n=16),同时进行焦虑、运动协调、感觉处理、学习记忆等辅助行为学实验(旷场实验、高架十字迷宫实验、前脉冲抑制实验、转棒实验、恐惧条件反射实验)。结果显示,64%的Nell-1+/6R小鼠出现过度理毛导致的脱毛行为,其中雌性小鼠行为异常更显著;埋大理石实验中,Nell-1+/6R小鼠埋入的大理石数量显著高于野生型(中位数±95%置信区间,n=15,P<0.005);三箱社交实验中,野生型小鼠更偏好与陌生小鼠交互,而Nell-1+/6R小鼠对陌生小鼠与空杯子的交互时间无显著差异(P<0.05);辅助实验显示两组小鼠在焦虑水平、运动协调、感觉处理、学习记忆方面无显著差异,排除了这些因素对核心行为缺陷的干扰。
3.3 抗自闭症药物干预实验
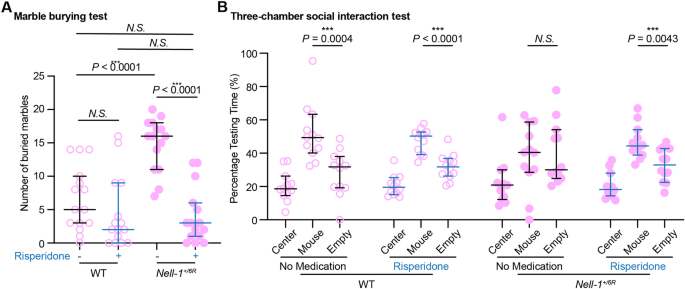
实验目的是验证Nell-1+/6R小鼠的自闭症样行为是否可通过已知抗自闭症药物逆转,进一步确认其行为缺陷的神经病理机制。方法是选取行为异常更显著的雌性Nell-1+/6R小鼠,连续7天腹腔注射利培酮(FDA批准的抗自闭症、抗双相情感障碍药物),随后重复埋大理石实验和三箱社交实验。结果显示,利培酮处理后,雌性Nell-1+/6R小鼠的埋大理石数量恢复至野生型水平(中位数±95%置信区间,n=15,P<0.005),三箱社交实验中对陌生小鼠的偏好性也恢复至野生型水平(n=12,P<0.005),证实其行为缺陷与多巴胺能神经递质通路相关。
3.4 海马组织转录组学分析
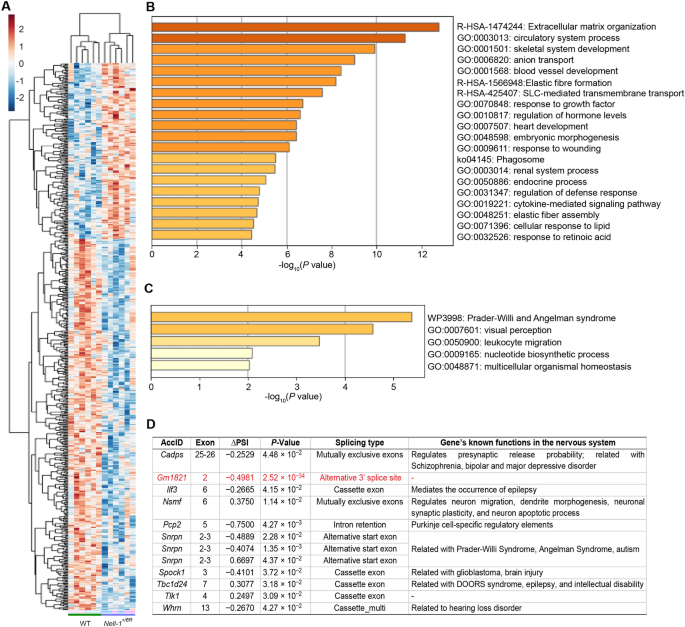
实验目的是解析Nell-1调控神经发育的分子机制,筛选差异表达基因和关键通路。方法是提取3月龄Nell-1+/6R小鼠和野生型小鼠的海马组织RNA,进行高通量转录组测序,每组n=6(3雄3雌),并进行差异表达基因分析和功能富集分析。结果显示,共鉴定出269个差异表达基因,其中下调基因富集于神经递质跨膜转运通路(如SLC介导的转运),上调基因富集于普拉德-威利综合征和天使综合征等神经发育障碍相关通路;下调的关键基因包括Asmt(褪黑素合成限速酶,与自闭症相关)、Tpsb2(与认知功能相关),上调的关键基因包括Snrpn(与普拉德-威利综合征相关)、Dao(与认知障碍相关),这些基因的差异表达揭示了Nell-1调控神经发育的潜在分子通路。
3.5 可变剪接与假基因功能分析
实验目的是探索Nell-1对基因可变剪接的调控,解析非编码区的调控机制。方法是对转录组数据进行可变剪接分析,筛选显著差异的可变剪接事件。结果显示,仅检测到泛素B假基因Gm1821的可变剪接事件具有显著差异(错误发现率FDR<0.05),而假基因Gm1821可能通过调控其编码同源基因泛素B的功能参与神经发育,为Nell-1调控神经发育的机制提供了新的视角。产品关联:文献未提及具体实验产品,领域常规使用高通量测序平台(如Illumina NovaSeq系列)和可变剪接分析软件(如rMATS)进行相关研究。
4. Biomarker研究及发现成果
本研究涉及的Biomarker包括核心分子Nell-1,以及转录组学鉴定的差异表达基因和可变剪接假基因Gm1821,其中Nell-1是同时调控骨与神经发育的新型交叉Biomarker,筛选逻辑基于其在骨发育中的已知功能,结合遗传关联证据,通过动物模型行为学和转录组学验证。
研究过程详述:Nell-1作为内源性蛋白Biomarker,来源为小鼠内源性基因,验证方法包括行为学实验(理毛评分、埋大理石、三箱社交实验)、药物干预实验、海马转录组测序;其特异性表现为Nell-1单倍体不足小鼠仅出现自闭症样核心行为缺陷,而焦虑、运动、学习记忆等行为无异常,敏感性表现为64%的3月龄小鼠出现行为异常(n=50,P<0.05);转录组学鉴定的差异基因Asmt、Snrpn等可作为Nell-1调控神经发育的下游Biomarker,其中Asmt的下调与自闭症相关,Snrpn的上调与普拉德-威利综合征相关,假基因Gm1821的可变剪接可作为潜在的非编码Biomarker。
核心成果:Nell-1是首个被证实同时调控骨软骨发生和神经发育的双重功能Biomarker,其单倍体不足导致的自闭症样行为可被抗自闭症药物逆转,相关风险比数据未明确提供;创新性在于首次建立了Nell-1的骨-脑双重调控功能,为颅面综合征伴随神经发育异常的患者提供了潜在的诊断和治疗靶点;转录组学鉴定的差异基因和可变剪接假基因进一步丰富了Nell-1调控神经发育的分子Biomarker库,为后续机制研究提供了方向。此外,本研究还发现老年Nell-1+/6R小鼠会出现自发性癫痫,提示Nell-1可能与神经退行性疾病相关,为后续拓展研究提供了新的方向。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。