Open conformation of hERG channel turrets revealed by a specific scorpion toxin BmKKx2
蝎毒素BmKKx2揭示了hERG通道塔状体的开放构象
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2014 | 起止号: | 2014;4:18 |
| doi: | 10.1186/2045-3701-4-18 | 靶点: | ERG |
文献解析
1. 领域背景与文献引入
文献英文标题:Open conformation of hERG channel turrets revealed by a specific scorpion toxin BmKKx2;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:钾离子通道结构与功能(hERG通道与蝎毒素相互作用机制)
钾离子通道是介导钾离子跨膜外流的重要膜蛋白,参与神经传导、心肌复极化、细胞增殖等多种生理病理过程,结构上可分为内向整流型、钙激活型、电压门控型等不同类型。由于真核钾离子通道结构复杂,晶体结构解析存在技术挑战,目前仅解析了Kv1.2、Kir2.2等少数真核钾离子通道的晶体结构。对比已解析的晶体结构发现,不同钾离子通道的胞外孔道入口(包括塔区(turret)和滤器区)存在显著构象差异。近年来,特异性蝎毒素作为分子探针被广泛用于探究钾离子通道的结构功能关系,例如电压门控钾通道Kv1.2的10个氨基酸的塔区在结合蝎毒素maurotoxin时呈开放构象,不影响毒素结合;小电导钙激活钾通道SKCa3的17个氨基酸的塔区形成“肽筛选器”紧凑构象,选择性控制毒素结合;大电导钙激活钾通道BKCa的19个氨基酸的塔区在结合蝎毒素charybdotoxin(ChTX)时呈开放构象,而结合辅助β4亚基后转为紧凑的“头盔”构象。
然而,对于人类ether-a-go-go相关基因钾离子通道(hERG通道),其具有独特的长塔区(含40个氨基酸),该塔区在蝎毒素结合中的作用存在争议:一项半胱氨酸扫描突变与计算模拟研究认为塔区的螺旋区参与蝎毒素BeKm-1的结合,另一项计算模拟研究则认为塔区螺旋区远离结合的毒素。本研究以新鉴定的hERG通道特异性蝎毒素BmKKx2为分子探针,采用丙氨酸扫描突变技术重新探究hERG通道塔区的构象与功能,解决领域内的争议,丰富钾离子通道塔区的结构功能多样性。
2. 文献综述解析
本文献综述以钾离子通道塔区的结构功能多样性为核心分类维度,系统梳理了不同类型钾离子通道塔区在蝎毒素结合中的构象差异,并重点阐述了hERG通道长塔区研究的争议点,为后续研究的创新点奠定基础。
现有研究根据钾离子通道的类型,分别揭示了不同通道塔区的构象与功能:电压门控钾通道Kv1.2的塔区在结合蝎毒素时呈开放构象,不影响毒素结合;钙激活钾通道SKCa3的塔区呈紧凑构象,选择性筛选结合的毒素;BKCa通道的塔区构象会随辅助亚基的结合发生转变,从而改变对毒素的敏感性。这些研究的优势在于利用特异性蝎毒素作为分子探针,能在接近生理状态下探究通道的构象与功能,避免了晶体结构解析的技术限制;但局限性在于部分研究依赖计算模拟,缺乏直接的实验验证,且对于hERG通道长塔区的研究存在结论冲突,半胱氨酸扫描突变可能因二硫键形成干扰通道功能与毒素结合,导致结果解读存在不确定性。
针对现有研究中hERG通道塔区作用的争议,以及半胱氨酸突变的潜在干扰,本研究采用新鉴定的特异性蝎毒素BmKKx2作为分子探针,通过丙氨酸扫描突变技术避免二硫键的影响,直接实验验证hERG通道塔区不同区域在毒素结合中的作用,首次明确hERG通道塔区在蝎毒素结合中呈开放构象,且仅起次要作用,解决了领域内的争议,为hERG通道的结构功能研究提供了新的实验依据。
3. 研究思路总结与详细解析
本研究的核心目标是探究hERG通道长塔区在蝎毒素结合中的构象状态与功能作用,核心科学问题为hERG通道塔区的构象是否参与蝎毒素结合,以及其在结合过程中的具体作用;技术路线遵循“分子探针鉴定→通道结合特性分析→突变体功能验证→构象结论推导”的闭环逻辑,通过丙氨酸扫描突变结合膜片钳技术,系统解析hERG通道塔区及孔道区的功能。
3.1 蝎毒素BmKKx2的表达与纯化
实验目的:获得高纯度的重组BmKKx2毒素,为后续hERG通道结合实验提供特异性分子探针。
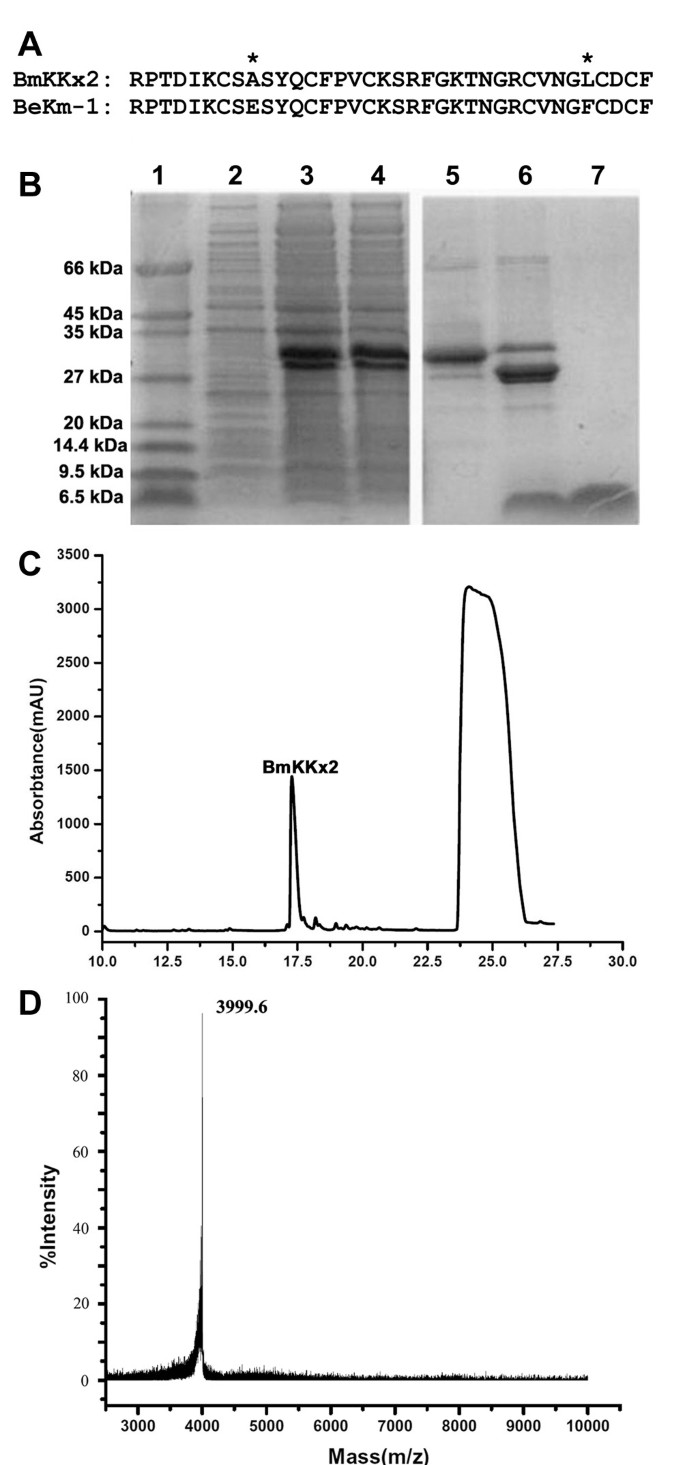
方法细节:从东亚钳蝎(Mesobuthus martensii)毒腺cDNA文库中克隆BmKKx2的全长编码序列,通过重叠PCR技术构建pGEX-6p-1-BmKKx2融合表达质粒,将质粒转化至大肠杆菌Rosetta (DE3)菌株中,经IPTG诱导表达谷胱甘肽S-转移酶(GST)-BmKKx2融合蛋白;采用谷胱甘肽亲和层析纯化融合蛋白,经肠激酶切割去除GST标签后,通过反相高效液相色谱(HPLC)分离纯化BmKKx2肽段;最后采用基质辅助激光解吸电离飞行时间质谱(MALDI-TOF-MS)验证重组毒素的分子量。
结果解读:SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE)结果显示,诱导表达的融合蛋白分子量约30 kDa,切割后得到26 kDa的GST和4.1 kDa的BmKKx2肽段;HPLC分离得到两个明显的洗脱峰,对应GST和BmKKx2;MALDI-TOF-MS检测到BmKKx2的分子量为3999.6,与理论分子量(考虑三对保守二硫键丢失6 Da后为4005.6 Da)高度一致,表明成功获得了结构正确的高纯度重组BmKKx2毒素。
产品关联:文献未提及具体实验产品,领域常规使用的试剂包括大肠杆菌表达菌株、GST亲和层析介质、肠激酶、HPLC系统、MALDI-TOF-MS质谱仪等。
3.2 BmKKx2对hERG通道的选择性与结合表面鉴定
实验目的:验证BmKKx2对hERG通道的特异性,并鉴定其与hERG通道结合的关键功能残基。
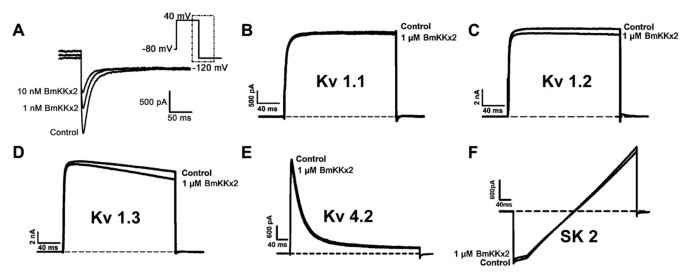
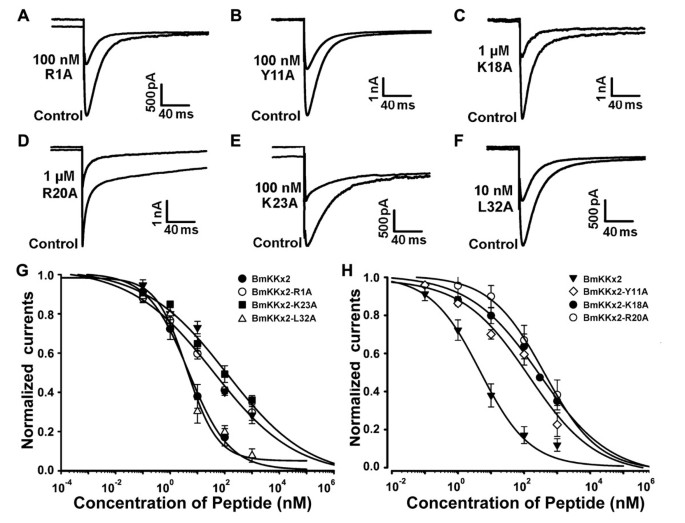
方法细节:将hERG通道质粒瞬时转染至人胚肾293(HEK293)细胞中,采用全细胞膜片钳技术检测不同浓度BmKKx2对hERG通道尾电流的抑制作用,通过Hill方程拟合计算半最大抑制浓度(IC₅₀);同时检测1 μM浓度的BmKKx2对Kv1.1、Kv1.2、Kv1.3、Kv4.2、SKCa2等其他类型钾离子通道的抑制作用;基于已知hERG抑制剂BeKm-1的功能表面,选择BmKKx2的6个候选残基(Arg1、Tyr11、Lys18、Arg20、Lys23、Leu32)进行丙氨酸定点突变,采用圆二色谱(CD)检测突变体的二级结构,通过膜片钳技术评估各突变体对hERG通道的结合亲和力。
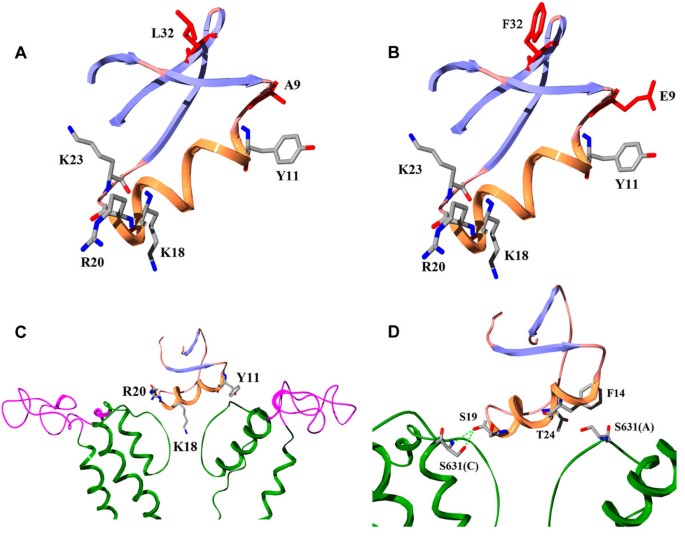
结果解读:BmKKx2对hERG通道的IC₅₀为6.7±1.7 nM,对其他检测的钾离子通道在1 μM浓度下几乎无抑制作用,表明其为hERG通道的高特异性阻滞剂;CD光谱显示所有突变体的二级结构与野生型BmKKx2无显著差异,说明定点突变未改变毒素的整体空间结构;突变体功能实验显示,K18A和R20A突变使毒素对hERG通道的亲和力分别下降56倍和61倍,Tyr11和Lys23突变使亲和力中度下降,Arg1和Leu32突变对亲和力影响较小,表明BmKKx2主要通过Tyr11、Lys18、Arg20、Lys23这四个残基与hERG通道结合,其功能表面与BeKm-1高度相似。
产品关联:文献未提及具体实验产品,领域常规使用的试剂包括HEK293细胞株、膜片钳放大器、CD光谱仪、定点突变试剂盒等。
3.3 hERG通道塔区不同区域在BmKKx2结合中的功能分析
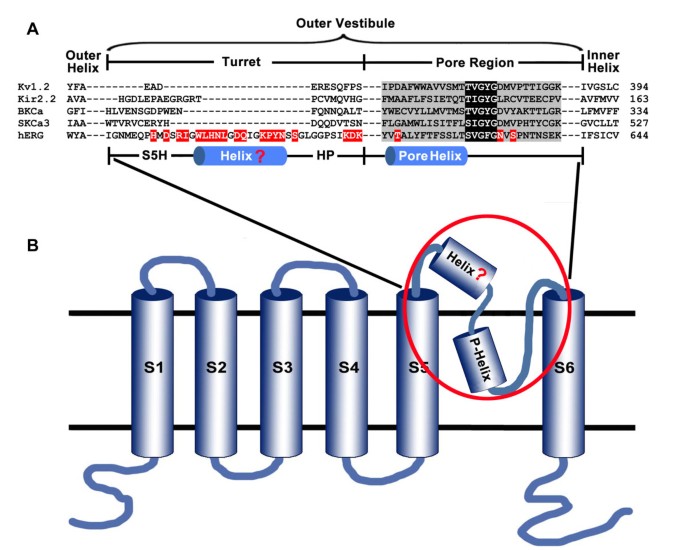
实验目的:探究hERG通道长塔区的三个亚区域(S5-螺旋连接区S5H、螺旋区、螺旋-孔道螺旋连接区HP)在毒素结合中的作用。
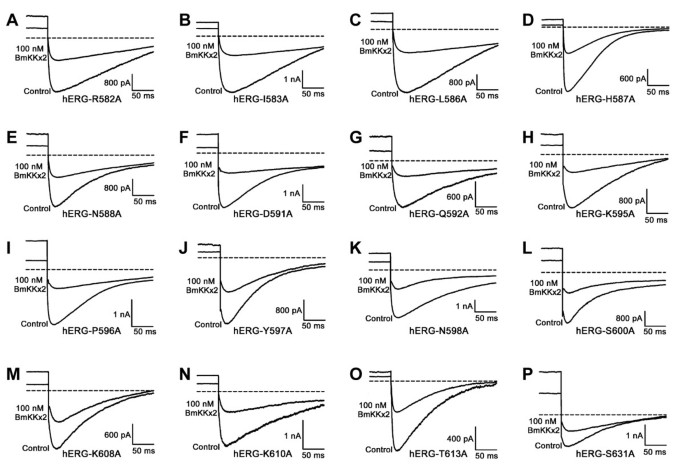
方法细节:基于hERG通道的结构模型,选择塔区的22个残基进行丙氨酸定点突变,构建突变体hERG通道质粒;将野生型和突变体质粒转染至HEK293细胞中,采用膜片钳技术检测各突变体通道的电流表达情况,对能正常表达电流的突变体,检测不同浓度BmKKx2对其电流的抑制作用,计算IC₅₀值并与野生型比较。
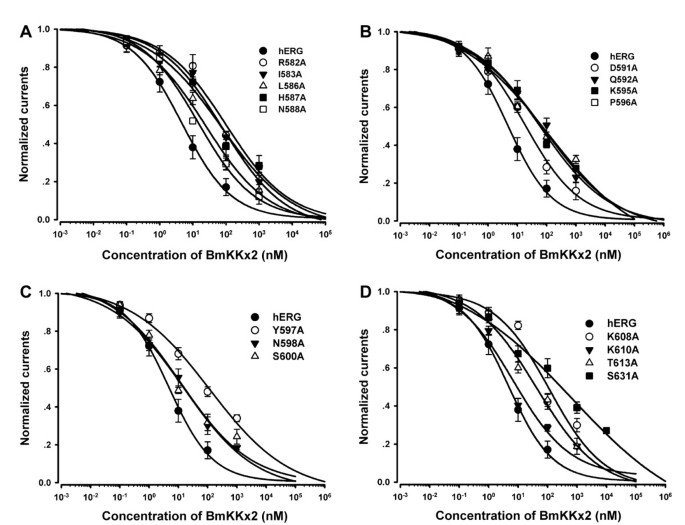
结果解读:S5H区域的R582A和I583A突变使BmKKx2的IC₅₀分别升至76.5 nM和87.5 nM,较野生型分别升高11.4倍和13.2倍;螺旋区的L586A、H587A、Q592A等突变使IC₅₀升高2-13倍;HP连接区的N598A、S600A、K608A等突变使IC₅₀升高2-17倍;所有塔区残基突变对毒素亲和力的下降幅度均不超过20倍,表明hERG通道塔区在毒素结合中仅起次要作用。
产品关联:文献未提及具体实验产品,领域常规使用的试剂包括细胞转染试剂、膜片钳系统等。
3.4 hERG通道孔道区在BmKKx2结合中的关键功能验证
实验目的:验证hERG通道孔道区在毒素结合中的保守且必需的作用。
方法细节:选择孔道区靠近选择性滤器的Ser631残基进行丙氨酸定点突变,构建hERG-S631A突变体质粒,转染至HEK293细胞中,采用膜片钳技术检测其对BmKKx2的敏感性。
结果解读:hERG-S631A突变使BmKKx2的IC₅₀升至698±64.4 nM,较野生型升高约104倍,表明孔道区的Ser631是BmKKx2结合hERG通道的关键残基,孔道区域在毒素结合中起保守且必需的作用。
产品关联:文献未提及具体实验产品,领域常规使用的试剂与上述细胞实验一致。
4. Biomarker研究及发现成果
本研究的核心发现为hERG通道塔区在蝎毒素结合中呈开放构象,以及孔道区Ser631为毒素结合的关键残基,这些发现丰富了钾离子通道塔区的结构功能多样性,为hERG通道相关药物研发提供了理论基础。
Biomarker定位:本研究中涉及的Biomarker为hERG通道的毒素结合关键残基,包括塔区的多个残基(如Q592、R582等)和孔道区的Ser631,筛选与验证逻辑为通过丙氨酸扫描突变结合全细胞膜片钳技术,评估每个残基突变对BmKKx2亲和力的影响,从而鉴定对毒素结合起关键作用的残基。
研究过程详述:这些关键残基来源于hERG通道的胞外功能区域(塔区和孔道区),验证方法为定点突变技术结合全细胞膜片钳电生理检测,通过测量不同浓度BmKKx2对野生型和突变体通道电流的抑制率,拟合得到IC₅₀值以反映毒素亲和力;特异性与敏感性数据显示,孔道区Ser631突变使毒素亲和力下降104倍,塔区Q592突变使亲和力下降13倍,其他塔区残基突变使亲和力下降2-17倍,表明孔道区残基对毒素结合的特异性远高于塔区残基。
核心成果提炼:本研究首次明确hERG通道的塔区在蝎毒素结合中呈开放构象,塔区在毒素结合中仅起次要作用,而孔道区的Ser631是毒素结合的核心必需残基;该发现解决了领域内关于hERG通道塔区构象与功能的争议,丰富了不同类型钾离子通道塔区的结构功能关系;实验数据中所有IC₅₀值均以均值±标准误表示,样本量未在单个实验中明确标注,但整体实验重复次数符合领域常规(推测n≥3),统计学差异通过IC₅₀的倍数变化体现,其中Ser631突变的亲和力下降幅度具有显著统计学意义(文献未明确提供P值,基于倍数变化推测P<0.001)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。