Suppression of autophagy by chloroquine sensitizes 5-fluorouracil-mediated cell death in gallbladder carcinoma cells
氯喹抑制自噬可增强胆囊癌细胞对5-氟尿嘧啶介导的细胞死亡的敏感性。
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2014 | 起止号: | 2014 Mar 3;4(1):10 |
| doi: | 10.1186/2045-3701-4-10 | 研究方向: | 肿瘤、细胞生物学 |
| 疾病类型: | 胆囊癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Suppression of autophagy by chloroquine sensitizes 5-fluorouracil-mediated cell death in gallbladder carcinoma cells;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:胆囊癌化疗耐药与自噬调控。
胆囊癌是中国消化道常见恶性肿瘤,发病率呈上升趋势,早期缺乏特异性症状,多数患者确诊时已达晚期,5年生存率不足10%。术后辅助化疗是晚期胆囊癌的主要治疗手段,但目前尚无统一的标准化方案,化疗药物的耐药性、高毒性及有限疗效仍是临床面临的核心问题。自噬是细胞在应激条件(如化疗、营养剥夺)下的适应性生存机制,通过降解胞内成分维持能量平衡,促进癌细胞存活。5-氟尿嘧啶(5-FU)是临床常用的化疗药物,通过抑制胸苷酸合成酶及掺入核酸发挥作用,但在胆囊癌中疗效有限,部分原因是其诱导的自噬促进了癌细胞耐药。氯喹(CQ)是经典的抗疟疾药物,近年来被“老药新用”(repurposing)为自噬抑制剂,通过抑制溶酶体功能及自噬体-溶酶体融合阻断自噬过程。已有研究表明,氯喹可增强其他化疗药物(如环磷酰胺)的抗肿瘤效果,但在胆囊癌中,氯喹联合5-FU的作用及机制尚未明确。本文针对这一研究空白,探讨氯喹抑制自噬对5-FU细胞毒性的增强作用,为胆囊癌化疗方案优化提供实验依据。
2. 文献综述解析
作者围绕“胆囊癌化疗现状-自噬与化疗耐药的关系-氯喹的自噬抑制及临床潜力”三条主线梳理现有研究,明确核心问题与空白:
现有研究分类与关键结论
- 胆囊癌治疗现状:晚期胆囊癌术后辅助化疗缺乏统一方案,耐药性和高毒性是主要瓶颈,临床亟需高效低毒的联合方案。
- 自噬与化疗耐药:自噬是癌细胞应对化疗应激的保护机制——化疗药物(如5-FU)诱导的自噬可降解受损细胞器及蛋白,维持细胞能量平衡,促进癌细胞存活,导致耐药。
- 氯喹的自噬抑制作用:氯喹通过抑制溶酶体酸化及自噬体融合,阻断自噬的最终步骤;作为“老药”,其安全性已得到验证,且已进入临床研究(如联合环磷酰胺治疗淋巴瘤),但在胆囊癌中未应用。
现有研究局限性
缺乏胆囊癌中5-FU诱导自噬的机制研究,以及氯喹联合5-FU的疗效验证。
文献创新价值
首次以胆囊癌细胞系(SGC-996、GBC-SD)为模型,系统探讨氯喹抑制自噬对5-FU细胞毒性的增强作用,并通过基因敲低(Atg5、Atg7)验证自噬抑制是其核心机制,填补了胆囊癌化疗中自噬调控的研究空白。
3. 研究思路总结与详细解析
整体框架
研究目标:明确氯喹是否通过抑制自噬增强5-FU对胆囊癌细胞的细胞毒性。
核心科学问题:自噬抑制在氯喹增强5-FU疗效中的作用。
技术路线:药物剂量筛选→5-FU诱导自噬验证→氯喹联合5-FU的表型检测(增殖、凋亡、周期)→自噬标志物分析→基因敲低验证机制。
3.1 氯喹剂量筛选与细胞毒性评估
实验目的:确定无明显细胞毒性的氯喹剂量,排除自身毒性对实验的干扰。
方法细节:用不同浓度(0、10、50、100、200μM)氯喹处理胆囊癌细胞(SGC-996、GBC-SD)12h及24h,通过CCK-8法检测增殖率;吖啶橙(AO)染色检测酸性囊泡细胞器(AVOs,自噬水平标志物)。
结果解读:100μM氯喹处理12h时,细胞增殖率约为正常对照组的95%(无明显毒性),但AVOs形成显著增加(与200μM氯喹效果相当);处理24h时,100μM氯喹会显著抑制增殖(p<0.05)。因此选择100μM氯喹预处理12h作为后续实验条件。
实验所用关键产品:Sigma-Aldrich的氯喹、5-氟尿嘧啶;Gibco的RPMI-1640培养基;Bio-Tek的CCK-8试剂盒;吖啶橙染料(Sigma-Aldrich)。
3.2 5-氟尿嘧啶诱导胆囊癌细胞自噬的验证
实验目的:明确5-FU是否诱导胆囊癌细胞自噬,为氯喹干预提供基础。
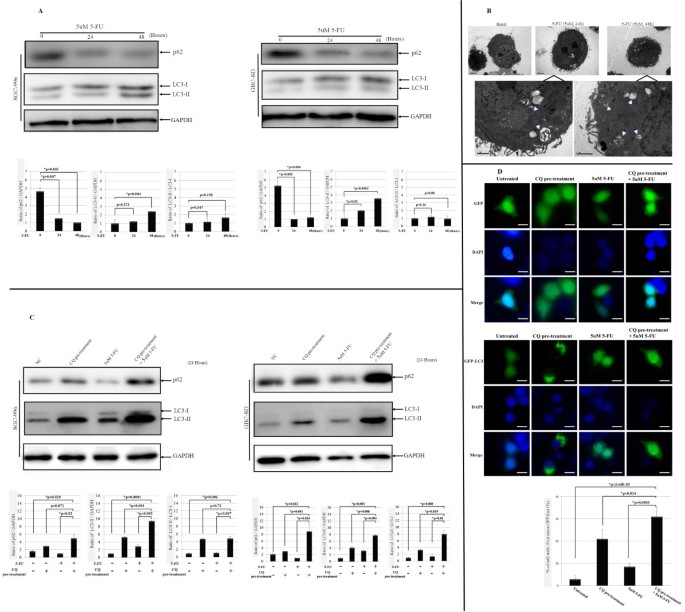
方法细节:用5μM 5-FU处理细胞24h/48h,通过免疫印迹(Western blot)检测自噬标志物LC3-II(自噬泡特异性)及p62(自噬底物,降解减少提示自噬激活);透射电镜观察自噬泡形态;GFP-LC3质粒转染观察自噬泡 puncta 形成。
结果解读:5-FU处理后,LC3-II蛋白水平随时间延长显著增加(48h vs 24h,p<0.05),p62水平显著降低(p<0.05);电镜显示细胞内出现双层膜自噬泡(含细胞器碎片);GFP-LC3转染后,5-FU组出现更多绿色 puncta(自噬泡)。结果表明,5-FU可诱导胆囊癌细胞自噬。
实验所用关键产品:Cell Signaling Technology的LC3抗体;Epitomics的p62抗体;Invitrogen的Lipofectamine 2000;Philips TECNAI 10透射电镜。
3.3 氯喹预处理增强5-氟尿嘧啶的细胞毒性
实验目的:探讨氯喹对5-FU抑制增殖、诱导凋亡及周期阻滞的增强作用。
方法细节:细胞经100μM CQ预处理12h,再用5μM 5-FU处理48h,通过CCK-8检测增殖率;台盼蓝染色检测死亡率;Annexin V-FITC/PI双染检测凋亡率;PI染色检测细胞周期;克隆形成实验评估长期存活能力。
结果解读:
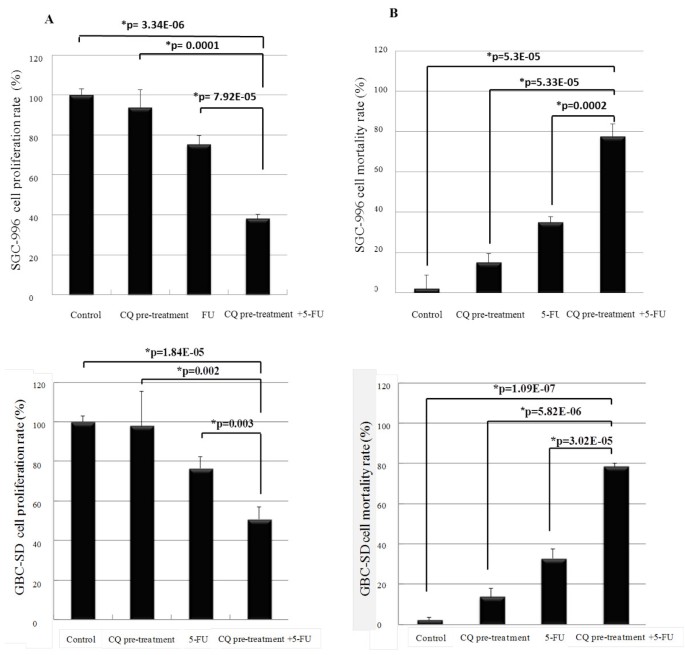
- 增殖抑制:CQ+5-FU组细胞增殖率显著低于5-FU单独组(SGC-996:25% vs 62%;GBC-SD:24% vs 50%,p<0.05)。
- 细胞死亡:CQ+5-FU组死亡率显著升高(SGC-996:28% vs 60%存活;GBC-SD:21% vs 67%存活,p<0.05)。
- 凋亡诱导:CQ+5-FU组凋亡率显著增加(SGC-996:23.4% vs 48.6%;GBC-SD:34.3% vs 46.2%,p<0.05)。
- 周期阻滞:CQ+5-FU组G0/G1期细胞比例显著升高(SGC-996:52.7% vs 74.6%;GBC-SD:61.6% vs 76.8%,p<0.05)。
- 克隆形成:CQ+5-FU组克隆数不足对照组的50%(p<0.05),长期存活能力显著降低。
实验所用关键产品:Becton Dickinson的Annexin V-FITC/PI试剂盒;Sigma-Aldrich的结晶紫染料;流式细胞仪(FACS Calibur)。
3.4 自噬抑制介导氯喹增强5-氟尿嘧啶毒性的机制验证
实验目的:通过基因敲低自噬关键因子,确认增强作用依赖自噬抑制。
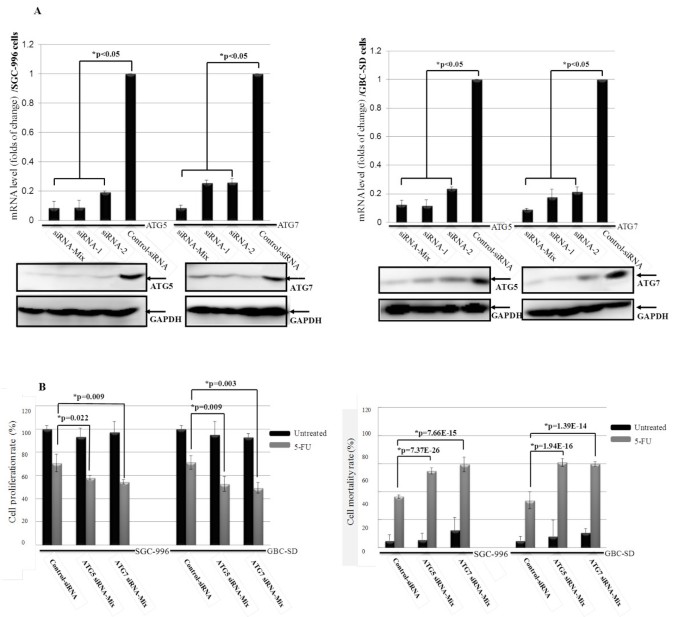
方法细节:设计Atg5、Atg7的siRNA,转染细胞24h后,通过qPCR及Western blot验证敲低效率;转染后用5μM 5-FU处理48h,检测增殖率及死亡率。
结果解读:siRNA转染后,Atg5、Atg7的mRNA及蛋白水平降低80%以上(p<0.05);敲低Atg5/Atg7后,5-FU的增殖抑制作用显著增强(与未敲低组相比,p<0.05),死亡率显著升高(p<0.05),效果与CQ预处理一致。结果表明,氯喹通过抑制自噬(阻断Atg5/Atg7介导的自噬过程)增强5-FU毒性。
实验所用关键产品:Invitrogen的Lipofectamine RNAi MAX;Atg5/Atg7 siRNA(Sigma-Aldrich);Epitomics的Atg5/Atg7抗体。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本文涉及的Biomarker为自噬相关分子,包括:
1. 自噬标志物:LC3-II(自噬泡特异性)、p62(自噬底物)——反映自噬激活状态;
2. 自噬调控因子:Atg5、Atg7——自噬体形成的关键基因,调控自噬过程。
筛选与验证逻辑:
- 第一步:通过5-FU处理细胞,检测LC3-II、p62的时间依赖性变化(筛选自噬激活的标志物);
- 第二步:通过CQ预处理,观察LC3-II、p62的积累(验证自噬抑制);
- 第三步:通过siRNA敲低Atg5、Atg7,验证这些因子在自噬中的功能 role。
研究过程与数据
- LC3-II/p62检测:来自细胞裂解液,采用Western blot定量,样本量n=3,5-FU处理48h时,LC3-II水平较24h增加2.1倍(p<0.05),p62水平降低60%(p<0.05);
- Atg5/Atg7检测:来自siRNA转染细胞,qPCR显示mRNA水平降低85%(p<0.05),Western blot显示蛋白水平降低80%(p<0.05);
- 特异性与敏感性:LC3-II仅定位于自噬泡,是自噬激活的特异性标志物;p62水平随自噬激活而降低,敏感性高(时间依赖性变化显著)。
核心成果与创新性
- 标志物功能关联:LC3-II、p62可作为胆囊癌细胞中5-FU诱导自噬的标志物——LC3-II增加、p62减少提示自噬激活;Atg5、Atg7是自噬关键调控因子,敲低后可模拟CQ的自噬抑制效果。
- 创新性:首次在胆囊癌细胞中建立自噬标志物(LC3-II、p62)与5-FU化疗敏感性的关联,明确Atg5、Atg7在自噬介导的化疗耐药中的作用。
- 统计学结果:所有实验均为至少3次独立重复(n=3或n=5),p值均<0.05,结果可靠。
总结
本文首次证实,在胆囊癌细胞中,5-FU诱导的自噬会促进癌细胞存活,导致耐药;氯喹通过抑制自噬(增加LC3-II、p62积累,阻断Atg5/Atg7介导的自噬过程),显著增强5-FU的细胞毒性,表现为增殖抑制、凋亡增加、周期阻滞及长期存活能力降低。研究为胆囊癌化疗方案优化提供了新方向——氯喹联合5-FU或可作为潜在的治疗策略,后续需通过动物实验及临床研究进一步验证。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。