Differential regulation of two histidine ammonia-lyase genes during Xenopus development implicates distinct functions during thyroid hormone-induced formation of adult stem cells
非洲爪蟾发育过程中两个组氨酸解氨酶基因的差异性调控表明,它们在甲状腺激素诱导的成体干细胞形成过程中具有不同的功能。
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2013 | 起止号: | 2013 Nov 13;3(1):43 |
| doi: | 10.1186/2045-3701-3-43 | 种属: | Xenopus |
| 研究方向: | 发育与干细胞、信号转导、细胞生物学、免疫/内分泌 | 细胞类型: | 干细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Differential regulation of two histidine ammonia-lyase genes during Xenopus development implicates distinct functions during thyroid hormone-induced formation of adult stem cells;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:发育生物学(爪蟾变态发育与成人肠道干细胞形成机制)。
成人器官特异性干细胞是维持器官稳态、修复组织损伤的核心,但这类干细胞在脊椎动物发育中的形成机制尚未完全阐明。哺乳动物肠道干细胞的研究表明,其更新依赖Wnt、Notch等信号通路调控的“干细胞龛”,但由于哺乳动物胚胎和新生期依赖母体,难以直接研究甲状腺激素(T3)对干细胞形成的调控——而T3是脊椎动物postembryonic发育的关键激素(如哺乳动物新生儿肠道成熟、两栖类变态发育)。爪蟾(如非洲爪蟾Xenopus laevis)的变态发育为解决这一问题提供了理想模型:该过程完全依赖T3,肠道重塑时幼虫单层上皮通过凋亡退化,少量幼虫上皮细胞去分化形成成人肠道干细胞,最终构建成与哺乳动物类似的“隐窝-绒毛”样结构(爪蟾为“槽-嵴”结构)。然而,哪些基因参与这一成人干细胞的“从头形成”过程仍不清楚。
组氨酸氨裂解酶(HAL)编码组氨酸代谢途径的第一个酶(组氨酸酶),催化L-组氨酸非氧化脱氨生成反式尿刊酸和氨。人类HAL缺乏会导致“组氨酸血症”(一种罕见的常染色体隐性代谢疾病),表现为血浆组氨酸、组胺升高,尿刊酸降低,患儿常伴随多动、语言障碍、发育迟缓等神经表型,但HAL在正常发育中的作用尚未被研究。因此,本研究聚焦于爪蟾发育过程中HAL基因的表达调控,旨在揭示其在T3诱导的成人肠道干细胞形成中的作用。
2. 文献综述解析
作者对现有研究的分类维度主要分为两部分:一是成人肠道干细胞形成的模型研究(哺乳动物模型的局限性与爪蟾模型的优势),二是HAL基因的功能研究(代谢作用与病理表型)。
现有研究的关键结论包括:①哺乳动物肠道干细胞的更新依赖干细胞龛的信号调控(如Wnt通路维持干细胞增殖、Notch通路调控分化),但难以研究T3对干细胞“形成”的调控(因胚胎依赖母体);②爪蟾变态发育的肠道重塑是研究成人干细胞形成的理想模型——T3可诱导幼虫上皮细胞去分化为成人干细胞前体,且该过程可通过体外实验操控;③HAL是组氨酸代谢的关键酶,其缺乏导致代谢紊乱,但HAL在发育中的具体功能未被探索。
现有研究的局限性:①哺乳动物模型无法直接解析T3调控的成人干细胞形成过程;②HAL基因在发育中的表达模式、调控机制及与干细胞的关系未知。
本研究的创新价值:首次发现爪蟾属(非洲爪蟾与热带爪蟾Xenopus tropicalis)中存在两个HAL基因(HAL1和HAL2),且二者在发育中呈“时空差异调控”——HAL2仅在变态高潮期的成人肠道干细胞中特异性表达,为HAL参与干细胞形成提供了直接证据,弥补了HAL在发育功能上的空白。
3. 研究思路总结与详细解析
本研究的整体框架:目标是阐明HAL基因在爪蟾肠道变态发育中的表达调控模式及其与成人干细胞的关系;核心科学问题是“爪蟾HAL基因是否重复?两个HAL基因的表达模式与T3调控的关系?HAL2是否定位于成人干细胞?”;技术路线为“序列分析→表达谱检测→T3调控实验→原位杂交定位”的闭环。
3.1 爪蟾HAL基因的序列分析与重复验证
实验目的:确认爪蟾属中HAL基因的重复情况及进化来源。
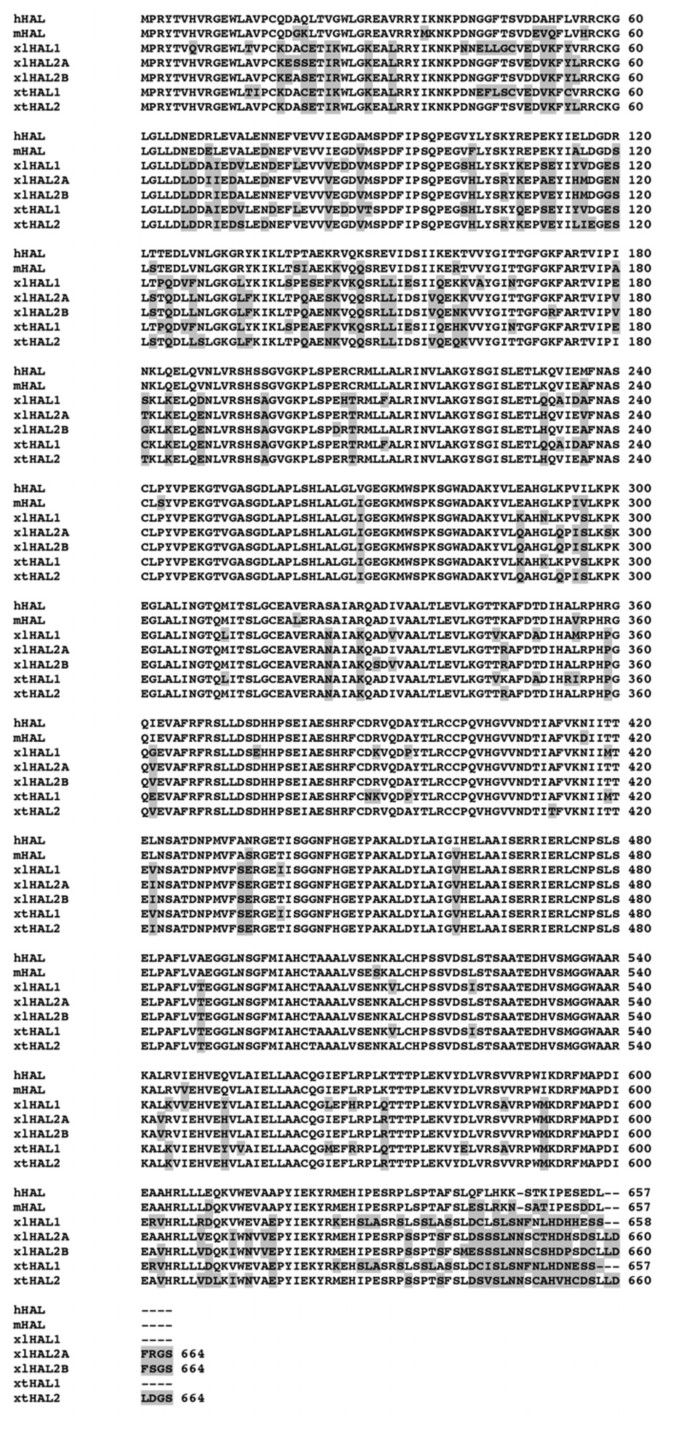
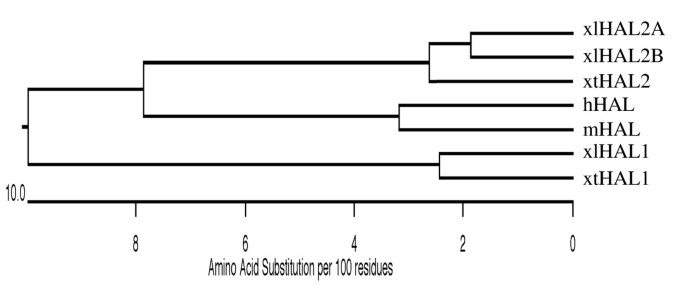
方法细节:检索GenBank数据库中非洲爪蟾(四倍体)和热带爪蟾(二倍体)的HAL基因序列,使用DNASTAR软件进行核苷酸/氨基酸序列比对,构建系统发育树分析进化关系。
结果解读:非洲爪蟾存在3个HAL序列(HAL1、HAL2A、HAL2B,其中HAL2A/B为HAL2的重复拷贝),热带爪蟾(二倍体)也存在2个HAL基因(HAL1、HAL2),说明HAL基因重复发生在两栖类与哺乳动物分化之后、非洲爪蟾与热带爪蟾分化之前;系统发育树显示,哺乳动物HAL更接近爪蟾HAL2,提示HAL1可能是两栖类特有的重复基因。
产品关联:序列分析使用DNASTAR软件,文献未提及具体实验试剂。
3.2 肠道变态发育中HAL基因的组织特异性表达分析
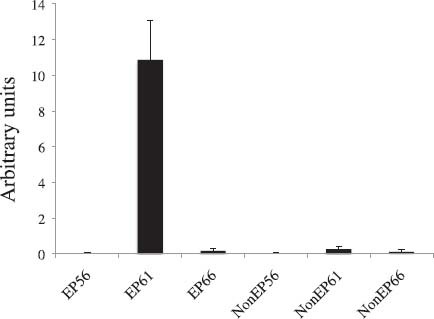
实验目的:检测HAL1/2在肠道不同组织(上皮Ep与非上皮non-Ep)及不同变态阶段的表达模式。
方法细节:分离非洲爪蟾预变态期(56期)、高潮期(61期)、变态后期(66期)的肠道上皮(Ep)和非上皮组织(non-Ep,主要为结缔组织),用TRIZOL试剂提取总RNA,通过基因特异性引物进行定量反转录聚合酶链反应(qRT-PCR,内参基因为EF-1α)。
结果解读:HAL2仅在高潮期(61期)的Ep中高表达,预变态和变态后期无表达,且在non-Ep中无检测信号;HAL1在所有阶段和组织中均无表达(RT-PCR未检测到信号)。
产品关联:RNA提取使用Invitrogen的TRIZOL试剂,qRT-PCR使用Applied Biosystems的SYBR® Green I染料和ABI Prism 7000系统,HAL2引物同时扩增HAL2A和HAL2B(序列:5′-AGCTGCTCACAGGTTGCTAGTT-3′/5′-AAGAGTCCAATGAAAAAGATGTA-3′)。
3.3 T3对HAL2表达的调控实验
实验目的:验证T3是否直接或间接调控HAL2的表达。
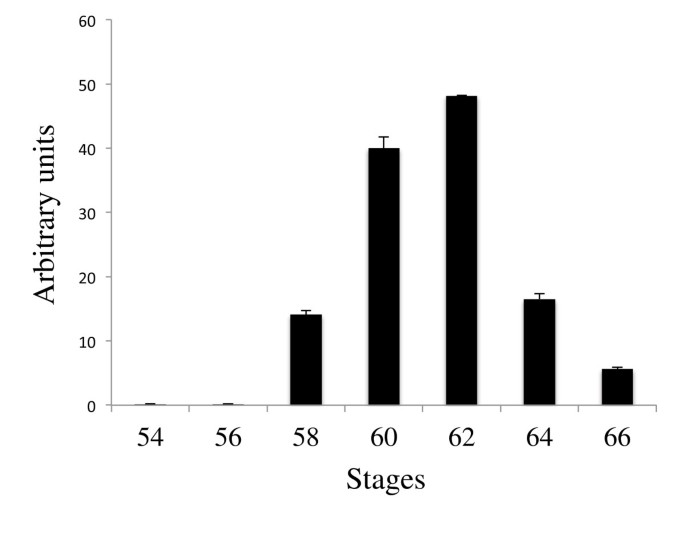
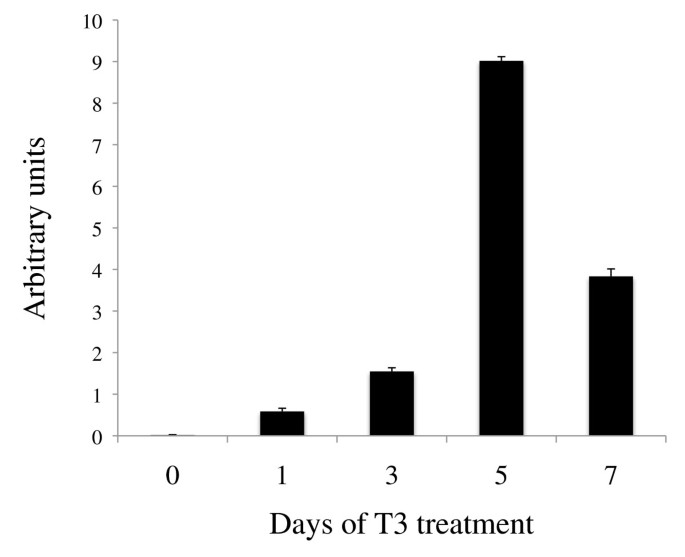
方法细节:用10 nM T3处理预变态期(54期)蝌蚪0-7天,提取肠道总RNA,qRT-PCR检测HAL2表达水平。
结果解读:T3处理1天即可诱导HAL2表达上调,5天达峰值(表达量较0天显著升高,文献未提供具体倍数,但趋势明显),之后维持高水平,说明HAL2的表达受T3调控。
产品关联:T3试剂未提及具体品牌,领域常规使用Sigma-Aldrich的L-甲状腺素(T3)。
3.4 HAL基因的原位杂交定位分析
实验目的:确定HAL2在肠道中的细胞定位,验证其是否与成人干细胞共定位。
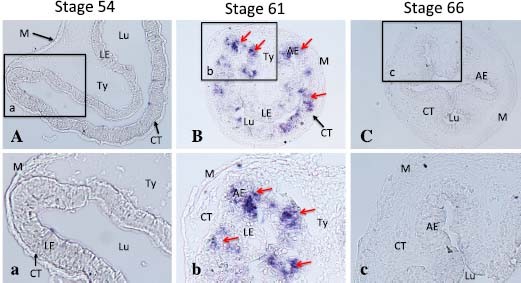
方法细节:设计HAL1/2的特异cRNA探针(669nt,同源性77%),用Roche的DIG RNA标记试剂盒合成探针;对不同变态阶段的肠道切片进行原位杂交,通过Olympus BX60显微镜观察信号分布。
结果解读:HAL2探针仅在高潮期(61期)肠道上皮的细胞簇中检测到强信号——这些细胞簇是已知的成人肠道干细胞(此时幼虫上皮细胞正在凋亡,仅干细胞存活);HAL1探针未检测到任何信号,与qRT-PCR结果一致。
产品关联:原位杂交使用Roche的DIG RNA Labeling Kit,切片观察使用Olympus BX60显微镜和QImaging Retiga Exi相机。
3.5 全动物发育中HAL基因的表达谱分析
实验目的:检测HAL1/2在全动物发育过程中的时空表达模式。
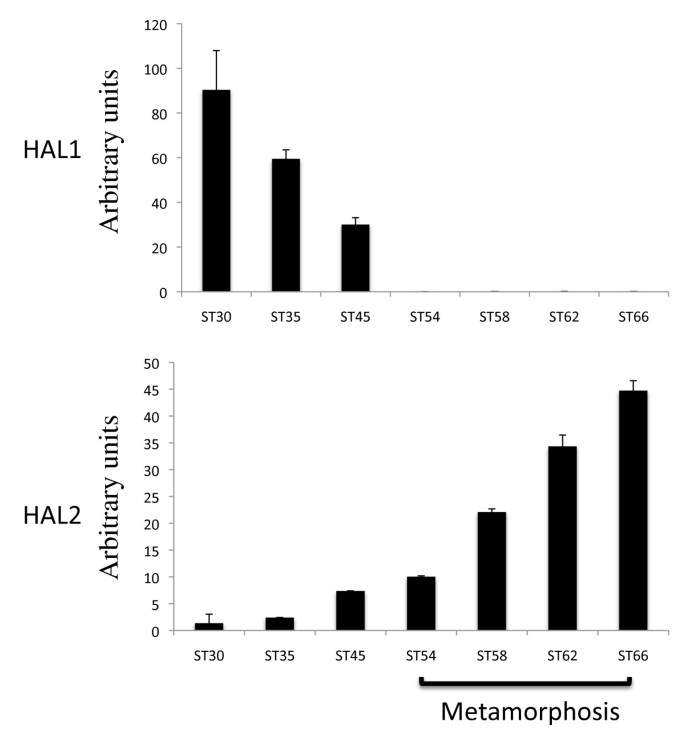
方法细节:提取非洲爪蟾胚胎期(30期)至变态后期(66期)的全动物总RNA,qRT-PCR检测HAL1/2表达水平。
结果解读:HAL1仅在胚胎期(30期)高表达,蝌蚪开始进食(45期)后表达受抑制;HAL2在胚胎期无表达,45期(进食开始)后表达上调,变态期达峰值,变态后期维持高表达。
产品关联:同3.2的qRT-PCR试剂。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究中的Biomarker为HAL2基因的mRNA表达,类型为“基因表达型生物标志物”。筛选/验证逻辑为:
1. 初筛:通过肠道组织特异性微阵列筛选到Ep中高表达的HAL基因;
2. 验证:qRT-PCR确认其在肠道高潮期Ep中的特异性表达;
3. 定位:原位杂交明确其定位于成人肠道干细胞簇。
研究过程详述
Biomarker来源:非洲爪蟾肠道上皮组织样本(不同变态阶段)。
验证方法:①qRT-PCR检测不同阶段/组织的表达水平(确认时空特异性);②原位杂交定位细胞类型(确认干细胞特异性)。
特异性数据:HAL2仅在变态高潮期(61期)的肠道上皮干细胞簇中表达,预变态/变态后期无表达,非上皮组织无信号;HAL1无表达。
敏感性数据:qRT-PCR可检测到T3处理1天后的HAL2上调(文献未提供ROC曲线或敏感性数值,但趋势显著)。
核心成果提炼
- 功能关联:HAL2是爪蟾肠道变态发育中成人干细胞的特异性标志物,其表达与干细胞的形成(去分化)和增殖阶段高度重合;
- 调控机制:HAL2的表达受T3调控(T3处理1天即上调),提示其可能是T3的直接靶基因(需后续启动子分析验证);
- 创新性:首次发现两栖类特有的HAL基因重复,且HAL2与成人干细胞的特异性关联,为研究HAL在干细胞代谢中的作用提供了新线索(如组氨酸代谢是否为干细胞增殖提供能量);
- 统计学结果:所有qRT-PCR实验重复2-3次,每次3-5只蝌蚪,结果一致(文献未提供具体P值,但表述为“显著上调”)。
本研究通过多层面实验揭示了HAL基因在爪蟾发育中的差异调控模式,为HAL2参与成人肠道干细胞形成提供了直接证据,也为理解组氨酸代谢在干细胞发育中的作用提供了新视角。后续研究可聚焦于HAL2的功能验证(如基因敲降后干细胞形成是否受影响)及T3调控的分子机制(如HAL2启动子的甲状腺激素反应元件分析)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。