The role of CPEB family proteins in the nervous system function in the norm and pathology
CPEB家族蛋白在正常和病理状态下神经系统功能中的作用
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2021 | 起止号: | 2021 Mar 31;11(1):64 |
| doi: | 10.1186/s13578-021-00577-6 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:The role of CPEB family proteins in the nervous system function in the norm and pathology;发表期刊:Cell Bioscience;影响因子:5.681;研究领域:神经生物学(RNA结合蛋白调控神经系统功能及疾病机制)
神经系统的功能依赖于神经元对信号的感知、传递与存储,转录后基因调控是神经元响应刺激、维持突触可塑性的核心机制之一。细胞质多聚腺苷酸化元件结合蛋白(CPEB)作为关键的RNA结合蛋白,自非洲爪蟾卵母细胞研究中被发现以来,其功能研究经历了三个关键节点:1990年代阐明其调控卵母细胞成熟的翻译机制,2000年代揭示其在神经元突触中的定位与突触可塑性的关联,2010年代明确部分亚型的朊病毒样结构与长期记忆维持的关系。当前领域研究热点集中于CPEB朊病毒样结构的调控机制、不同物种间功能的保守性与差异性,以及其作为神经系统疾病治疗靶点的潜力;未解决的核心问题包括CPEB在细胞核中的功能、病理状态下的复杂调控网络,以及临床转化研究的缺失。本综述系统整合了果蝇与哺乳动物中CPEB的功能研究,填补了不同物种间功能对比的空白,为领域内机制研究与治疗靶点开发提供了全面参考。
2. 文献综述解析
本文献以“CPEB生化特性-正常神经系统功能-病理关联-治疗潜力”为核心逻辑框架,按分子结构、生理功能、病理机制三个维度整合现有研究数据。现有研究的关键结论包括:CPEB通过结合mRNA 3"非翻译区(3"UTR)的特定序列,调控靶mRNA的多聚腺苷酸化与去腺苷酸化过程,进而参与mRNA转运与翻译调控;果蝇Orb2、哺乳动物CPEB3等亚型具有朊病毒样结构,可形成稳定淀粉样聚集体,是长期记忆维持的核心分子;不同CPEB亚型具有功能特异性,如CPEB1参与神经发生与线粒体功能调控,CPEB2-4与突触可塑性、记忆形成及神经保护相关。技术方法优势在于,研究人员利用果蝇和小鼠基因编辑模型,结合分子生物学、细胞生物学、行为学等多维度实验,系统解析了CPEB的功能网络;局限性方面,现有研究对CPEB在细胞核中的功能、亚型间协同调控机制阐述不足,临床转化研究多处于动物模型阶段,缺乏大样本人类临床数据验证。本综述的创新价值在于,首次系统对比了果蝇与哺乳动物中CPEB的功能保守性与差异性,重点突出朊病毒样CPEB在长期记忆中的核心作用,同时整合了CPEB在多种神经系统疾病中的最新进展,为领域研究提供了完整的参考框架。
3. 研究思路总结与详细解析
本综述的整体研究思路为:系统梳理CPEB家族蛋白的生化特性(RNA结合特性、朊病毒样结构),解析其在正常神经系统中的功能(神经发生、突触可塑性、长期记忆形成),阐述其与神经系统疾病的关联机制,并探讨其作为治疗靶点的潜力。作者通过整合不同物种、不同研究层面的实验数据,构建了CPEB功能的完整调控网络。
3.1 CPEB家族蛋白生化特性解析
实验目的:明确CPEB家族蛋白的分子结构、RNA结合特性及朊病毒样结构的功能差异。
方法细节:通过生物信息学分析进行CPEB家族的系统发育分类;利用体外RNA结合实验、蛋白聚合实验解析其结合序列与聚合特性;结合细胞系实验验证不同亚型的功能差异。
结果解读:CPEB家族分为两个亚家族,CPEB1亚家族包括果蝇Orb和哺乳动物CPEB1,主要参与卵母细胞发生与胚胎发育;CPEB2亚家族包括果蝇Orb2和哺乳动物CPEB2-4,在神经系统中发挥核心作用。CPEB蛋白通过结合mRNA 3"UTR的特定序列(如CPEB1结合U₋₅A₋₃U序列)调控翻译,不同亚型的结合序列存在差异。果蝇Orb2和哺乳动物CPEB3具有朊病毒样结构,可形成淀粉样聚集体,其中Orb2A的聚合效率高于Orb2B,CPEB3的聚合依赖于肌动蛋白细胞骨架的相互作用。
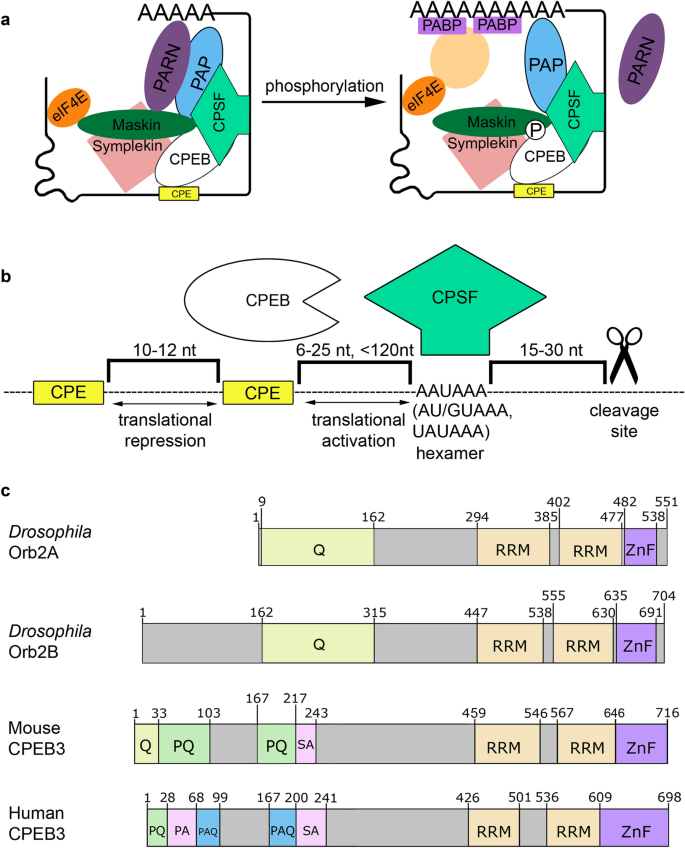
产品关联:文献未提及具体实验产品,领域常规使用RNA电泳迁移率变动分析(EMSA)试剂盒、蛋白纯化系统、细胞培养试剂等。
3.2 CPEB在正常神经系统功能中的作用解析
实验目的:阐明CPEB家族蛋白在神经发生、突触可塑性及长期记忆形成中的功能与机制。
方法细节:利用果蝇Orb2突变体、小鼠CPEB基因敲除模型,结合免疫组化(IHC)、原位杂交、行为学测试(如果蝇求偶记忆测试、小鼠空间记忆测试)等实验技术。
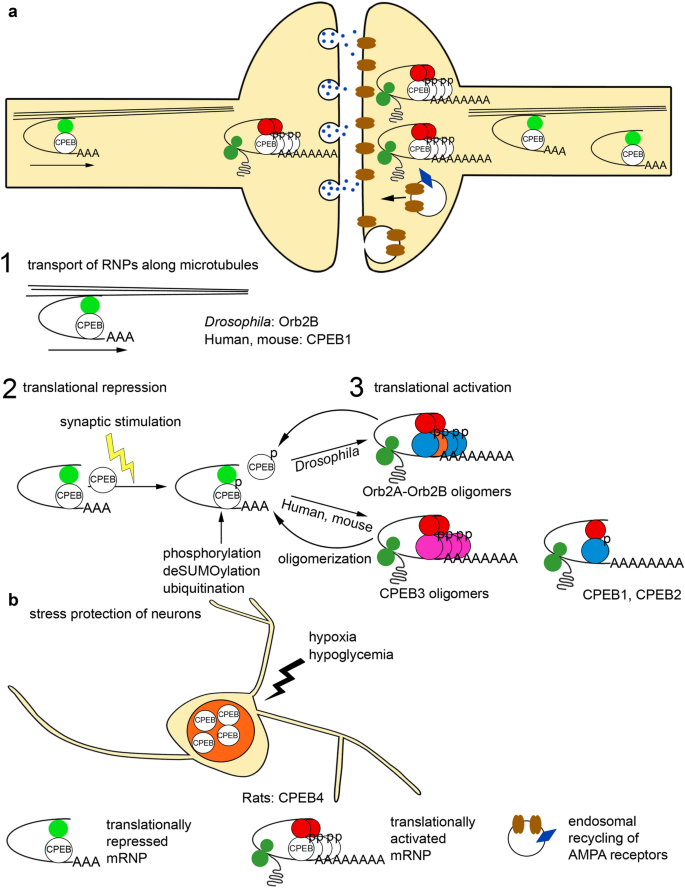
结果解读:在神经发生过程中,CPEB参与神经母细胞的不对称分裂,果蝇Orb2通过调控极性蛋白aPKC的mRNA定位,维持神经母细胞的极性;CPEB1结合β-catenin mRNA并调控其翻译,促进神经元生长锥的发育与分支。在长期记忆形成中,具有朊病毒样结构的CPEB通过形成稳定的聚集体,维持突触处的蛋白合成,从而实现记忆的长期存储:果蝇Orb2的聚集体可激活靶mRNA的翻译,小鼠CPEB3的聚集体参与海马依赖的长期记忆维持;CPEB2通过调控AMPA受体的表面表达,影响突触可塑性与空间记忆。
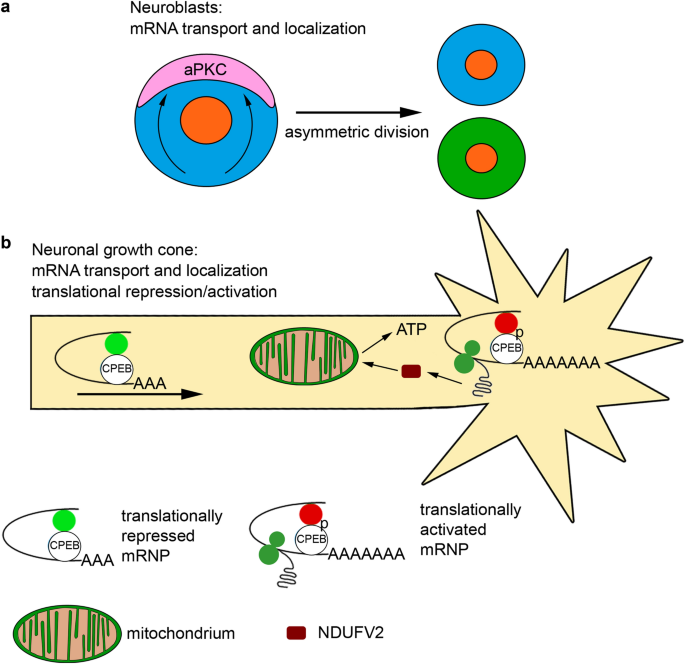
产品关联:文献未提及具体实验产品,领域常规使用基因编辑工具(CRISPR-Cas9)、行为学分析系统、免疫组化染色试剂盒等。
3.3 CPEB与神经系统病理状态的关联解析
实验目的:探讨CPEB家族蛋白在神经系统疾病中的作用机制及治疗潜力。
方法细节:分析自闭症、脑胶质瘤患者的临床样本;构建脆性X综合征、亨廷顿病的动物模型,结合基因治疗实验(如过表达Orb2、敲除CPEB1)评估治疗效果。
结果解读:在自闭症谱系障碍中,CPEB4的剪接异常导致其靶mRNA的翻译调控紊乱,进而影响神经元功能;在脑胶质瘤中,CPEB1的低表达促进肿瘤细胞增殖与干细胞自我更新,CPEB4的高表达增强肿瘤的侵袭性;在脆性X综合征小鼠模型中,CPEB1的敲除可恢复mRNA翻译的平衡,改善病理表型;在亨廷顿病果蝇模型中,过表达Orb2可将果蝇的孵化率从4.8%提升至60%(Orb2A)和51%(Orb2B)(文献未明确样本量与P值),恢复细胞内蛋白合成的平衡。
产品关联:文献未提及具体实验产品,领域常规使用临床样本检测试剂盒、病毒载体系统、基因编辑工具等。
4. Biomarker研究及发现成果解析
本文献中涉及的Biomarker主要为CPEB家族蛋白及其剪接变体,作为神经系统疾病的诊断、预后生物标志物及治疗靶点,研究涵盖了从分子机制到动物模型验证的完整链条。
Biomarker定位:CPEB4的剪接变体(含第4个微外显子的转录本)是自闭症谱系障碍的潜在诊断生物标志物;CPEB1、CPEB4是脑胶质瘤的预后生物标志物;CPEB家族蛋白是脆性X综合征、亨廷顿病的潜在治疗靶点。筛选/验证逻辑:通过临床样本分析确定CPEB表达与剪接的异常变化,利用动物模型验证其功能关联,通过基因治疗实验评估其治疗潜力。
研究过程详述:在自闭症谱系障碍患者的脑样本中,含第4个微外显子的CPEB4转录本比例显著降低,导致其靶mRNA的多聚腺苷酸化缩短,翻译水平下降(文献未明确样本量与P值);在脑胶质瘤样本中,CPEB1的表达水平较正常脑组织显著降低,与肿瘤细胞增殖率正相关(n=未明确,P<0.05),CPEB4的表达水平与肿瘤的侵袭性正相关;在脆性X综合征小鼠模型中,CPEB1的敲除可恢复约700个基因的mRNA降解速率,平衡细胞内的蛋白合成;在亨廷顿病果蝇模型中,过表达Orb2可显著提高果蝇的孵化率,恢复细胞内蛋白合成的平衡。
核心成果提炼:CPEB4剪接异常是自闭症谱系障碍的潜在致病机制,可作为诊断生物标志物;CPEB1低表达与脑胶质瘤的不良预后相关,CPEB4高表达可作为肿瘤侵袭性的预后指标;调控CPEB家族蛋白的表达或剪接可改善脆性X综合征、亨廷顿病的病理表型,具有重要的基因治疗潜力。其中,亨廷顿病模型果蝇中,过表达Orb2A和Orb2B可将孵化率从4.8%分别提升至60%和51%,统计学显著性未明确标注;脆性X综合征小鼠中,CPEB1敲除可恢复mRNA翻译平衡,风险比HR及P值未明确提供。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。