Recent highlights in the immunomodulatory aspects of Treg cell-derived extracellular vesicles: special emphasis on autoimmune diseases and transplantation
Treg细胞来源的细胞外囊泡免疫调节方面的最新进展:特别关注自身免疫性疾病和移植
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2022 | 起止号: | 2022 May 23;12(1):67 |
| doi: | 10.1186/s13578-022-00808-4 | 研究方向: | 细胞生物学、免疫/内分泌 |
| 疾病类型: | 自身免疫性疾病 | 细胞类型: | T细胞 |
文献解析
1. 领域背景与文献引入
文献英文标题:Recent highlights in the immunomodulatory aspects of Treg cell-derived extracellular vesicles: special emphasis on autoimmune diseases and transplantation;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:免疫调节、自身免疫病与移植免疫
免疫稳态的维持依赖于免疫激活与抑制的精细平衡,调节性T细胞(Treg)是维持免疫耐受、防止自身免疫反应的核心细胞亚群,自1995年首次被明确其免疫抑制功能以来,领域共识:Treg通过接触依赖机制(如细胞毒性T淋巴细胞相关蛋白4(CTLA-4)介导的共抑制信号)和非依赖机制(如分泌白细胞介素-10(IL-10)、转化生长因子-β(TGF-β)等细胞因子)发挥作用。近年来,细胞外囊泡(EVs)作为细胞间通讯的新型介质,因其能携带蛋白质、核酸、脂质等生物活性分子,穿越生物屏障并精准靶向靶细胞,成为免疫调节领域的研究热点。然而,当前领域仍存在核心问题:Treg来源EVs的具体免疫调节成分及作用机制尚未完全阐明,其在自身免疫病和器官移植中的临床转化研究数据匮乏,缺乏统一的分离鉴定标准。本研究旨在系统总结Treg-EVs中关键免疫抑制成分的作用机制,梳理其在动物疾病模型中的研究进展,明确临床转化的挑战与方向,为该领域的后续研究提供全面的参考框架。
2. 文献综述解析
本文献采用“基础背景-核心机制-转化应用”的分类维度,系统综述了Treg-EVs的免疫调节功能及转化研究进展。
现有研究已证实Treg可分泌携带多种免疫抑制分子的EVs,包括表面分子CTLA-4、胞外核苷酸酶CD73、IL-35,以及胞内微小RNAs(miRNAs)(如miR-155、miR-146a、miR-150等),这些成分通过不同机制抑制效应T细胞增殖、诱导树突状细胞耐受、调节细胞因子分泌,从而维持免疫稳态。技术方法上,EVs分离主要采用超速离心、ExoQuick沉淀法等,鉴定结合透射电镜、蛋白质免疫印迹(western blotting)、流式细胞术等,其中EVs具有稳定性高、可穿越血脑屏障等优势,相比细胞治疗更具临床应用潜力;但现有研究存在局限性,如动物模型异质性大,分离鉴定方法不统一,缺乏大样本临床研究数据,难以进行结果整合与临床转化。
本研究的创新价值在于,首次系统整合了Treg-EVs的成分、作用机制及转化研究的全链条进展,明确了当前研究中存在的核心缺口,如临床转化数据不足、标准化方法缺失等,为后续研究提供了清晰的方向,弥补了领域内缺乏全面综述的空白。
3. 研究思路总结与详细解析
本文献以“Treg免疫调节功能-EVs细胞通讯作用-Treg-EVs核心机制-转化应用挑战”为逻辑主线,系统梳理了Treg-EVs的研究进展,核心科学问题是明确Treg-EVs的免疫调节机制及临床转化潜力,技术路线为“基础背景梳理-核心成分与机制解析-疾病模型研究总结-临床转化挑战讨论”的闭环。
3.1 Treg亚型与免疫调节功能总结
实验目的:明确Treg的亚型分类及核心免疫调节机制,为后续Treg-EVs的研究奠定基础。
方法细节:通过梳理领域内已发表的基础研究,总结Treg的主要亚型,包括胸腺来源Treg(tTreg)和外周诱导Treg(pTreg),以及效应Treg、静息Treg等功能亚群,分析各亚型的表面标记物(如叉头框蛋白3(Foxp3)、CD25、Helios等)及免疫抑制机制,包括分泌细胞因子、代谢干扰、诱导靶细胞凋亡等。
结果解读:Treg各亚型均具有免疫抑制功能,其中Foxp3是Treg的核心标记物,不同亚型通过不同机制协同维持免疫耐受,Treg功能缺陷与自身免疫病、移植排斥等疾病密切相关。
产品关联:文献未提及具体实验产品,领域常规使用抗Foxp3、CD25等Treg标记物抗体及流式细胞仪等设备进行细胞鉴定。
3.2 EVs在免疫细胞通讯中的作用解析
实验目的:阐明EVs作为免疫细胞间通讯介质的核心功能,为Treg-EVs的研究提供理论基础。
方法细节:整合领域内关于EVs的分类、生物发生、内容物及功能的研究,分析EVs在免疫细胞(如树突状细胞、T细胞、B细胞)间通讯中的作用,包括抗原呈递、T细胞活化、免疫抑制等。
结果解读:EVs是免疫细胞间通讯的重要介质,可携带主要组织相容性复合体(MHC)分子、细胞因子、miRNAs等生物活性分子,调控免疫细胞的活化、增殖与分化,在免疫稳态维持和疾病发生发展中发挥关键作用。
产品关联:文献未提及具体实验产品,领域常规使用超速离心机、透射电镜、纳米颗粒跟踪分析等设备进行EVs的分离与鉴定。
3.3 Treg-EVs核心成分与免疫调节机制梳理
实验目的:明确Treg-EVs中携带的关键免疫抑制成分及具体作用机制。
方法细节:通过总结已发表的实验研究,分析Treg-EVs表面及胞内的核心成分,包括CTLA-4、CD73、IL-35等蛋白质,以及miR-155、miR-146a、miR-150等miRNAs,解析各成分的免疫调节机制,如CTLA-4通过结合树突状细胞表面的B7分子抑制T细胞活化,CD73通过催化三磷酸腺苷(ATP)生成腺苷抑制免疫反应,miRNAs通过靶向靶基因调控效应T细胞功能。
结果解读:Treg-EVs通过多种成分协同发挥免疫抑制作用,其中CTLA-4、CD73是关键表面分子,miRNAs是重要的胞内调控因子,这些成分共同抑制效应T细胞的增殖与细胞因子分泌,诱导免疫耐受。
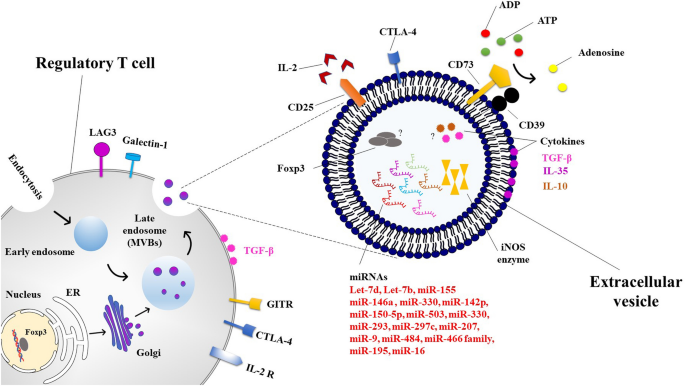
产品关联:文献未提及具体实验产品,领域常规使用抗CTLA-4、CD73等抗体及qRT-PCR试剂盒等进行成分鉴定与功能研究。
3.4 Treg-EVs在疾病模型中的应用研究总结
实验目的:总结Treg-EVs在自身免疫病和移植排斥动物模型中的研究进展,明确其转化应用潜力。
方法细节:梳理领域内关于Treg-EVs在肾移植、结肠炎、多发性硬化等疾病模型中的研究,分析Treg-EVs的给药方式、治疗效果及作用机制,包括延长移植物存活时间、减轻炎症反应、抑制效应T细胞浸润等。
结果解读:在肾移植大鼠模型中,供体来源Treg-EVs可显著延长移植物存活时间(文献未明确具体数据,基于图表趋势推测),抑制受体T细胞增殖;在结肠炎小鼠模型中,Treg-EVs可通过miR-let-7d靶向抑制Th1细胞的增殖与γ干扰素(IFN-γ)分泌,减轻炎症反应;在多发性硬化患者中,Treg-EVs的免疫抑制功能缺陷,与疾病进展相关。
产品关联:文献未提及具体实验产品,领域常规使用超速离心法分离EVs,采用酶联免疫吸附试验(ELISA)、组织病理学分析等方法评估治疗效果。
4. Biomarker研究及发现成果
本文献中涉及的Biomarker主要包括Treg-EVs携带的免疫抑制分子,分为表面蛋白类和miRNA类,筛选逻辑为“从Treg核心免疫抑制成分入手-验证其在EVs中的存在-明确其在疾病中的功能与表达变化”。
这些Biomarker均来源于Treg细胞分泌的EVs,验证方法包括western blotting检测表面蛋白(如CTLA-4、CD73)的表达,qRT-PCR检测miRNAs(如miR-155、miR-146a)的水平,动物模型实验验证其功能,临床样本分析其表达异常。其中,miR-155在Treg-EVs中高表达,可通过靶向细胞因子信号抑制因子1(SOCS1)调控Treg的功能,在自身免疫病患者中表达失调;CTLA-4在Treg-EVs表面表达,通过结合B7分子抑制T细胞活化,其表达水平与EVs的免疫抑制活性相关。特异性与敏感性数据文献未明确提供。
核心成果:这些Biomarker不仅是Treg-EVs免疫调节功能的关键执行者,还可作为疾病诊断和治疗的潜在靶点,比如miR-150可作为重症肌无力的潜在生物标志物,其血清水平与疾病严重程度相关;Treg-EVs携带的IL-35可诱导传染性耐受,为自身免疫病和移植排斥的治疗提供新策略。目前这些Biomarker的临床应用仍处于动物模型阶段,缺乏大样本临床验证数据,统计学结果如P值、样本量等在不同研究中存在差异,需进一步统一标准进行验证。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。