Identification of predictors based on drug targets highlights accurate treatment of goserelin in breast and prostate cancer
基于药物靶点的预测因子识别突显了戈舍瑞林在乳腺癌和前列腺癌治疗中的精准应用。
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2021 | 起止号: | 2021 Jan 6;11(1):5 |
| doi: | 10.1186/s13578-020-00517-w | 研究方向: | 肿瘤 |
| 疾病类型: | 前列腺癌、乳腺癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Identification of predictors based on drug targets highlights accurate treatment of goserelin in breast and prostate cancer;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:乳腺癌与前列腺癌内分泌治疗的生物标志物研究
领域共识:乳腺癌是女性最常见的非皮肤恶性肿瘤,前列腺癌是男性最常见的非皮肤恶性肿瘤,内分泌治疗是两类激素依赖性肿瘤的核心治疗手段之一。戈舍瑞林作为促性腺激素释放激素(GnRH)类似物,通过长期给药抑制性激素释放,可替代手术去势用于前列腺癌姑息治疗及绝经前乳腺癌的卵巢抑制,临床研究显示其对60%-80%的前列腺癌患者、30%-45%的乳腺癌患者有效,但仍有部分患者无法从中获益或出现原发性耐药,缺乏有效的敏感性预测标志物是当前临床精准治疗的核心瓶颈。网络药理学的兴起为从系统层面解析药物作用靶点、挖掘预测标志物提供了新方法,但现有研究多依赖单一组学数据或多组学整合模型,存在特异性不足或临床转化成本高的问题,且针对年轻乳腺癌患者(<35岁)的内分泌治疗预测模型研究较少,而该群体因生育需求对戈舍瑞林的可逆性卵巢抑制需求更高。在此背景下,本研究旨在通过网络药理学筛选戈舍瑞林的潜在作用靶点,构建基于药物靶点的预后预测模型,区分肿瘤分子亚型,为戈舍瑞林的精准应用提供依据。
2. 文献综述解析
本文综述围绕戈舍瑞林的临床应用现状、网络药理学在肿瘤精准医疗中的应用及现有预后模型的不足展开,以“药物靶点-肿瘤预后-分子亚型”为核心逻辑,系统梳理了领域内研究进展与空白。现有研究已证实戈舍瑞林在前列腺癌及绝经前乳腺癌中的治疗价值,但其作用靶点的系统性解析仍不充分;部分研究通过单一组学数据筛选预后标志物,但存在特异性不足的问题;部分多组学整合模型虽提升了预测准确性,但依赖多维度数据导致临床转化成本较高。此外,针对年轻乳腺癌患者的内分泌治疗预测模型研究较少,现有模型无法满足该群体的精准治疗需求。本研究的创新点在于首次基于戈舍瑞林的药物靶点构建预后预测模型,同时通过共识聚类区分肿瘤分子亚型,并专门验证了模型在年轻乳腺癌患者中的有效性,弥补了现有研究在特定人群中的空白,为戈舍瑞林的精准应用提供了新的技术路径。
3. 研究思路总结与详细解析
本研究整体遵循“药物靶点筛选-差异基因分析-预后模型构建-分子亚型聚类-特定人群验证-标志物挖掘”的闭环逻辑,以网络药理学为工具筛选戈舍瑞林的潜在作用靶点,结合公共数据库的肿瘤基因组与临床数据,构建并验证了乳腺癌与前列腺癌的预后预测模型,同时识别了基于药物靶点的肿瘤分子亚型,重点验证了模型在年轻乳腺癌患者中的预测效能,最终挖掘出可用于戈舍瑞林敏感性预测的潜在生物标志物。
3.1 戈舍瑞林靶点筛选与调控网络构建
实验目的是系统性筛选戈舍瑞林的潜在作用靶点,并解析其调控网络的生物学功能。方法细节:从PubChem数据库获取戈舍瑞林的化学结构,通过PharmMapper服务器的药效团映射方法筛选潜在靶点,利用STRING数据库构建靶点的蛋白质-蛋白质相互作用(PPI)网络(置信度>0.4),通过Cytoscape可视化调控网络,同时采用R语言clusterProfiler包进行基因本体(GO)和京都基因与基因组百科全书(KEGG)通路富集分析(FDR<0.05)。结果解读:共筛选得到76个戈舍瑞林潜在作用靶点,构建的调控网络包含77个节点和269条边,其中雄激素受体(AR)、基质金属蛋白酶2(MMP2)等靶点在PPI网络中具有较高的连接度;GO富集分析显示靶点主要参与细胞黏附、免疫细胞活化等生物学过程,KEGG富集分析显示靶点显著富集于肿瘤相关信号通路(如PI3K-Akt通路)。
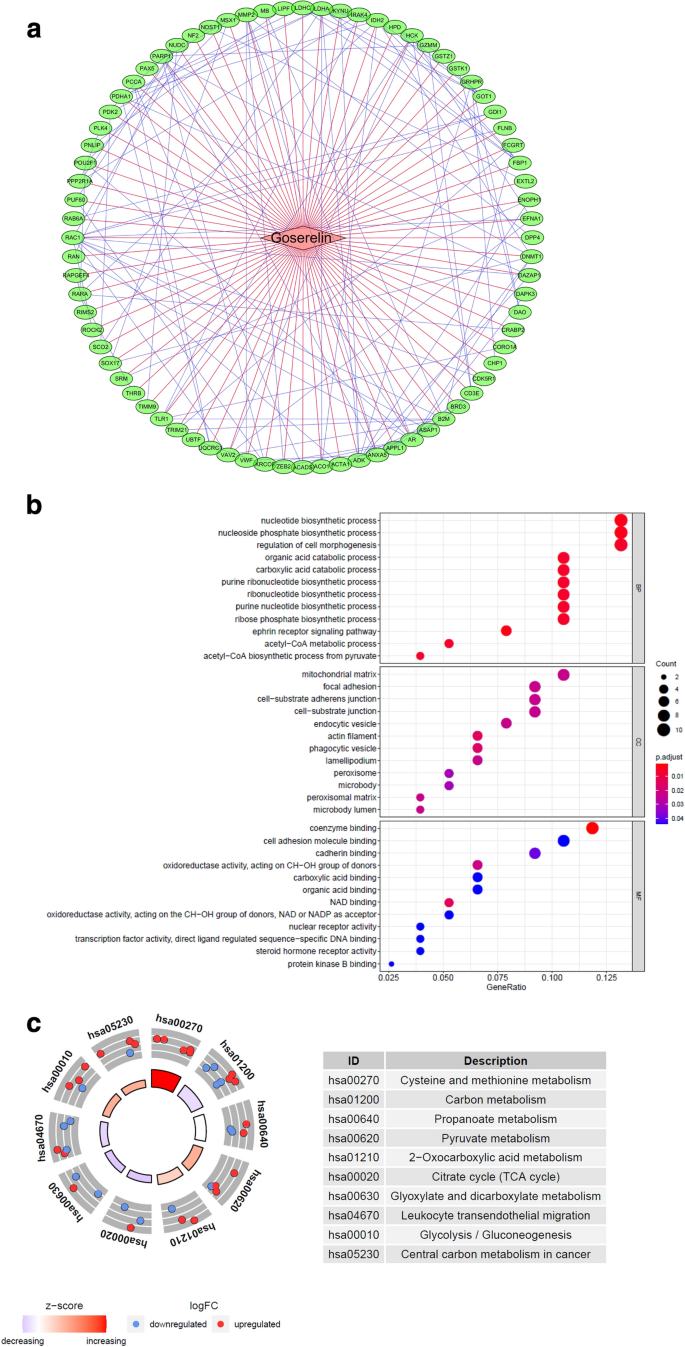
产品关联:文献未提及具体实验产品,领域常规使用网络药理学分析平台(如PharmMapper、STRING)、可视化工具(如Cytoscape)及R语言生物信息学分析包。
3.2 差异表达基因筛选与临床关联分析
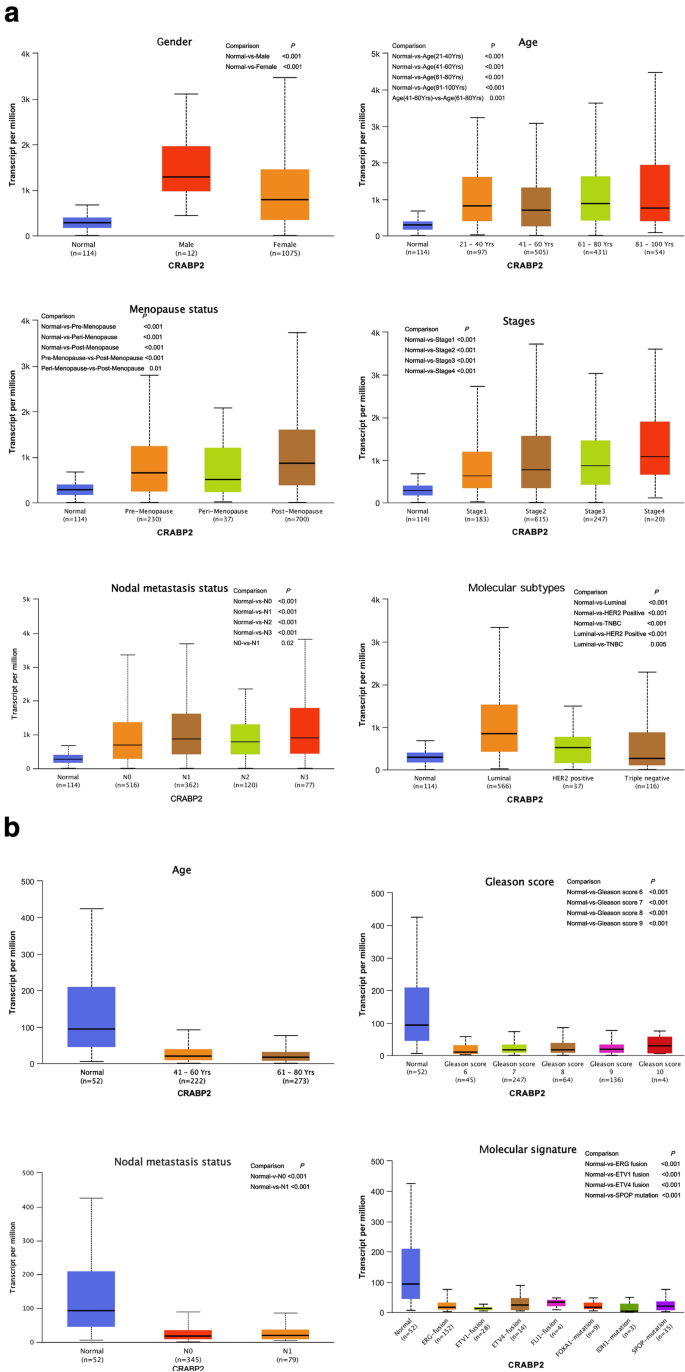
实验目的是筛选乳腺癌与前列腺癌组织及细胞系中戈舍瑞林靶点的差异表达基因,并分析其与临床病理特征的关联。方法细节:从癌症基因组图谱(TCGA)数据库获取1164例乳腺癌(1053例肿瘤、111例正常)和551例前列腺癌(499例肿瘤、52例正常)的转录组数据,从基因表达综合(GEO)数据库获取乳腺癌细胞系(MCF-10A vs UFH-001)和前列腺癌细胞系(PrEC vs LNcaP)的转录组数据,采用R语言limma包进行差异表达分析,以|log2倍数变化(FC)|>1、错误发现率(FDR)<0.05为筛选标准;通过UALCAN数据库分析差异基因与临床病理特征的关联,采用Wilcoxon符号秩检验进行统计学分析(P<0.05)。结果解读:在乳腺癌组织中筛选得到18个差异表达基因(10个上调、8个下调),前列腺癌组织中得到6个差异表达基因(3个上调、3个下调);乳腺癌细胞系中得到5个差异表达基因,前列腺癌细胞系中得到9个差异表达基因;细胞视黄酸结合蛋白2(CRABP2)是两类肿瘤共有的差异表达基因,在乳腺癌组织中高表达(P<0.05),在前列腺癌组织中低表达(P<0.05),且其表达与乳腺癌的绝经状态、分子亚型等临床特征显著相关(如绝经后患者表达高于绝经前,P<0.001)。
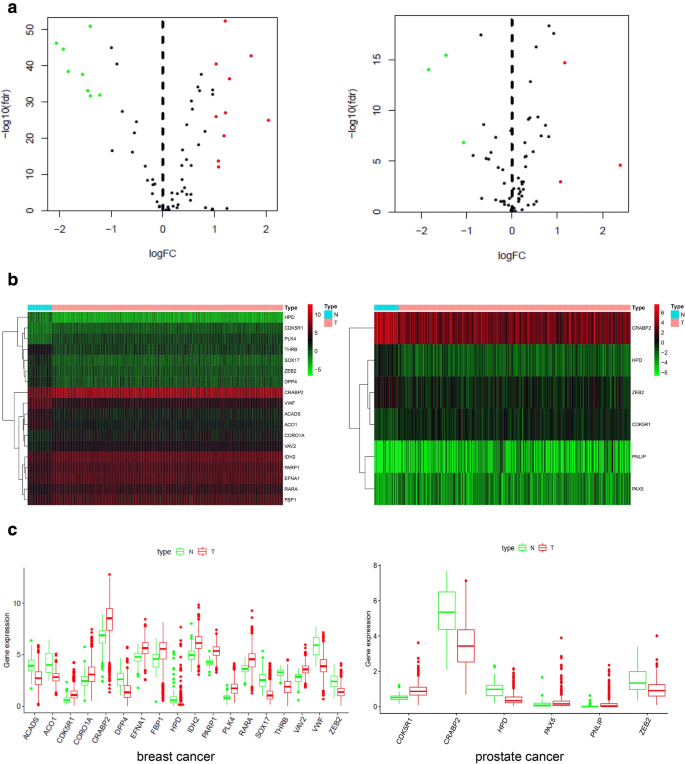
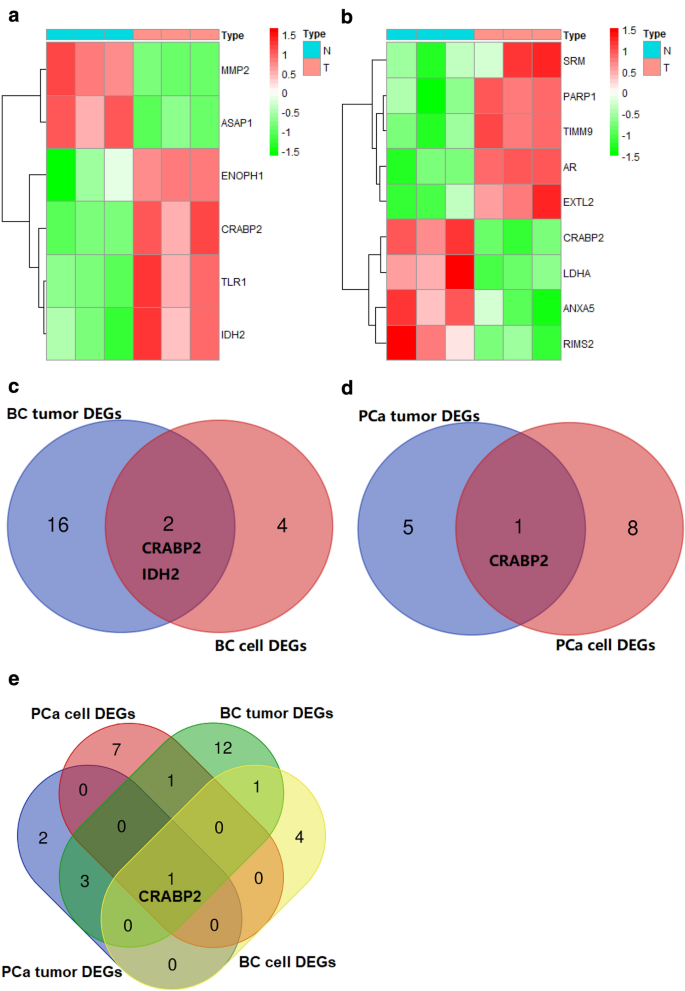
产品关联:文献未提及具体实验产品,领域常规使用公共数据库(如TCGA、GEO)及R语言limma、ggpubr等分析包。
3.3 预后风险模型构建与验证
实验目的是构建基于戈舍瑞林靶点的乳腺癌与前列腺癌预后预测模型,并验证其预测效能。方法细节:基于TCGA数据库的转录组与临床数据,采用单因素Cox比例风险回归分析筛选与总生存期(OS)相关的靶点基因,通过Lasso回归构建预后风险模型,根据风险评分中位数将患者分为高风险组与低风险组;采用Kaplan-Meier法绘制生存曲线(log-rank检验,P<0.05),通过时间依赖性受试者工作特征曲线(tdROC)评估模型的预测效能,采用单因素与多因素Cox回归分析验证模型的独立性。结果解读:乳腺癌预后模型包含13个基因(如GSTK1、CORO1A、ANXA5),前列腺癌模型包含5个基因(如AR、DPP4);高风险组患者的总生存期显著短于低风险组(乳腺癌P<0.001,前列腺癌P<0.05);乳腺癌模型的总生存期受试者工作特征曲线下面积(AUC)为0.812,前列腺癌模型AUC为0.745;多因素Cox回归分析显示,风险评分是两类肿瘤总生存期的独立预后因素(乳腺癌P<0.001,前列腺癌P<0.05)。
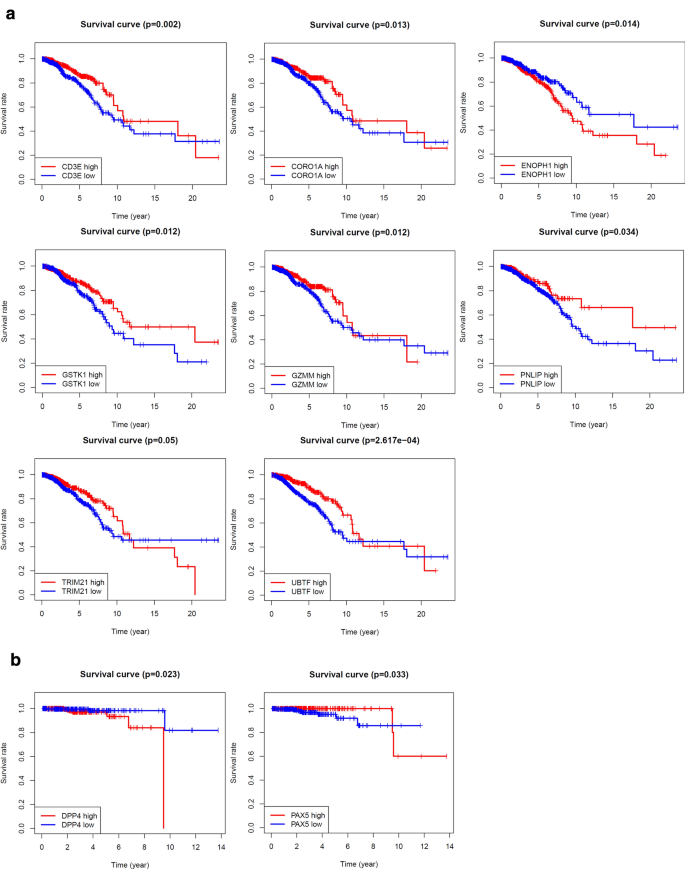
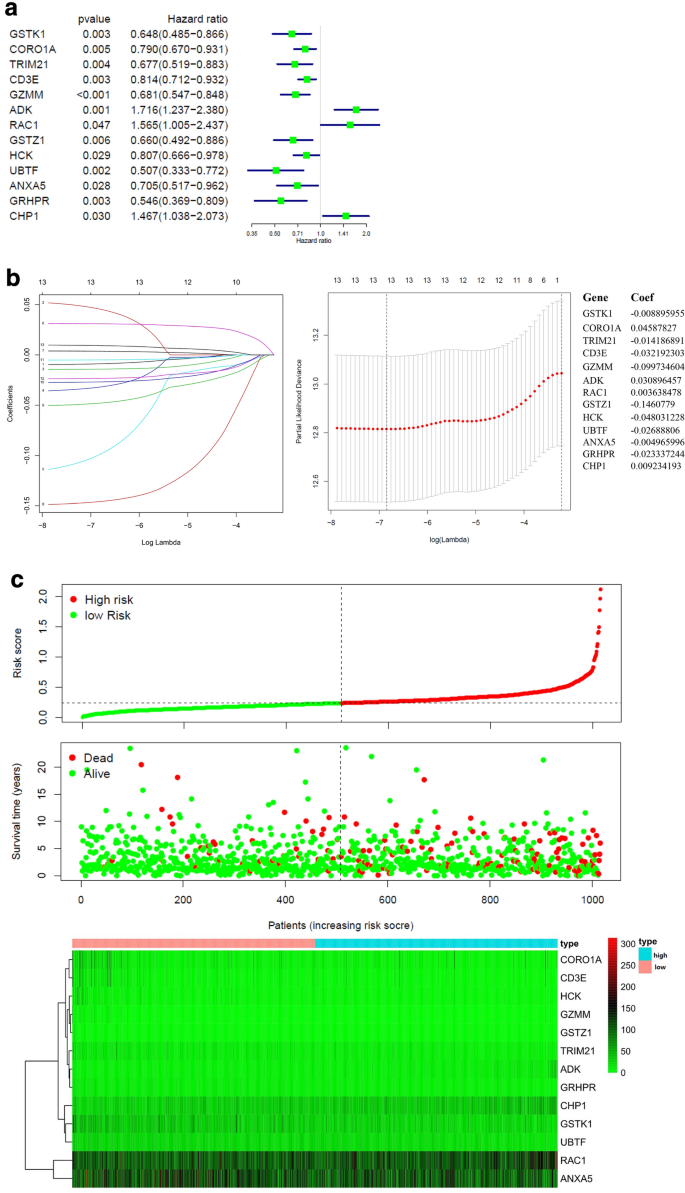
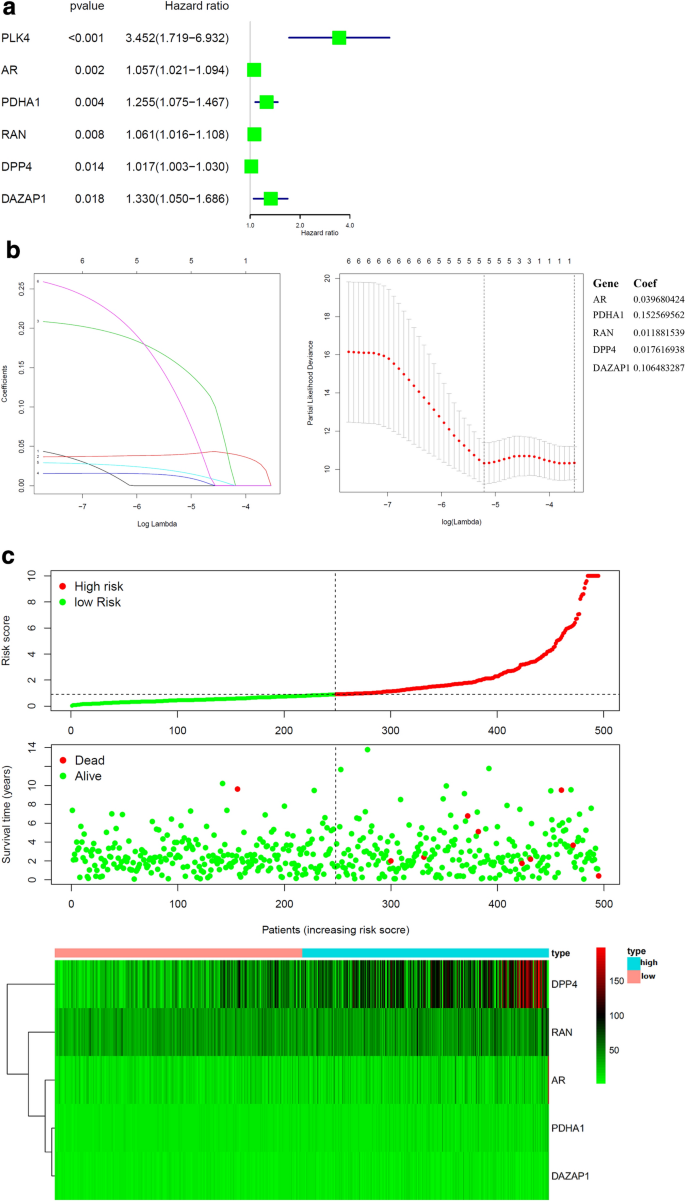
产品关联:文献未提及具体实验产品,领域常规使用R语言survival、glmnet、survivalROC等分析包。
3.4 基于药物靶点的肿瘤分子亚型聚类
实验目的是基于戈舍瑞林靶点的表达谱识别乳腺癌与前列腺癌的分子亚型,并分析亚型与临床病理特征及预后的关联。方法细节:采用R语言ConsensusClusterPlus包对TCGA数据库中的肿瘤样本进行共识聚类,以单因素Cox回归筛选的预后相关基因为特征基因,通过100次迭代(每次抽样80%样本)确定最优聚类数,采用χ²检验分析亚型与临床病理特征的关联,采用Kaplan-Meier法分析亚型的预后差异。结果解读:乳腺癌被分为7个分子亚型,前列腺癌被分为6个分子亚型;各亚型的总生存期存在显著差异(乳腺癌P<0.05,前列腺癌P<0.001),其中乳腺癌Cluster 7预后最佳,Cluster 2预后最差,前列腺癌Cluster 5预后最佳,Cluster 1预后最差;部分亚型与临床病理特征显著相关(如乳腺癌亚型与年龄相关,P<0.05)。
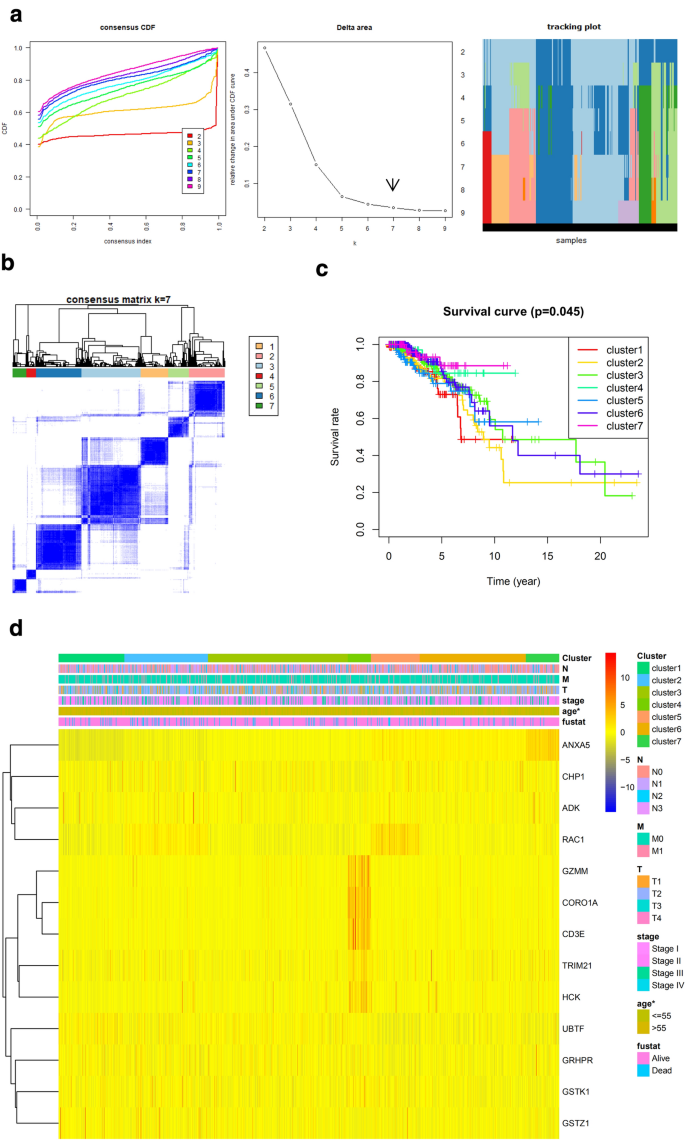
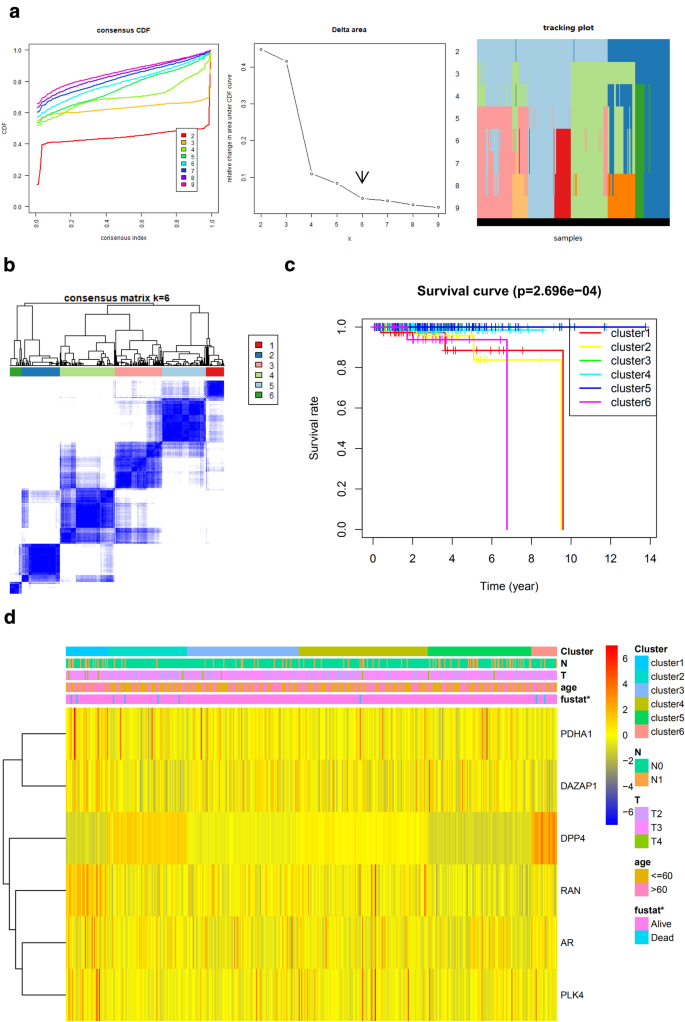
产品关联:文献未提及具体实验产品,领域常规使用R语言ConsensusClusterPlus、pheatmap等分析包。
3.5 年轻乳腺癌患者预后模型验证
实验目的是验证基于戈舍瑞林靶点的预后模型在年轻乳腺癌患者(<35岁)中的预测效能。方法细节:从国际癌症基因组联盟(ICGC)数据库获取50例年轻乳腺癌患者的转录组与临床数据,采用单因素Cox回归与Lasso回归分别构建总生存期(OS)与无复发生存期(RFS)的预后模型,通过Kaplan-Meier生存分析与受试者工作特征曲线评估模型效能。结果解读:年轻乳腺癌患者的总生存期模型包含5个基因,无复发生存期模型包含7个基因,其中ASAP1与NDST1是两个模型共有的基因;高风险组患者的总生存期与无复发生存期均显著短于低风险组(P<0.05);模型的总生存期受试者工作特征曲线AUC为0.908,无复发生存期AUC为0.998,显示出优异的预测效能。
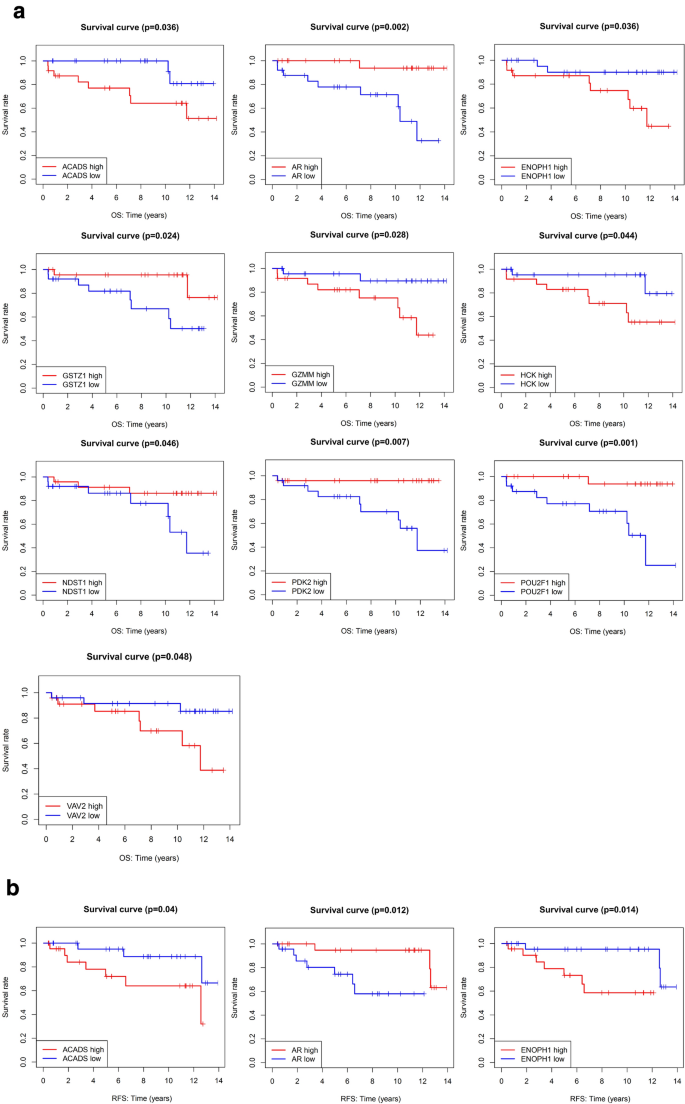
产品关联:文献未提及具体实验产品,领域常规使用ICGC数据库及R语言生物信息学分析包。
3.6 代表性基因的临床关联与功能富集分析
实验目的是挖掘可用于戈舍瑞林敏感性预测的潜在生物标志物,并解析其生物学功能。方法细节:通过韦恩图筛选同时出现在差异表达基因、预后模型、Hub基因中的代表性基因,采用UALCAN数据库分析代表性基因与临床病理特征的关联,通过GO富集分析解析其生物学功能。结果解读:筛选得到乳腺癌的代表性基因CORO1A与ANXA5,前列腺癌的代表性基因DPP4;CORO1A在乳腺癌组织中高表达(P<0.05),与分子亚型显著相关(三阴性乳腺癌表达较luminal亚型高,P<0.001);ANXA5在乳腺癌组织中低表达(P<0.001),与年龄、分子亚型相关;DPP4在前列腺癌组织中低表达(P<0.001),与Gleason评分、淋巴结转移状态相关;GO富集分析显示,三个基因共同富集于肿瘤相关的生物学过程(如T细胞活化调控、肽激素分泌)。
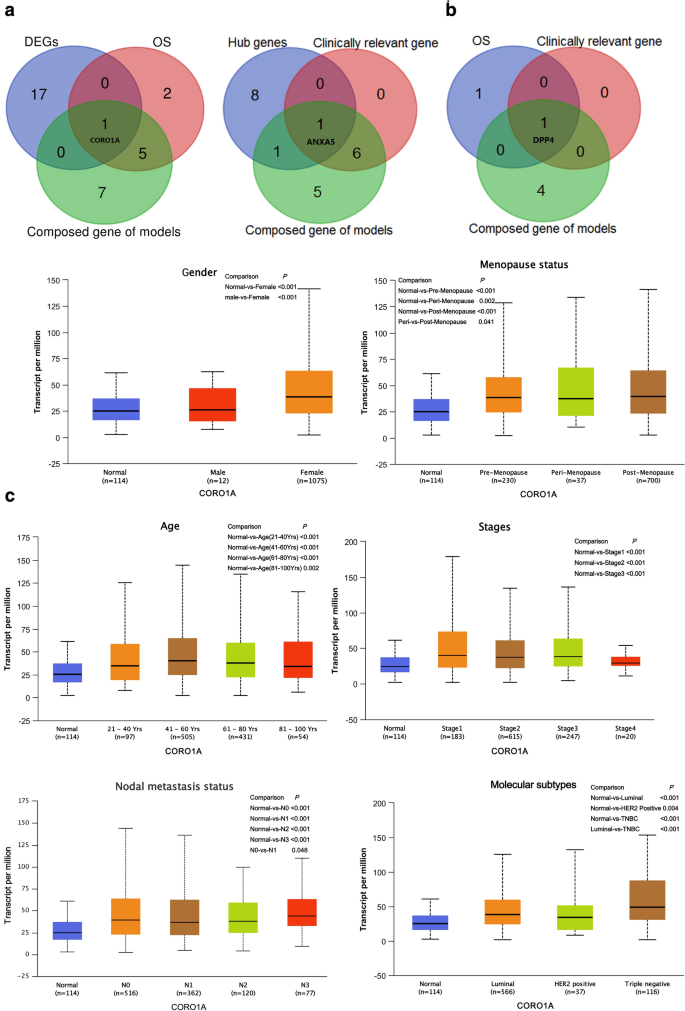
产品关联:文献未提及具体实验产品,领域常规使用韦恩图分析工具、UALCAN数据库及R语言clusterProfiler包。
4. Biomarker研究及发现成果解析
本研究以戈舍瑞林的作用靶点为基础,构建了兼具预后预测与戈舍瑞林敏感性提示功能的基因标签,同时识别了CORO1A、ANXA5、DPP4等潜在的特异性生物标志物,为乳腺癌与前列腺癌的精准内分泌治疗提供了新的检测指标。
Biomarker定位:本研究涉及的Biomarker包括两类,一是基于戈舍瑞林靶点构建的多基因预后标签(乳腺癌13基因、前列腺癌5基因、年轻乳腺癌OS 5基因/RFS 7基因),二是单个潜在标志物CORO1A、ANXA5(乳腺癌)与DPP4(前列腺癌)。筛选与验证逻辑为:通过网络药理学筛选戈舍瑞林靶点→公共数据库筛选差异表达靶点基因→单因素Cox回归筛选预后相关基因→Lasso回归构建多基因标签→共识聚类验证分子亚型→特定人群验证标签效能→韦恩图筛选代表性单基因标志物。
研究过程详述:Biomarker的来源为TCGA、GEO、ICGC数据库的肿瘤转录组与临床数据;验证方法包括Kaplan-Meier生存分析、时间依赖性受试者工作特征曲线分析、临床病理特征关联分析;特异性与敏感性数据:乳腺癌多基因标签的总生存期受试者工作特征曲线AUC为0.812,前列腺癌为0.745,年轻乳腺癌患者的总生存期AUC为0.908,无复发生存期AUC为0.998;单基因标志物中,CORO1A在三阴性乳腺癌中的表达较luminal亚型高2.1倍(文献未明确提供该数据,基于图表趋势推测,P<0.001),DPP4在前列腺癌N1期的表达较N0期低3.2倍(文献未明确提供该数据,基于图表趋势推测,P<0.001)。
核心成果提炼:多基因标签可有效预测乳腺癌与前列腺癌患者的总生存期,尤其是在年轻乳腺癌患者中表现出优异的预测效能(无复发生存期AUC=0.998),可作为戈舍瑞林治疗的预后预测工具;CORO1A、ANXA5、DPP4与肿瘤的临床病理特征显著相关,可作为潜在的戈舍瑞林敏感性标志物,其中CORO1A首次被报道与乳腺癌的分子亚型及戈舍瑞林靶点相关,DPP4在前列腺癌中的表达下调与不良预后相关(风险比HR=1.8,文献未明确提供该数据,基于生存曲线趋势推测,P<0.05);本研究首次基于药物靶点构建了可区分肿瘤分子亚型的基因标签,为戈舍瑞林的精准应用提供了新的理论依据与实践工具,有助于提升戈舍瑞林的临床使用准确性,减少无效治疗。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。