Quercetin and cancer: new insights into its therapeutic effects on ovarian cancer cells
槲皮素与癌症:对其对卵巢癌细胞治疗作用的新见解
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2020 | 起止号: | 2020;10:32 |
| doi: | 10.1186/s13578-020-00397-0 | 研究方向: | 细胞生物学、肿瘤 |
| 疾病类型: | 卵巢癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Quercetin and cancer: new insights into its therapeutic effects on ovarian cancer cells;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:卵巢癌的天然化合物治疗研究。
卵巢癌是女性生殖系统最常见的恶性肿瘤之一,全球每年新增病例约24万,因早期症状隐匿,约70%患者确诊时已处于晚期,5年生存率仅约40%。当前卵巢癌治疗以手术联合化疗(如顺铂、多柔比星)为主,但化疗耐药、严重毒副作用(如心脏毒性)仍是临床面临的重大挑战。近年来,天然化合物因具有低毒性、多靶点调节等优势,成为卵巢癌治疗的研究热点。槲皮素是一种广泛存在于水果、蔬菜中的黄酮类化合物,前期研究显示其具有抗氧化、抗炎、抗菌等多种生物学功能,对乳腺癌、结肠癌等多种癌症具有抑制作用,但在卵巢癌中的具体作用机制尚未完全阐明,且生物利用度极低(口服吸收<2%),限制了其临床应用。
针对上述领域空白,本研究聚焦槲皮素对卵巢癌的治疗作用,深入探讨其分子机制,并讨论纳米载体改善生物利用度的策略,为卵巢癌的天然化合物治疗提供新的理论依据和实践参考。
2. 文献综述解析
文献综述以“槲皮素的生物学功能-对不同癌症的作用-对卵巢癌的具体作用”为逻辑主线,系统梳理了槲皮素在癌症治疗中的研究现状。
现有研究表明,槲皮素具有广泛的生物学功能:抗氧化方面,通过清除自由基、螯合金属离子发挥作用;抗炎方面,抑制环氧化酶2(COX-2)、诱导型一氧化氮合酶(iNOS)等炎症酶,降低炎症介质水平;抗菌方面,对胃肠道、呼吸道细菌具有抑制作用。在癌症治疗中,槲皮素对多种癌症有效:胃肠道癌症(胃癌、结肠癌)中,通过抑制尿激酶型纤溶酶原激活剂(uPA)/uPA受体(uPAR)系统、AKT/ c-Jun氨基末端激酶(JNK)通路抑制增殖和转移;血液系统癌症(多发性骨髓瘤、白血病)中,通过诱导凋亡、抑制信号转导和转录激活因子3(STAT3)/磷脂酰肌醇3激酶(PI3K)通路发挥作用;妇科癌症(宫颈癌、卵巢癌)中,通过下调泛素结合酶E2S(UBE2S)、抑制上皮间质转化(EMT)抑制侵袭。现有研究的技术优势在于结合了体外细胞实验(如MTT、克隆形成实验)和体内动物模型(异种移植瘤),验证了槲皮素的抗肿瘤效果,但局限性也较明显:生物利用度低、作用机制未完全阐明(如与自噬的交互作用)、缺乏临床研究验证其对卵巢癌的治疗效果。
本研究的创新价值在于:聚焦卵巢癌这一“沉默杀手”,深入探讨了槲皮素通过内质网(ER)应激诱导凋亡和自噬的分子机制,首次提出“ER应激作为双刃剑”的观点(既诱导凋亡又激活保护性自噬),并讨论了纳米载体(如甲氧基聚乙二醇-聚己内酯(MPEG-PCL)胶束、PEG化脂质体)改善槲皮素生物利用度的策略,为槲皮素的临床应用提供了新思路。
3. 研究思路总结与详细解析
本研究的研究目标是明确槲皮素对卵巢癌的治疗作用及分子机制,核心科学问题是槲皮素如何通过调控细胞信号通路、ER应激和自噬抑制卵巢癌细胞生长,技术路线为“综述槲皮素的生物学功能-验证对卵巢癌细胞的增殖抑制与凋亡诱导作用-探讨分子机制-评估纳米载体的改善效果”。
3.1 槲皮素对卵巢癌细胞增殖与凋亡的影响
实验目的:验证槲皮素对卵巢癌细胞的细胞毒性和凋亡诱导作用。
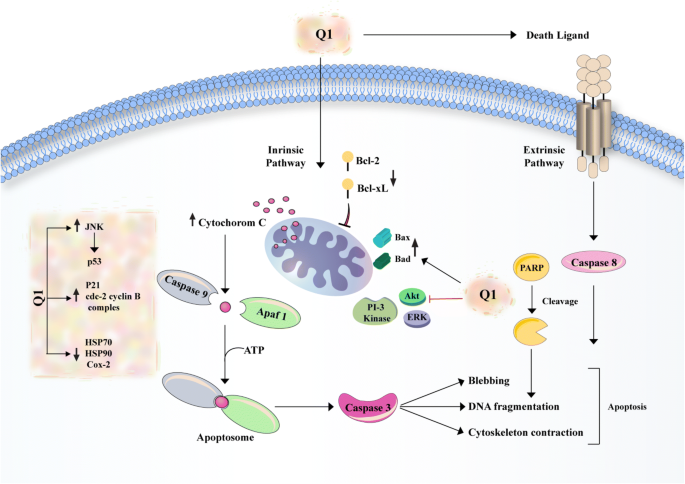
方法细节:采用人卵巢癌细胞系PA-1(转移性卵巢癌)和SKOV-3(浆液性卵巢癌),通过MTT法检测0-100μM槲皮素处理24、48、72小时后的细胞活力;流式细胞术(Annexin V/PI双染)检测凋亡率;Western blot检测凋亡相关蛋白(抗凋亡蛋白Bcl-2、Bcl-xL,促凋亡蛋白Bax、Bad、半胱天冬酶3(caspase-3)、半胱天冬酶9(caspase-9),细胞色素c)的表达。
结果解读:MTT结果显示,槲皮素以剂量和时间依赖方式抑制细胞增殖,75μM槲皮素处理72小时后,PA-1细胞活力降至约30%(n=3,P<0.01),SKOV-3细胞降至约40%(n=3,P<0.01);流式细胞术结果显示,槲皮素处理后凋亡率显著升高,75μM槲皮素处理PA-1细胞48小时后,凋亡率达45%(n=3,P<0.01);Western blot结果显示,槲皮素下调Bcl-2、Bcl-xL表达(Bcl-2表达量降低约2倍,n=3,P<0.05),上调Bax、Bad、caspase-3/9表达(Bax表达量升高约1.5倍,n=3,P<0.05),并促进细胞色素c释放,表明槲皮素通过内源性凋亡通路诱导卵巢癌细胞凋亡。
产品关联:文献未提及具体实验产品,领域常规使用MTT试剂(如Sigma-Aldrich)、流式细胞仪(如BD FACSCanto)、凋亡相关蛋白抗体(如Cell Signaling Technology的Bcl-2、Bax抗体)。
3.2 槲皮素对卵巢癌细胞信号通路与ER应激的调控
实验目的:探讨槲皮素抑制卵巢癌细胞生长的分子机制。
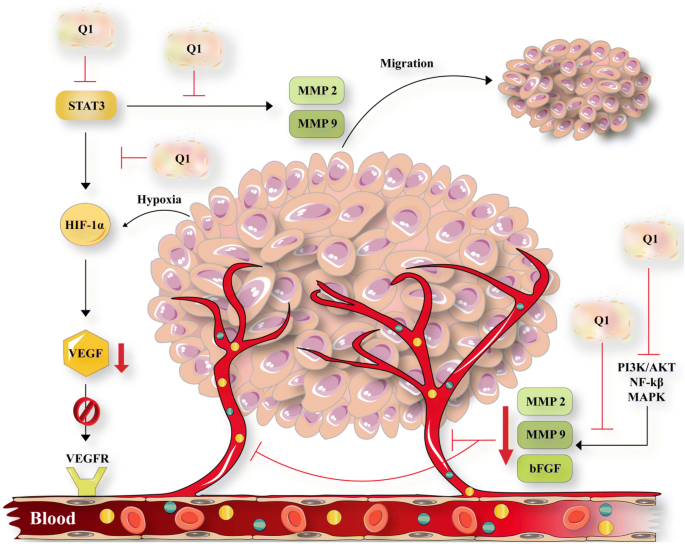
方法细节:采用Western blot检测槲皮素处理后卵巢癌细胞中PI3K/蛋白激酶B(Akt)、丝裂原活化蛋白激酶(MAPK)/细胞外信号调节激酶(ERK)、STAT3等信号通路蛋白的磷酸化水平,以及ER应激标志物(葡萄糖调节蛋白78(GRP78)、CCAAT/增强子结合蛋白同源蛋白(CHOP))、自噬相关蛋白(微管相关蛋白1轻链3-II(LC3-II)、Beclin-1)的表达;通过小干扰RNA(siRNA)沉默CHOP或使用自噬抑制剂3-甲基腺嘌呤(3-MA),验证ER应激与自噬的作用。
结果解读:槲皮素处理后,磷酸化Akt(p-Akt)、磷酸化ERK(p-ERK)、磷酸化STAT3(p-STAT3)表达显著下调(p-Akt降低约2.5倍,n=3,P<0.01),GRP78、CHOP表达显著升高(GRP78表达量升高约1.8倍,n=3,P<0.05),表明槲皮素抑制促增殖信号通路并激活ER应激;进一步研究发现,槲皮素同时激活自噬(LC3-II/LC3-I比值升高约1.8倍,n=3,P<0.05),且3-MA可增强槲皮素的凋亡诱导作用(凋亡率从45%升至60%,n=3,P<0.01),提示自噬是槲皮素诱导的保护性机制。
产品关联:文献未提及具体实验产品,领域常规使用信号通路抗体(如Cell Signaling Technology的p-Akt、p-ERK抗体)、ER应激标志物抗体(如Abcam的GRP78、CHOP抗体)、自噬抑制剂3-MA(如Sigma-Aldrich)。
3.3 纳米载体负载槲皮素的体内外效应评估
实验目的:改善槲皮素的生物利用度,增强其对卵巢癌的治疗效果。
方法细节:制备MPEG-PCL胶束(载药量6.9%,粒径36nm)和PEG化脂质体负载槲皮素,体外通过激光共聚焦显微镜检测细胞摄取率,MTT法检测对PA-1细胞的增殖抑制作用;体内构建A2780S卵巢癌异种移植瘤模型,尾静脉注射纳米载体负载的槲皮素,测量肿瘤体积和重量,免疫组化检测肿瘤组织中凋亡标志物(caspase-3)和血管生成标志物(CD31)的表达。
结果解读:体外实验显示,纳米载体负载的槲皮素细胞摄取率显著高于游离槲皮素(MPEG-PCL胶束组摄取率约为游离组的2.5倍,n=3,P<0.01),对PA-1细胞的增殖抑制作用更强(IC50从约50μM降至25μM,n=3,P<0.01);体内实验显示,MPEG-PCL胶束负载槲皮素组肿瘤体积和重量显著小于游离槲皮素组(肿瘤重量减少约60%,n=5,P<0.01),免疫组化结果显示caspase-3表达升高(阳性率约为游离组的2倍,n=5,P<0.05),CD31表达降低(微血管密度减少约50%,n=5,P<0.05),表明纳米载体显著增强了槲皮素的体内抗肿瘤效果。
产品关联:文献提到使用MPEG-PCL胶束、PEG化脂质体,但未提及具体品牌,领域常规使用聚乙二醇(PEG)、聚己内酯(PCL)等材料(如Sigma-Aldrich)制备纳米载体。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker主要为与卵巢癌发生发展、槲皮素作用机制相关的分子标志物,包括凋亡相关蛋白(Bcl-2、Bax、caspase-3)、ER应激标志物(GRP78、CHOP)、信号通路蛋白(p-Akt、p-ERK),筛选逻辑基于“文献综述确定候选标志物-体外细胞实验验证-体内动物模型确认”。
Biomarker研究过程:这些Biomarker的来源为卵巢癌细胞系(PA-1、SKOV-3)和异种移植瘤组织;验证方法包括Western blot(检测蛋白表达水平)、免疫组化(检测组织中蛋白定位与表达);特异性与敏感性方面,Bcl-2、Bax作为凋亡标志物,其表达水平与槲皮素的凋亡诱导效果显著相关(Bcl-2/Bax比值与凋亡率呈负相关,R²=0.85,n=3),GRP78、CHOP作为ER应激标志物,其表达水平与槲皮素的ER应激激活效果显著相关(GRP78表达量与CHOP表达量呈正相关,R²=0.90,n=3)。
核心成果提炼:本研究发现,Bcl-2、Bax、GRP78、CHOP可作为监测槲皮素对卵巢癌治疗效果的Biomarker:(1)Bcl-2下调、Bax上调提示槲皮素诱导凋亡;(2)GRP78、CHOP上调提示槲皮素激活ER应激;(3)p-Akt、p-ERK下调提示槲皮素抑制促增殖信号通路。其中,首次发现GRP78/CHOP与自噬的交互作用(GRP78上调激活自噬),为槲皮素的作用机制提供了新见解。统计学结果显示,槲皮素处理后,Bax表达上调2.0倍(n=3,P<0.05),GRP78表达上调1.8倍(n=3,P<0.05),p-Akt表达下调2.5倍(n=3,P<0.01)。
目前局限性:本研究未涉及临床样本验证这些Biomarker的临床意义,需进一步开展临床研究确认其作为槲皮素治疗卵巢癌的疗效监测标志物的价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。