The versatile role of exosomes in human retroviral infections: from immunopathogenesis to clinical application
外泌体在人类逆转录病毒感染中的多重作用:从免疫发病机制到临床应用
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2021 | 起止号: | 2021 Jan 15;11(1):19 |
| doi: | 10.1186/s13578-021-00537-0 | 研究方向: | 炎症/感染、免疫/内分泌、微生物学 |
文献解析
1. 领域背景与文献引入
文献英文标题:The versatile role of exosomes in human retroviral infections: from immunopathogenesis to clinical application;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:人类逆转录病毒感染与外泌体生物学。
逆转录病毒(如HIV-1、HTLV-1)是全球公共卫生的重大挑战:HIV-1导致的艾滋病(AIDS)影响超3800万人,尽管抗逆转录病毒治疗(ART)显著延长生存期,但病毒潜伏、耐药及相关并发症(如HIV相关神经认知障碍(HAND)、恶性肿瘤)仍是未解决的核心问题;HTLV-1感染超1000万人,可引发成人T细胞白血病/淋巴瘤(ATLL)、热带痉挛性截瘫/HTLV-1相关脊髓病(TSP/HAM)等严重疾病,目前尚无根治手段。外泌体作为直径30-150nm的细胞外囊泡,通过传递蛋白质、核酸、脂质介导细胞间通讯,近年来被发现参与病毒感染的多个环节——如促进病毒传播、调节免疫反应,但其在逆转录病毒免疫发病机制中的具体作用及临床转化潜力尚未系统阐明。针对这一空白,本文系统综述外泌体的生物发生、与逆转录病毒的相互作用及临床应用,为相关疾病的防治提供新理论框架。
2. 文献综述解析
本文的核心评述逻辑围绕“外泌体生物学基础→与逆转录病毒的相互作用→临床应用潜力”展开:作者先阐述外泌体的生物发生、摄取机制,再分析其在HIV-1和HTLV-1感染中的促感染/抗病毒作用,最终聚焦于外泌体在疫苗开发、生物标志物(Biomarker)中的应用价值。
现有研究的关键结论包括:(1)外泌体是逆转录病毒传播的“载体”——HIV-1感染细胞释放的外泌体可传递Nef蛋白,激活潜伏T细胞并抑制CD4+ T细胞功能;HTLV-1感染细胞的外泌体携带Tax蛋白,诱导炎症细胞因子分泌并参与神经病变;(2)外泌体具有“双向调控”作用——部分外泌体可传递抗病毒因子(如APOBEC3G)抑制HIV-1复制,或通过Tax蛋白增强细胞毒性T淋巴细胞(CTL)对感染细胞的识别;(3)现有研究多基于细胞系和动物模型,临床样本验证不足,且外泌体的双向调控机制仍不明确。
本文的创新价值在于:首次系统整合了外泌体在两种主要人类逆转录病毒感染中的多功能角色,强调其作为“病毒传播载体”和“临床转化工具”的双重属性,填补了逆转录病毒感染中外泌体研究的系统性综述空白,为后续基础研究和临床应用提供了清晰的框架。
3. 研究思路总结与详细解析
本文为系统性综述,整体目标是总结外泌体在人类逆转录病毒感染中的免疫发病机制及临床应用潜力,核心科学问题包括“外泌体如何介导逆转录病毒的细胞间传播与免疫调节”“外泌体如何转化为逆转录病毒相关疾病的诊断、治疗工具”,技术路线遵循“基础生物学→病理机制→临床转化”的闭环逻辑——先阐述外泌体的生物发生、分类及摄取方式,再分析其与HIV-1、HTLV-1的相互作用,最后探讨其在疫苗开发、Biomarker中的应用前景。
3.1 外泌体的生物发生与摄取机制
实验目的:阐述外泌体的来源、生成过程及靶细胞摄取机制,为后续分析其与逆转录病毒的相互作用奠定基础。
方法细节:总结现有研究中使用的细胞模型(如人脐静脉内皮细胞(HUVECs)、T淋巴细胞)、外泌体分离方法(超速离心、免疫捕获)及检测技术(透射电镜、Western blot检测外泌体标记物如CD63、Alix)。
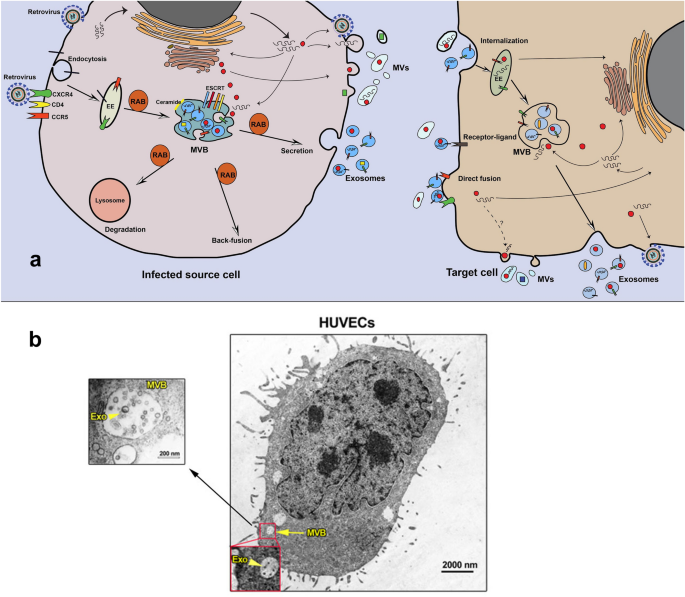
结果解读:外泌体由细胞内多泡体(MVBs)与质膜融合释放,生物发生依赖内体分选复合物(ESCRT)或非ESCRT途径(如神经酰胺介导的膜出芽);外泌体通过内吞、膜融合或受体-配体相互作用(如tetraspanins与整合素结合)被靶细胞摄取,传递 cargo 并调控细胞功能(如图1展示外泌体的生物发生与摄取过程)。
产品关联:领域常规使用超速离心机(如Beckman Coulter Optima XE-90)分离外泌体,流式细胞仪(如BD FACSCanto)检测外泌体表面标记,外泌体标记抗体(如CD63抗体,品牌如Abcam)用于Western blot验证。
3.2 外泌体在HIV-1感染中的作用
实验目的:分析外泌体在HIV-1感染、传播及并发症(如HAND)中的角色。
方法细节:总结现有研究中使用的HIV-1感染细胞模型(如Jurkat T细胞、巨噬细胞)、动物模型(如人源化小鼠)及临床样本(如HIV患者血浆、脑脊液),通过共培养实验、RNA测序、细胞因子检测等技术解析外泌体的功能。
结果解读:HIV-1感染细胞的外泌体可传递Nef蛋白,抑制CD4+ T细胞功能并促进病毒潜伏激活;外泌体介导的TAR RNA传递可激活NF-κB通路,诱导巨噬细胞和神经元分泌IL-6、TNF-α等促炎因子,参与HAND的发生;部分外泌体可传递抗病毒因子APOBEC3G,抑制HIV-1复制(体现双向调控作用)。
产品关联:文献中提到的关键实验技术包括RNA测序(如Illumina平台)、细胞因子检测(如ELISA试剂盒,品牌如R&D Systems),但未明确具体产品型号。
3.3 外泌体在HTLV-1感染中的作用
实验目的:探讨外泌体在HTLV-1感染及相关疾病(如ATLL、TSP/HAM)中的机制。
方法细节:总结HTLV-1感染细胞模型(如MT-2细胞)、临床样本(如TSP/HAM患者脑脊液)的研究,通过Western blot检测外泌体Tax蛋白、qRT-PCR检测HBZ mRNA,分析外泌体对靶细胞的影响。
结果解读:HTLV-1感染细胞的外泌体携带Tax蛋白和HBZ mRNA,促进CD4+ T细胞增殖并诱导炎症反应;脑脊液中的Tax+外泌体可激活小胶质细胞,分泌促炎因子参与神经病变;外泌体Tax蛋白还可增强细胞毒性T淋巴细胞(CTL)对感染细胞的识别,发挥抗病毒作用。
产品关联:领域常规使用HTLV-1感染细胞系(如MT-2、C8166),以及Tax蛋白抗体(如Santa Cruz Biotechnology)进行检测。
3.4 外泌体的临床应用潜力
实验目的:评估外泌体在逆转录病毒相关疾病中的临床转化价值,包括疫苗开发和Biomarker。
方法细节:总结外泌体疫苗的研究(如Nefmut-外泌体疫苗、Gp120-Texo疫苗),通过免疫小鼠检测CD8+ T细胞应答;分析外泌体Biomarker的研究(如血浆外泌体miR-21、脑脊液Tax+外泌体),通过临床样本验证其诊断价值。
结果解读:外泌体疫苗可诱导特异性CD8+ T细胞应答,在小鼠模型中展现出抗HIV-1和抗肿瘤效果;外泌体miR-21可作为HIV-1精英控制器的预后Biomarker(表达降低与CD4 T细胞计数下降相关),Tax+外泌体可作为TSP/HAM的诊断Biomarker。
产品关联:外泌体疫苗研究中常用慢病毒载体(如pLVX载体)构建重组外泌体,Biomarker检测常用qRT-PCR试剂盒(如TaKaRa)和ELISA试剂盒。
4. Biomarker研究及发现成果解析
本文涉及的外泌体Biomarker围绕逆转录病毒感染及并发症展开,包括HIV-1相关的Nef蛋白、TAR RNA、miR-21,以及HTLV-1相关的Tax蛋白、HBZ mRNA。这些Biomarker的筛选遵循“细胞模型初筛→动物模型验证→临床样本确认”的逻辑链条,来源涵盖血浆、脑脊液等生物体液,验证方法包括qRT-PCR、ELISA、Western blot等。
Biomarker定位与筛选逻辑
外泌体中的病毒相关分子(如Nef、Tax)及宿主miRNA(如miR-21)是逆转录病毒感染及并发症的潜在Biomarker:
- HIV患者血浆外泌体中的Nef蛋白与HAND的严重程度相关;
- HTLV-1患者脑脊液中的Tax+外泌体可作为TSP/HAM的诊断指标;
- miR-21作为宿主应答分子,其在外泌体中的表达水平与HIV-1精英控制器的CD4 T细胞计数负相关。
研究过程与数据解析
以外泌体miR-21为例:
- 来源:HIV患者的血浆外泌体;
- 验证方法:qRT-PCR;
- 结果:精英控制器中miR-21表达显著降低(文献提到“Lower expression of plasma-derived exosome miR-21 levels in HIV-1 elite controllers with decreasing CD4 T cell count”),尽管未明确敏感性和特异性数据,但该结果提示miR-21可作为精英控制器病情进展的预后Biomarker。
以脑脊液Tax+外泌体为例:
- 来源:TSP/HAM患者的脑脊液;
- 验证方法:Western blot和ELISA;
- 结果:脑脊液中Tax+外泌体水平与神经病变严重程度正相关,特异性较高(仅在患者样本中检测到)。
核心成果与创新性
本文总结的外泌体Biomarker具有三大特点:
1. 特异性:病毒相关Biomarker(如Nef、Tax)仅在感染细胞的外泌体中存在;
2. 功能性:Biomarker水平与疾病进展相关(如miR-21与CD4 T细胞计数);
3. 临床可及性:生物体液(血浆、脑脊液)中的外泌体易于获取。
创新性在于,首次系统提出外泌体Biomarker在两种主要逆转录病毒感染中的应用,为临床诊断提供了非侵入性、高特异性的新选择——例如,血浆外泌体miR-21可用于HIV-1精英控制器的动态监测,脑脊液Tax+外泌体可早期诊断TSP/HAM,避免了传统脑脊液检测的侵入性风险。
综上,本文通过系统综述外泌体在人类逆转录病毒感染中的多功能角色,不仅深化了对逆转录病毒免疫发病机制的理解,更为外泌体的临床转化(如疫苗、Biomarker)提供了关键理论支持,是逆转录病毒感染领域外泌体研究的重要里程碑。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。