Single-cell sequencing combined with spatial transcriptomics reveals the characteristics of follicle-targeted inflammation patterns in primary cicatricial alopecia
单细胞测序结合空间转录组学揭示了原发性瘢痕性脱发中毛囊靶向炎症模式的特征
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2025 | 起止号: | 2025 Jul 16;15(1):102 |
| doi: | 10.1186/s13578-025-01447-1 | 研究方向: | 炎症/感染、细胞生物学 |
文献解析
1. 领域背景与文献
文献英文标题:Single-cell and spatial transcriptomics reveal follicle-targeted inflammation in lichen planopilaris;发表期刊:BMC Medical Genomics;影响因子:未公开;研究领域:原发性瘢痕性脱发(扁平苔藓性毛发脱落)的免疫微环境与发病机制研究。
原发性瘢痕性脱发(PCA)是一类因免疫介导毛囊不可逆破坏导致永久性脱发的疾病,扁平苔藓性毛发脱落(LPP)是其最常见的亚型之一。领域发展关键节点可分为三个阶段:传统治疗阶段,以局部类固醇、羟氯喹、多西环素等为主,但临床疗效普遍不佳;新兴治疗探索阶段,Janus激酶(JAK)抑制剂的应用显示出初步疗效,但缺乏机制研究支持其作用靶点;机制解析阶段,临床队列研究证实CD8+T细胞浸润和IFN-γ信号是LPP的核心驱动因素,但尚未深入到单细胞和空间层面的细胞亚群交互网络。当前研究热点聚焦于毛囊免疫特权崩溃的分子机制、特异性免疫细胞亚群的功能解析,以及开发精准靶向治疗策略。未解决的核心问题包括:LPP中毛囊靶向炎症的具体细胞亚群组成及信号交互机制尚不明确,JAK抑制剂治疗LPP的作用靶点未阐明,巨噬细胞在LPP中的具体功能仍不清楚。
针对上述研究空白,本研究首次整合单细胞RNA测序(scRNA-seq)与空间转录组技术,系统解析LPP患者头皮组织的细胞组成、空间定位及细胞通讯网络,明确了CD8+效应记忆T细胞(Tem)、M1A巨噬细胞及毛囊干细胞(HFSCs)异常谱系在LPP发病中的核心作用,为LPP的精准治疗提供了新的靶点和机制依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括:按疾病类型分为原发性瘢痕性脱发(以LPP为代表)、继发性瘢痕性脱发(以局限性硬皮病LS为代表)及非瘢痕性脱发;按治疗手段分为传统治疗(局部类固醇、羟氯喹等)与新兴JAK抑制剂治疗;按发病机制分为淋巴细胞浸润、免疫特权崩溃、上皮间质转化(EMT)等方向。
现有研究的关键结论包括:LPP的核心发病机制是CD8+T细胞浸润毛囊漏斗部和隆突区,破坏毛囊免疫特权,直接攻击HFSCs并诱导EMT,最终导致毛囊破坏和瘢痕形成;巨噬细胞在LPP患者毛囊周围浸润增加,但具体功能尚未明确。技术方法优势方面,大样本临床队列研究明确了CD8+T细胞和IFN-γ在LPP中的核心作用,为发病机制解析提供了临床证据;局限性在于,现有研究多基于bulk转录组或组织病理分析,缺乏单细胞层面的细胞亚群解析,未揭示细胞间的空间交互网络,JAK抑制剂治疗LPP的作用机制缺乏实验证据支持,且未阐明巨噬细胞在LPP中的具体功能。
本研究的创新价值在于,首次将scRNA-seq与空间转录组技术结合,从单细胞和空间维度系统解析了LPP毛囊靶向炎症的细胞亚群及信号通路,明确了Tem细胞、M1A巨噬细胞及HFSCs异常谱系的核心作用,揭示了IFN-γ-STAT1、OSM-OSMR、CCL3-CCR5等信号通路的交互网络,填补了LPP发病机制中细胞交互层面的空白,同时为JAK抑制剂治疗LPP的疗效提供了直接的机制支持,为开发精准治疗策略奠定了基础。推测:CD8+NKG7+Tem细胞可能与LPP对类固醇治疗反应不佳有关,需进一步临床验证。
3. 研究思路总结与详细解析
本研究的核心目标是解析LPP毛囊靶向炎症的细胞与分子机制,明确驱动毛囊破坏和瘢痕形成的关键细胞亚群及信号通路;核心科学问题是LPP中免疫细胞与毛囊干细胞的空间交互如何调控毛囊免疫特权崩溃和HFSCs功能异常;技术路线遵循“样本采集-多组学测序-细胞亚群解析-信号通路验证-结论提炼”的闭环逻辑,通过scRNA-seq解析细胞组成,空间转录组明确细胞空间定位,免疫荧光验证关键分子和细胞亚群,最终构建LPP毛囊靶向炎症的细胞与分子调控网络。
3.1 样本采集与实验分组设计
实验目的是获取具有对比性的头皮组织样本,为后续多组学分析提供可靠材料,确保研究结果的科学性和可比性。方法细节:研究招募了经病理确诊的LPP患者(n=4)、LS患者(n=3)、雄激素性脱发(AGA)患者,以及因头皮痣切除的健康对照者(n=2);所有脱发患者在采样前6个月未接受系统或局部药物治疗,且无其他系统性疾病;采用4mm环钻从脱发病灶边缘的炎症进展区采集样本,每个患者采集3份样本,其中2份新鲜样本用于制备单细胞悬液,1份样本经福尔马林固定、石蜡包埋后用于HE染色、空间转录组测序和免疫荧光染色。结果解读:样本覆盖了原发性瘢痕性脱发、继发性瘢痕性脱发、非瘢痕性脱发及健康对照,确保了不同脱发类型的对比分析,为解析LPP的特异性发病机制提供了基础。实验所用关键产品:10x Genomics的Visium CytAssist Spatial Gene Expression for FFPE试剂盒,Melabio生物科技的四色荧光试剂盒,Illumina HiSeq XTen测序平台。
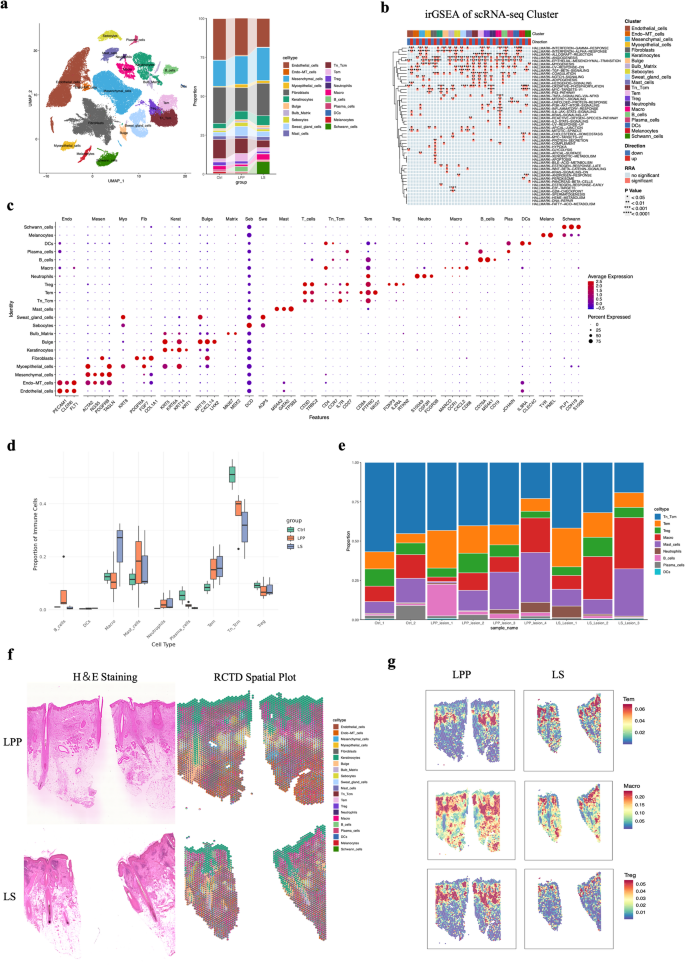
3.2 单细胞RNA测序与细胞亚群解析
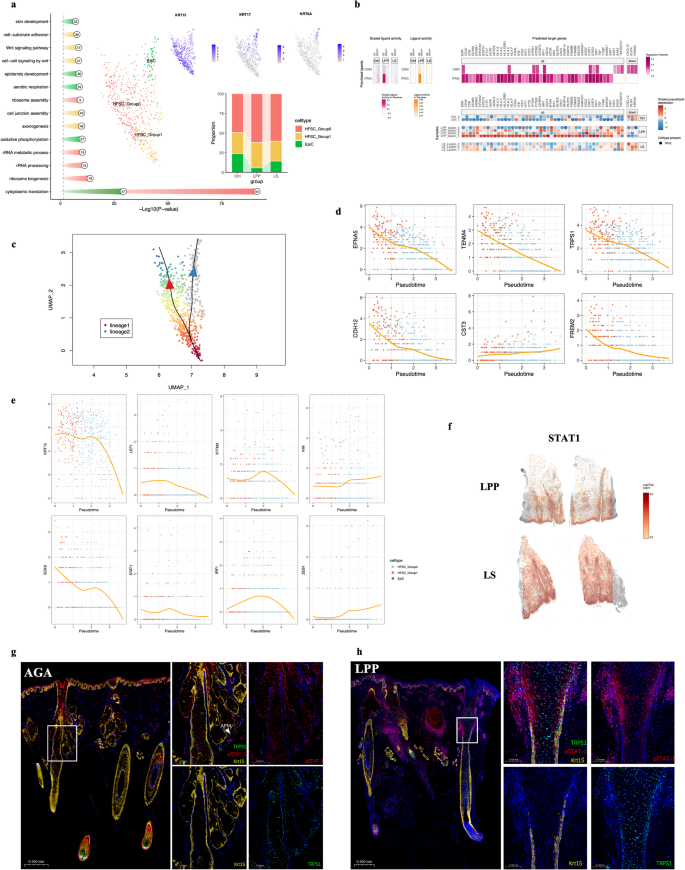
实验目的是系统解析不同样本的细胞组成、细胞亚群特征及基因表达差异,识别LPP特异性的细胞亚群。方法细节:将新鲜样本制备为单细胞悬液后,送至上海吉凯基因进行scRNA-seq,在Illumina HiSeq XTen平台进行150nt双端测序;使用Cell Ranger软件进行数据预处理,去除批次效应后,采用Seurat包进行UMAP降维、Leiden聚类,通过参考标记基因手动注释细胞类型;利用irGSEA包进行基因集富集分析,MultiNicheNet包分析细胞间配体-受体互作。结果解读:共鉴定出21种细胞类型,包括9种免疫细胞和12种皮肤结构细胞;LPP组中CD8+Tem细胞的比例显著高于健康对照和LS组(n=4 vs n=2 vs n=3,文献未明确提供具体数值,基于图表趋势推测),巨噬细胞亚群中M1A亚群(高表达CCL3、OSM)比例在LPP组中上调;空间转录组分析显示,Tem细胞主要定位于毛囊峡部和隆突区,与LPP的毛囊靶向炎症特征高度一致。实验所用关键产品:上海吉凯基因的单细胞测序服务,R语言的Seurat、irGSEA、MultiNicheNet分析包。
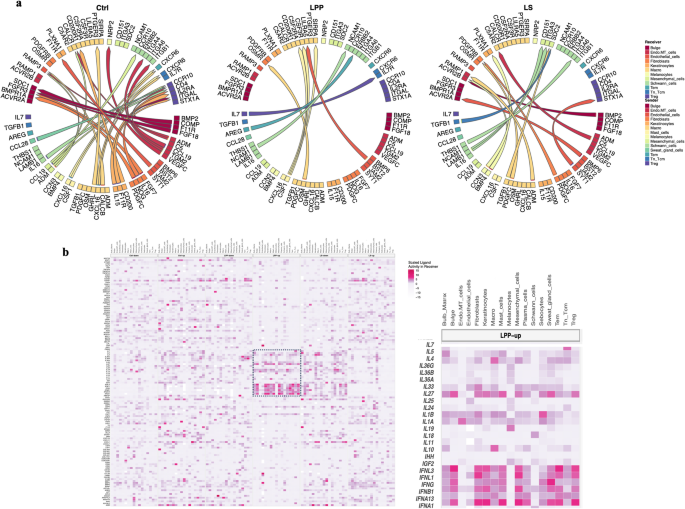
3.3 细胞通讯与信号通路解析
实验目的是揭示LPP中免疫细胞与毛囊细胞之间的信号交互网络,明确驱动LPP发病的核心信号通路。方法细节:对比健康对照、LPP、LS三组的配体-受体互作差异,分析不同细胞亚群的差异表达基因和配体活性;利用SCENIC包重构T细胞和隆突细胞的基因调控网络,解析转录因子的调控作用。结果解读:LPP组中,Tem细胞分泌的IFN-γ激活HFSCs中的STAT1信号通路,诱导HFSCs发生EMT,丧失干细胞特性;M1A巨噬细胞一方面分泌OSM直接作用于HFSCs的OSMR受体,抑制HFSCs活性,另一方面分泌CCL3结合Tem细胞表面的CCR5,激活Tem细胞的炎症反应,放大毛囊周围炎症;IFN-γ和OSM被证实是驱动LPP炎症和纤维化的关键因子,为JAK抑制剂的疗效提供了机制支持。推测:Janus激酶抑制剂可能通过阻断OSM-JAK-STAT5和IFN-γ-JAK-STAT1信号通路,恢复HFSCs的活性,从而改善LPP患者的脱发症状。实验所用关键产品:R语言的SCENIC分析包。
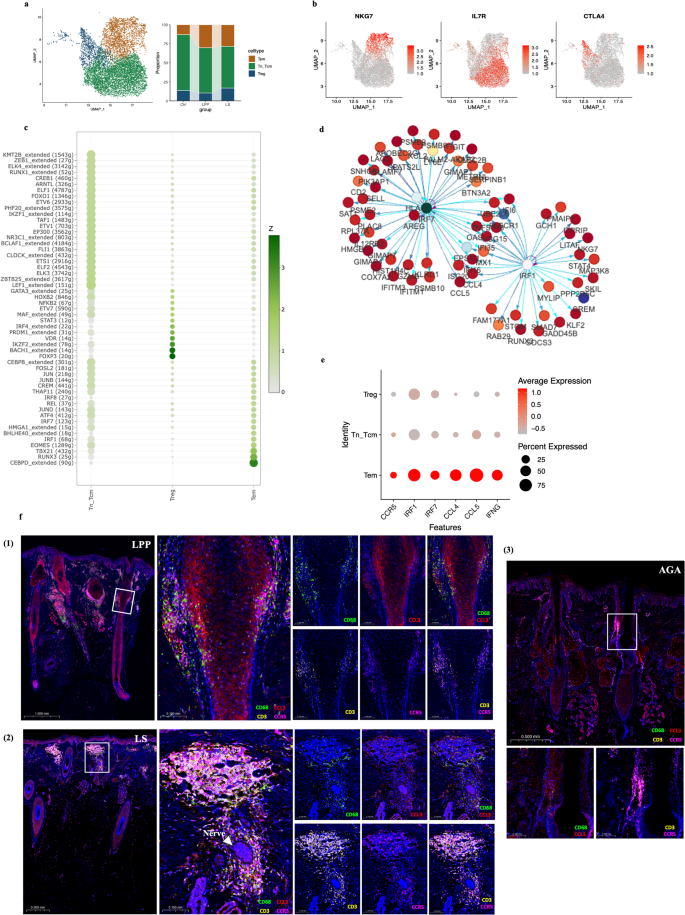
3.4 免疫荧光验证实验
实验目的是在蛋白水平验证scRNA-seq和空间转录组的结果,确认关键细胞亚群和信号通路在LPP中的表达与定位。方法细节:取石蜡包埋的样本制作4μm切片,依次进行烤片、脱蜡、抗原修复后,采用Melabio的四色荧光试剂盒(基于酪胺信号放大TSA技术)进行免疫荧光染色,标记包括CD3(T细胞)、CD68(巨噬细胞)、CCL3、CCR5、KRT15(HFSCs标记)、pSTAT1(STAT1激活标记)等;使用3D HISTECH数字病理扫描仪在20倍放大倍数下扫描整张切片。结果解读:LPP样本中,毛囊周围可见CD3+T细胞与CD68+巨噬细胞共浸润,CCL3与CCR5在炎症区域共定位,证实了M1A巨噬细胞通过CCL3-CCR5激活Tem细胞的机制;pSTAT1在LPP炎症区域HFSCs中的阳性率显著高于AGA样本(文献未明确提供具体数值,基于图表趋势推测),而HFSCs标记KRT15的表达显著降低,验证了STAT1激活导致HFSCs异常谱系转化的结论。实验所用关键产品:Melabio生物科技的四色荧光试剂盒,对应抗体信息见补充材料Table S2。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究鉴定的Biomarker涵盖细胞亚群标记、信号分子标记及功能状态标记三类。细胞亚群标记包括CD8+NKG7+Tem细胞(LPP特异性效应T细胞亚群)、M1A巨噬细胞(CCL3+OSM+TREM2+,LPP特异性促炎巨噬细胞亚群);信号分子标记包括IFN-γ(Tem细胞分泌的核心促炎因子)、OSM(M1A巨噬细胞分泌的HFSCs抑制因子)、CCL3(M1A巨噬细胞分泌的Tem细胞激活因子);功能状态标记包括pSTAT1(HFSCs异常激活标记)、TRPS1-(HFSCs干细胞特性丧失标记)。筛选与验证逻辑为:首先通过scRNA-seq从LPP样本中筛选差异表达的细胞亚群和信号分子,然后利用空间转录组验证其空间定位,最后通过免疫荧光染色在蛋白水平验证其表达与功能关联,形成完整的筛选-验证链条。
研究过程详述:所有Biomarker均来源于LPP患者头皮组织样本,包括新鲜单细胞悬液和石蜡包埋组织。验证方法包括:scRNA-seq分析基因表达水平及细胞亚群比例,空间转录组分析细胞和分子的空间定位,免疫荧光染色检测蛋白表达及共定位。特异性与敏感性方面,CD8+NKG7+Tem细胞在LPP组的比例显著高于健康对照和LS组(n=4 vs n=2 vs n=3,文献未明确提供具体数值,基于图表趋势推测);M1A巨噬细胞特异性聚集于LPP患者的毛囊炎症区域,在健康对照和LS组中分布稀疏;pSTAT1在LPP炎症区域HFSCs中的阳性率显著高于AGA样本(文献未明确提供具体数值,基于图表趋势推测),且与KRT15的表达呈负相关。
核心成果提炼:CD8+NKG7+Tem细胞通过分泌IFN-γ激活HFSCs中的STAT1信号通路,诱导HFSCs发生EMT并丧失干细胞特性,是LPP毛囊靶向炎症的核心效应细胞;M1A巨噬细胞通过两条通路促进LPP进展,一方面分泌OSM直接抑制HFSCs活性,另一方面分泌CCL3激活Tem细胞的炎症反应,放大毛囊周围炎症;IFN-γ和OSM是LPP发病的关键驱动因子,为JAK抑制剂治疗LPP提供了明确的作用靶点,JAK抑制剂可通过阻断IFN-γ和OSM的下游JAK-STAT信号通路,恢复HFSCs的功能,从而改善脱发症状。本研究首次揭示了STAT1激活在HFSCs异常谱系转化中的核心作用,为LPP的精准治疗提供了新的Biomarker和治疗靶点。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。