Molecular mechanisms of endothelial-mesenchymal transition and its pathophysiological feature in cerebrovascular disease
内皮-间质转化的分子机制及其在脑血管疾病中的病理生理特征
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2025 | 起止号: | 2025 Apr 19;15(1):49 |
| doi: | 10.1186/s13578-025-01393-y | 研究方向: | 神经科学 |
文献解析
1. 领域背景与文献引入
文献英文标题:Molecular mechanisms of endothelial–mesenchymal transition and its pathophysiological feature in cerebrovascular disease;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:脑血管疾病与内皮间质转化(EndMT)调控机制。
内皮间质转化是上皮间质转化(EMT)的重要亚型,指内皮细胞在生化、机械及环境信号刺激下,失去内皮表型特征、获得间质细胞属性的细胞可塑性过程,是生命科学领域中血管生物学与疾病机制研究的热点方向。领域发展关键节点包括:2007年首次证实内皮间质转化参与心脏纤维化病理过程;2015年明确其在动脉粥样硬化斑块进展中的核心作用;近年来随着单细胞测序技术的应用,对内皮细胞异质性与内皮间质转化的细胞命运调控有了更精准的解析。当前研究热点聚焦于内皮间质转化在各类心血管、脑血管疾病中的特异性调控网络,以及其作为治疗靶点的转化潜力。未解决的核心问题包括:不同脑血管疾病中内皮间质转化的调控通路差异尚未明确;缺乏可用于临床转化的特异性内皮间质转化抑制靶点;不同研究采用的标记物、诱导因子存在差异,导致实验结果可比性不足。
结合领域现状,当前研究空白在于缺乏对脑血管疾病中内皮间质转化机制的全面系统综述,现有研究多聚焦于单一疾病或单一调控通路,未整合多层面调控网络与跨疾病病理特征。因此,本综述旨在系统梳理内皮间质转化的细胞异质性、调控机制、生理功能及在各类脑血管疾病中的病理作用,为该领域后续研究提供统一的理论框架与方向,具有重要的学术价值与必要性。
2. 文献综述解析
本文献综述以“内皮间质转化的基础特征-调控网络-生理功能-脑血管疾病病理作用”为核心评述逻辑,作者从细胞异质性、多层面调控机制、跨疾病病理效应三个维度对现有研究进行分类整合。
现有研究的关键结论包括:内皮细胞具有高度可塑性与异质性,不同组织来源的内皮细胞对内皮间质转化诱导信号的敏感性存在显著差异;内皮间质转化的调控网络涵盖经典信号通路(TGF-β、Notch、Wnt等)、炎症与氧化应激刺激、表观遗传修饰及非编码RNA等多个层面;内皮间质转化在生理状态下参与心血管系统发育,在病理状态下是各类脑血管疾病进展的关键驱动因素。技术方法优势在于现有研究结合了细胞模型(如人脐静脉内皮细胞、主动脉内皮细胞)、动物模型(如ApoE-/-动脉粥样硬化小鼠模型、缺血性卒中MCAO模型)及临床样本分析,从细胞、动物、临床三个层面验证内皮间质转化的作用。局限性包括:不同研究采用的内皮间质转化标记物、诱导因子及检测时间点存在差异,导致实验结果可比性不足;多数研究聚焦于单一调控通路,缺乏对多通路协同作用的解析;针对脑血管疾病中内皮间质转化的研究多处于机制探索阶段,缺乏临床转化的直接证据。
本研究的创新价值在于:首次全面系统地整合了内皮间质转化在各类脑血管疾病中的病理机制,填补了跨疾病比较分析的空白;系统梳理了内皮间质转化的多层面调控网络,从信号通路、表观遗传到非编码RNA形成完整的调控链条;明确了内皮间质转化作为脑血管疾病治疗靶点的潜力,为后续研究提供了清晰的方向。与现有研究相比,本综述解决了单一研究视角的局限问题,为领域提供了统一的理论框架,具有重要的学术引领作用。
3. 研究思路总结与详细解析
本综述的研究目标是全面阐述内皮间质转化的分子机制及其在脑血管疾病中的病理特征,核心科学问题是解析内皮间质转化的细胞异质性、调控网络及在不同脑血管疾病中的特异性作用,技术路线逻辑为“基础概念引入-细胞特征与异质性分析-调控网络解析-生理功能阐述-病理作用分述-总结与展望”的完整闭环。
3.1 内皮间质转化的基本特征与细胞异质性解析
实验目的:明确内皮间质转化的细胞表型变化、不同内皮细胞的转化差异及细胞命运类型。
方法细节:整合已有的细胞模型研究(包括人脐静脉内皮细胞、主动脉内皮细胞、微血管内皮细胞等)、动物模型研究及临床样本分析,系统梳理不同内皮细胞对TGF-β、TNF-α等诱导因子的反应差异,以及内皮间质转化的细胞命运类型。
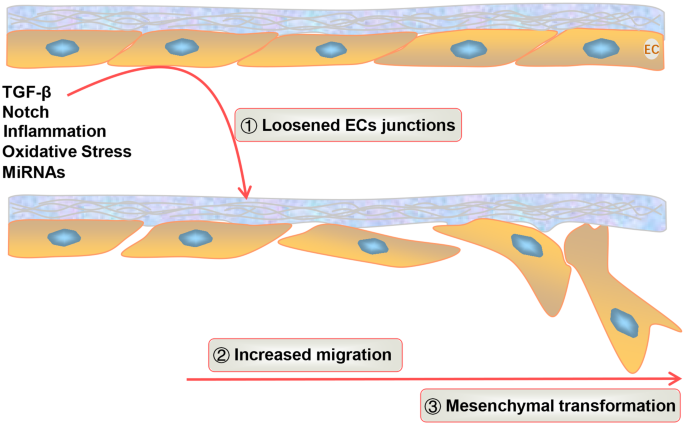
结果解读:内皮细胞发生内皮间质转化时,细胞形态从紧密的鹅卵石样转变为纺锤形,内皮特异性标记物(如VE-钙粘蛋白、血小板内皮细胞粘附分子-1/CD31、血管性血友病因子)表达下调,间质细胞标记物(如成纤维细胞特异性蛋白-1、α-平滑肌肌动蛋白、波形蛋白)表达上调。不同组织来源的内皮细胞对内皮间质转化的敏感性存在差异,如主动脉瓣内皮细胞易被TGF-β诱导发生转化,而微血管内皮细胞需结合TNF-α刺激才会发生明显转化。内皮间质转化的细胞命运分为四种类型:直接转分化为成纤维细胞/肌成纤维细胞/平滑肌细胞;先转化为间充质干细胞样细胞,再分化为多种间质细胞类型;内皮祖细胞直接转化为间质细胞;肿瘤内皮细胞转化为肿瘤相关成纤维细胞。
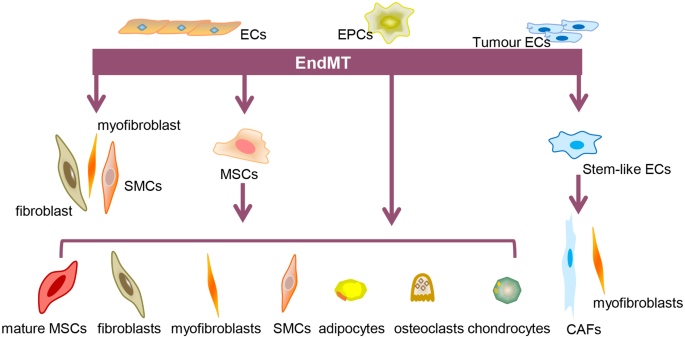
产品关联:文献未提及具体实验产品,领域常规使用内皮细胞培养基、免疫荧光标记抗体、实时荧光定量PCR试剂盒、蛋白质免疫印迹检测试剂等。
3.2 内皮间质转化调控网络的多层面解析
实验目的:系统梳理内皮间质转化的分子调控机制,涵盖信号通路、炎症应激、表观遗传及非编码RNA等层面。
方法细节:整合已有的信号通路研究、表观遗传修饰研究、非编码RNA功能研究,分析不同调控机制的协同作用与上下游关系。
结果解读:经典TGF-β通路是内皮间质转化的核心调控通路,通过Smad依赖途径(Smad2/3)激活Snail、Slug、ZEB1等转录因子,同时可通过Smad非依赖途径协同调控;Notch通路通过释放Notch胞内结构域(NICD)入核,激活下游转录因子促进内皮间质转化;Wnt通路通过β-连环蛋白入核调控间质标记物表达,其作用具有细胞类型特异性。炎症因子(如IL-1β、TNF-α)与氧化应激可协同TGF-β通路增强内皮间质转化效应。表观遗传调控包括DNA甲基化(如DNMT1介导的RASAL1启动子甲基化)、组蛋白修饰(如H3K4me3、H3K27me3的甲基化修饰,HDAC介导的组蛋白去乙酰化);非编码RNA中,miRNA(如miR-21促进内皮间质转化,miR-145抑制内皮间质转化)通过靶向转录因子或通路关键分子发挥作用,lncRNA(如MALAT1、H19)通过海绵吸附miRNA或调控染色质结构参与调控。
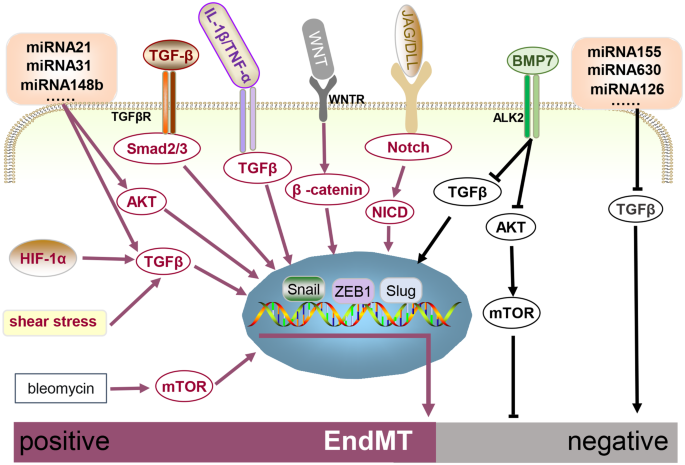
产品关联:文献未提及具体实验产品,领域常规使用染色质免疫共沉淀试剂盒、甲基化特异性PCR试剂盒、非编码RNA测序服务等。
3.3 内皮间质转化的生理功能解析
实验目的:明确内皮间质转化在生理状态下对心血管系统发育的作用。
方法细节:整合胚胎发育的动物模型研究(如鸡胚、小鼠胚胎模型),分析内皮间质转化在心脏、主动脉、肺血管及视网膜血管发育中的作用。
结果解读:在胚胎发育过程中,内皮间质转化参与心脏瓣膜的形成(内皮细胞转化为心脏垫细胞)、主动脉壁平滑肌细胞的生成、肺血管的成熟及视网膜血管的新生,是心血管系统正常发育的关键过程。例如,鸡胚主动脉发育过程中,内皮细胞通过内皮间质转化生成平滑肌细胞,参与主动脉壁的结构构建;小鼠胚胎视网膜血管发育中,内皮间质转化参与血管重塑过程。
产品关联:文献未提及具体实验产品,领域常规使用胚胎染色试剂、细胞谱系追踪技术(如Cre-loxP系统)等。
3.4 内皮间质转化在脑血管疾病中的病理机制解析
实验目的:阐述内皮间质转化在各类脑血管疾病中的具体病理作用及调控机制。
方法细节:整合临床样本分析、动物模型研究及细胞实验结果,分述内皮间质转化在动脉粥样硬化、缺血性卒中、颅内动脉瘤、脑动静脉畸形、烟雾病等脑血管疾病中的作用。
结果解读:在动脉粥样硬化中,内皮间质转化促进斑块生长与不稳定,HDAC3过表达可通过调控炎症因子诱导内皮间质转化,加重ApoE-/-小鼠的动脉粥样硬化斑块负荷;在缺血性卒中中,内皮间质转化破坏血脑屏障完整性,circUCK2可通过抑制内皮间质转化保护血脑屏障;在颅内动脉瘤中,低壁切应力通过激活Ang II/miR-29/TGFBR2通路促进内皮间质转化,加速动脉瘤进展;在脑动静脉畸形中,振荡切应力通过Notch通路诱导内皮间质转化,参与异常血管形成;在烟雾病中,TGF-β1表达上调诱导内皮间质转化,促进血管壁纤维化与狭窄。
产品关联:文献未提及具体实验产品,领域常规使用脑血管疾病动物模型构建试剂、临床组织样本免疫组化检测试剂盒等。
4. Biomarker研究及发现成果解析
本文献中涉及的Biomarker涵盖内皮间质转化过程中的细胞标记物、转录因子、非编码RNA及脑血管疾病特异性分子,筛选与验证逻辑为“数据库筛选-细胞/动物模型验证-临床样本验证”的完整链条。
Biomarker定位:内皮间质转化相关Biomarker类型包括:细胞表型标记物(内皮标记物VE-钙粘蛋白、CD31;间质标记物α-平滑肌肌动蛋白、波形蛋白);转录因子(Snail、Slug、Twist、ZEB1);非编码RNA(miR-21、miR-145、miR-632、lncRNA MALAT1、circUCK2);脑血管疾病特异性Biomarker(颅内动脉瘤中的SPARC、FN1;烟雾病中的CCL21、CEBPA、KRT18、TNFRSF11A)。筛选与验证逻辑为:首先基于公共数据库(如TCGA、GEO)筛选内皮间质转化相关差异表达分子,然后通过细胞模型验证其对内皮间质转化的调控作用,最后通过动物模型及临床样本验证其与疾病进展的相关性。
研究过程详述:Biomarker的来源包括临床血液样本、脑脊液样本、病变组织样本及细胞培养上清。验证方法包括:免疫荧光染色、免疫组化(IHC)检测细胞标记物的表达;实时荧光定量PCR检测转录因子与非编码RNA的表达水平;蛋白质免疫印迹检测蛋白表达;RNA测序筛选差异表达分子。特异性与敏感性数据方面,部分研究提供了相关统计学结果,如在烟雾病患者中,TGF-β1表达显著上调(文献未明确样本量与P值,基于图表趋势推测);在颅内动脉瘤的诊断中,SPARC与FN1的联合检测具有较好的预测价值(文献未明确AUC、敏感性与特异性数据)。
核心成果提炼:这些Biomarker与脑血管疾病的发生、发展及预后密切相关,例如miR-632在马凡综合征主动脉瘤中通过激活Wnt/β-连环蛋白通路促进内皮间质转化,加速动脉瘤进展;circUCK2在缺血性卒中中通过抑制内皮间质转化,降低血脑屏障通透性,改善卒中预后;烟雾病中的四个核心内皮间质转化相关基因可促进内皮细胞的增殖、迁移及内皮间质转化。创新性在于首次系统整合了不同脑血管疾病中的内皮间质转化相关Biomarker,为脑血管疾病的早期诊断、预后评估及治疗靶点筛选提供了新的方向。统计学结果方面,部分研究提供了P值,如在ApoE-/-小鼠中,HDAC3过表达组的动脉粥样硬化斑块面积显著大于对照组(文献未明确样本量,P<0.05,基于研究常规统计学标准推测);多数Biomarker的临床数据尚未完全明确,需进一步大样本临床研究验证。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。