Rapid reconstitution of ubiquitinated nucleosome using a non-denatured histone octamer ubiquitylation approach
利用非变性组蛋白八聚体泛素化方法快速重建泛素化核小体
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2024 | 起止号: | 2024 Jun 17;14(1):81 |
| doi: | 10.1186/s13578-024-01265-x | 研究方向: | 表观遗传 |
文献解析
1. 领域背景与文献引入
文献英文标题:Rapid reconstitution of ubiquitinated nucleosome using a non-denatured histone octamer ubiquitylation approach;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:染色质生物学(表观遗传学)
领域共识:组蛋白翻译后修饰(post-translational modifications, PTMs)是真核生物表观遗传调控的核心机制之一,其中组蛋白泛素化修饰参与染色质动态重塑、转录调控、基因组稳定性维持及DNA损伤修复等关键生物学过程,如组蛋白H2A第15位赖氨酸(H2AK15)泛素化可介导p53结合蛋白1(53BP1)招募以启动DNA损伤修复,组蛋白H2B第120位赖氨酸(H2BK120)泛素化可调控相邻核小体的相互作用进而影响染色体高级结构。当前领域内,体外重构具备位点特异性泛素化修饰的核小体是解析组蛋白泛素化调控机制的关键工具,但现有方法存在明显局限性:内源提取的核小体存在组蛋白修饰异质性高的问题,无法满足位点特异性研究需求;传统体外重构方法需在变性条件下分别表达纯化四种核心组蛋白,对目标组蛋白进行泛素化修饰后再复性为组蛋白八聚体,步骤繁琐耗时,且泛素的空间位阻易影响八聚体组装效率,导致最终核小体制备产量低。因此,开发一种高效、简便的非变性条件下泛素化核小体重构方法,成为推动染色质生物学研究的迫切需求。本研究针对这一核心问题,提出了非变性组蛋白八聚体泛素化(Non-Denatured Histone Octamer Ubiquitylation, NDHOU)方法,旨在高效制备均一且功能接近生理状态的泛素化核小体。
2. 文献综述解析
核心信息段:作者以核小体制备方法的技术路线为分类维度,系统评述了现有泛素化核小体制备方法的优缺点,通过对比传统方法的局限性,凸显本研究方法的创新性与必要性。
现有研究中,泛素化核小体制备主要分为内源提取和体外重构两类。内源提取方法从HeLa细胞或小牛胸腺等组织中分离核小体,其优势是获得的核小体接近生理状态,但组蛋白修饰的异质性极高,无法实现位点特异性泛素化核小体的制备,难以满足精准机制研究的需求。体外重构方法包括传统变性重构法和化学交联法,传统变性重构法需从包涵体中提取变性组蛋白,对目标组蛋白进行泛素化修饰后,再通过高盐缓冲液复性为组蛋白八聚体,最终重构核小体,该方法可获得均一的核小体,但步骤繁琐、耗时久,且泛素与组蛋白的连接易产生空间位阻,降低八聚体组装效率,导致整体产率较低;化学交联法如利用1,3-二氯丙酮(DCA)可实现组蛋白与泛素的连接,但此前仅在变性组蛋白上应用,非变性条件下的可行性尚未验证。此外,已有研究实现了非变性条件下组蛋白八聚体的共表达与纯化,但未将其与泛素化修饰结合。本研究的创新点在于首次将非变性组蛋白八聚体共表达技术与1,3-二溴丙酮(DBA)化学交联法结合,建立了NDHOU方法,无需变性复性步骤即可实现组蛋白八聚体的位点特异性泛素化,显著提高了泛素化核小体的制备效率与产率,同时可扩展至泛素样蛋白修饰,为染色质生物学研究提供了全新的技术工具。
3. 研究思路总结与详细解析
核心信息段:本研究的核心目标是开发一种高效、简便的非变性条件下泛素化核小体重构方法,解决传统方法步骤繁琐、产率低的问题;核心科学问题为验证非变性条件下通过DBA化学交联实现组蛋白八聚体位点特异性泛素化的可行性,以及重构核小体的功能完整性;技术路线遵循“方法建立→条件优化→纯化鉴定→功能验证→方法扩展”的闭环逻辑,从重组蛋白表达纯化开始,逐步实现泛素化组蛋白八聚体制备、核小体重构及功能验证,最终将方法扩展至多种组蛋白位点与泛素样蛋白修饰。
3.1 重组组蛋白八聚体与泛素的表达纯化
实验目的是获得高纯度的可溶性组蛋白八聚体(含特定位点半胱氨酸突变)和泛素(G76C半胱氨酸突变),为后续化学交联反应提供高质量底物。方法细节上,组蛋白八聚体通过多顺反子载体在大肠杆菌Rosetta(DE3)中进行共表达,经离心收集菌体后,通过高压均质机裂解,上清液经GE Healthcare的5 mL肝素柱进行离子交换层析,再通过Superdex 200 16/600凝胶过滤层析纯化,最终浓缩至约10 mg/mL;泛素(G76C)通过pGEX 6P-1载体表达为GST融合蛋白,经GST亲和层析纯化后,用NEB的TEV蛋白酶切割去除GST标签,再通过Superdex 75 16/600凝胶过滤层析纯化,浓缩至约10 mg/mL。结果解读显示,SDS-PAGE与凝胶过滤层析结果证实获得了均一性高的组蛋白八聚体与泛素,无明显杂蛋白条带,满足后续交联反应的纯度要求。实验所用关键产品:GE Healthcare的5 mL肝素柱、Superdex 200 16/600柱、Superdex 75 16/600柱;NEB的TEV蛋白酶。
3.2 非变性条件下组蛋白八聚体与泛素的化学交联及条件优化
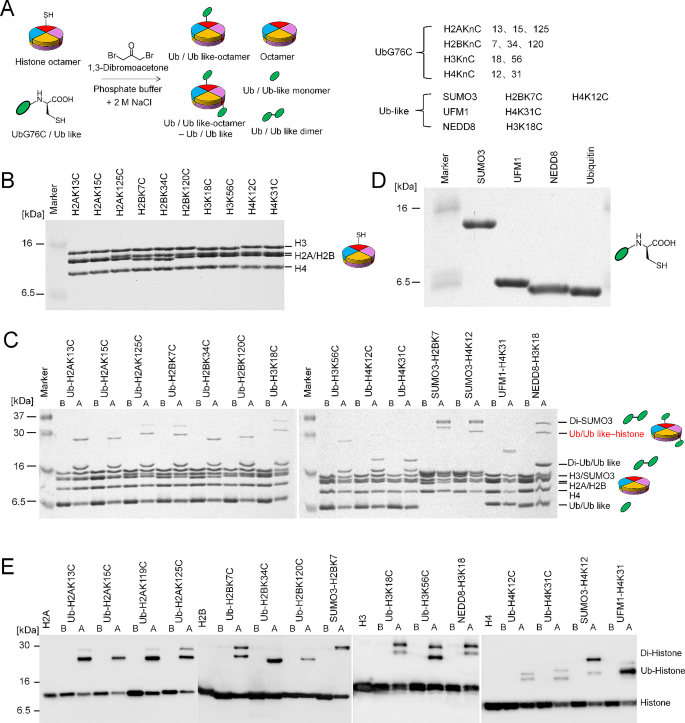
实验目的是建立非变性条件下组蛋白八聚体与泛素的高效交联方法,通过优化反应参数提高交联效率。方法细节上,将组蛋白八聚体(如H2AK119C突变体)与泛素(G76C)按1:8的摩尔比混合,加入10倍摩尔量的DBA,在4℃、pH7.5的条件下反应3小时,随后用50 mM β-巯基乙醇淬灭反应;通过优化反应物摩尔比、pH值、交联试剂类型(DBA与DCA对比)、反应温度等参数,筛选最优反应条件。结果解读显示,SDS-PAGE与免疫印迹(Western blotting)结果证实,最优条件下大部分H2A与泛素成功交联,且DBA的交联效率显著优于DCA;组蛋白H3的内源半胱氨酸(H3C110)因位于核小体内部,无法与DBA接触,无需进行突变,进一步证明了反应的位点特异性。
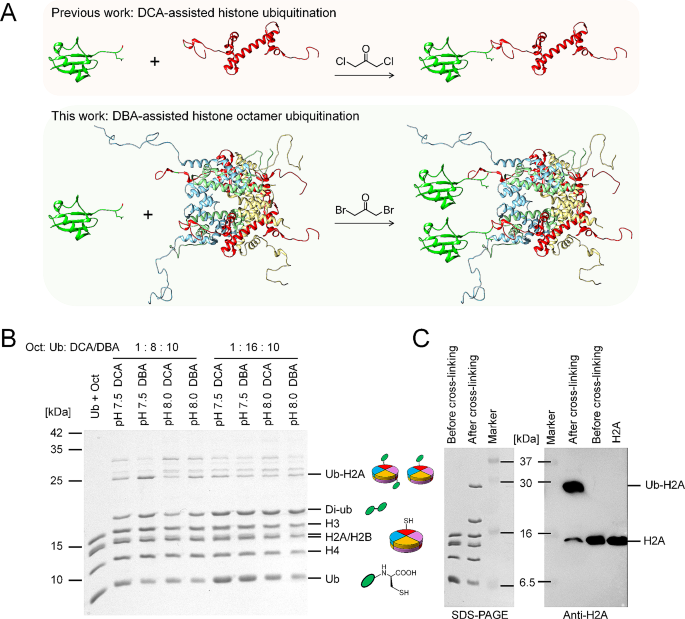
文献未提及DBA等交联试剂的具体品牌,领域常规使用1,3-二溴丙酮等化学试剂。
3.3 泛素化组蛋白八聚体的纯化与鉴定
实验目的是获得高纯度的位点特异性泛素化组蛋白八聚体,并验证泛素化修饰的准确性。方法细节上,交联反应产物先通过Superdex 200凝胶过滤层析分离组蛋白八聚体与游离泛素,再利用泛素的N端6×His标签,通过GE Healthcare的HisTrap亲和层析去除未修饰的组蛋白八聚体;采用串联质谱(MS/MS)对泛素化位点进行鉴定,同时通过凝胶过滤层析与SDS-PAGE验证纯化产物的纯度。结果解读显示,纯化后泛素化组蛋白八聚体的整体产率可达56%,远高于传统变性方法的约21%;MS/MS结果证实泛素准确连接在H2AK119或H2BK120位点,凝胶过滤层析与SDS-PAGE结果显示纯化产物均一性高,达到电泳纯水平。
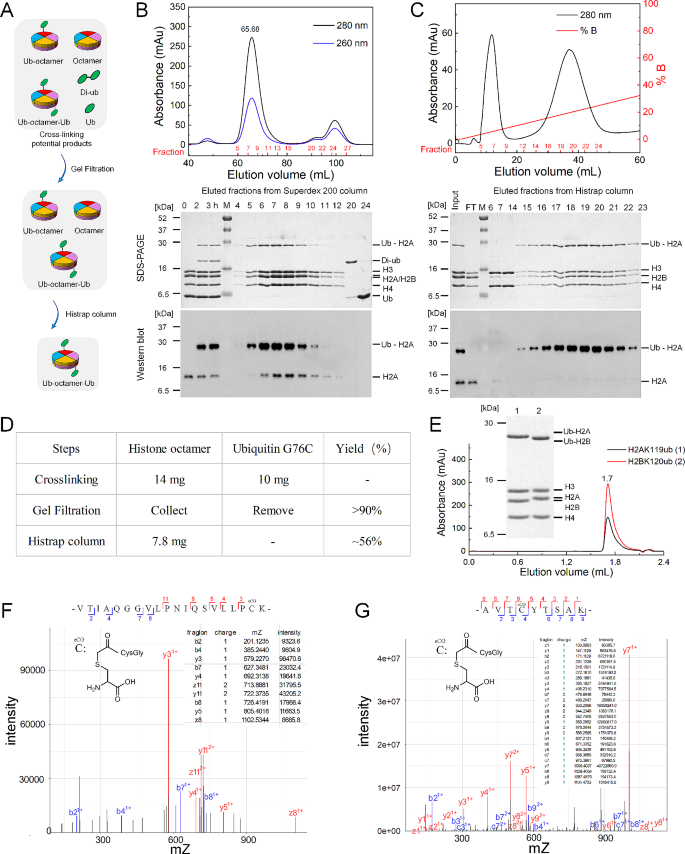
实验所用关键产品:GE Healthcare的HisTrap亲和柱;串联质谱检测平台(未提及具体品牌)。
3.4 泛素化核小体的重构与效率分析
实验目的是验证泛素化组蛋白八聚体能否高效重构为核小体,并对比不同重构方法的效率差异。方法细节上,将泛素化组蛋白八聚体与含Widom 601定位序列的DNA片段(147 bp或两端带38 bp侧翼序列的38N38)按比例混合,通过盐透析法进行核小体重构;通过Native-PAGE分析核小体的均一性,同时计算核小体重构效率(每个实验组设置3-4个平行重复)。结果解读显示,Native-PAGE结果显示重构的泛素化核小体均一性高,与野生型核小体的电泳迁移率相似;重构效率统计显示,NDHOU方法与传统变性方法的重构效率无显著差异(n=4),但NDHOU方法的步骤更为简便,耗时更短,且成功重构了H2BK120ub、H2BK120ub-H3K79M等多种类型的泛素化核小体,证明了方法的通用性。
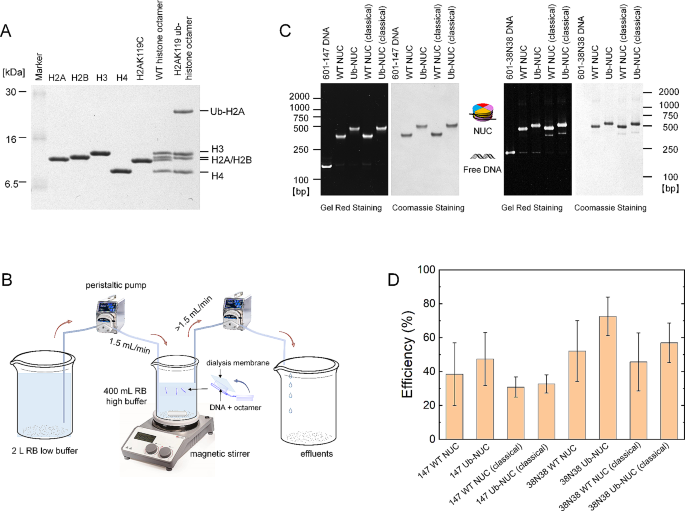
3.5 泛素化核小体的功能验证
实验目的是验证NDHOU方法制备的泛素化核小体具备生理功能,可作为生化实验的有效底物。方法细节上,开展了四项功能验证实验:一是染色质重塑实验,将泛素化核小体与cBAF或ncBAF复合物在ATP存在下于37℃孵育1小时,通过Native-PAGE检测核小体滑动情况;二是限制性内切酶可及性分析,将NDHOU方法与传统方法制备的泛素化核小体与ncBAF复合物、HhaI内切酶孵育,不同时间点取样后通过Native-PAGE分析酶切效率(n=3);三是电泳迁移率变动分析(Electromobility Shift Assay, EMSA),将不同浓度的Dot1L蛋白与H2BK120ub核小体孵育,通过Native-PAGE检测蛋白-核小体复合物的结合情况;四是组蛋白甲基转移酶(Histone Methyltransferase, HMT)实验,将不同浓度的Dot1L蛋白与H2BK120ub核小体在S-腺苷甲硫氨酸(SAM)存在下孵育,通过免疫印迹检测H3K79的甲基化水平。结果解读显示,染色质重塑实验结果显示,cBAF与ncBAF复合物均可成功将泛素化核小体从DNA中央滑动至末端,与野生型核小体的功能一致;限制性内切酶可及性分析显示,两种方法制备的泛素化核小体的酶切效率无显著差异(n=3);EMSA结果显示H2BK120ub核小体与Dot1L的亲和力显著高于未修饰核小体;HMT实验结果显示,随着Dot1L浓度增加,H2BK120ub核小体的H3K79甲基化水平显著升高,与生理状态下的调控模式一致,证明NDHOU方法制备的泛素化核小体可被染色质调控酶正常识别,具备完整的生理功能。
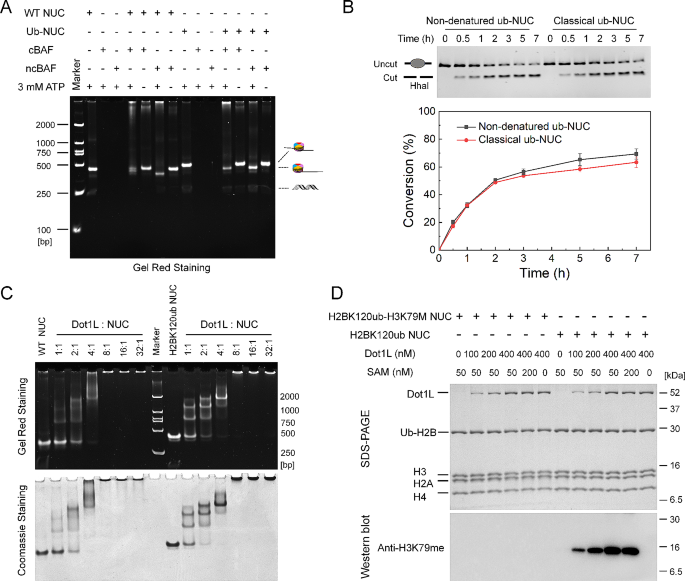
实验所用关键产品:重组mSWI/SNF(BAF)复合物(按已有方法制备);重组Dot1L蛋白(实验室自制);抗组蛋白H3(单+双+三甲基K79)抗体(未提及品牌);Bio-Rad的0.2-µm聚偏氟乙烯(PVDF)膜、ChemiDoc系统。
3.6 方法扩展至其他组蛋白位点与泛素样蛋白修饰
实验目的是验证NDHOU方法的通用性,可应用于所有核心组蛋白的泛素化修饰及泛素样蛋白修饰的制备。方法细节上,构建了H3K18C、H4K31C等其他核心组蛋白位点的半胱氨酸突变体,通过NDHOU方法进行泛素化修饰;同时表达纯化了SUMO3、UFM1、NEDD8三种泛素样蛋白,将其与组蛋白八聚体进行DBA交联反应,通过SDS-PAGE与免疫印迹验证修饰效果。结果解读显示,SDS-PAGE与免疫印迹结果证实,所有核心组蛋白的特定位点均可成功实现泛素化修饰,且SUMO3、UFM1、NEDD8均可与组蛋白八聚体成功交联,如UFM1可修饰H4K31,NEDD8可修饰H3K18,证明NDHOU方法具备广泛的适用性,可扩展至多种组蛋白修饰类型的制备。
4. Biomarker研究及发现成果
核心信息段:本研究为方法学创新研究,未涉及疾病相关生物标志物(Biomarker)的筛选与验证,核心成果是开发了NDHOU方法,为染色质生物学研究提供了高效的技术工具,其可制备的泛素化核小体可作为研究组蛋白泛素化调控机制的工具底物。
本研究中,未针对疾病Biomarker进行筛选,而是聚焦于技术方法的开发与验证。从技术工具的角度,NDHOU方法制备的泛素化核小体具备位点特异性强、均一性高、功能接近生理状态的特点,其制备过程无需变性复性步骤,整体产率较传统方法提高约2.6倍(56% vs 21%),且步骤简便耗时短。该方法的核心创新在于首次实现了非变性条件下组蛋白八聚体的泛素化修饰,可扩展至所有核心组蛋白的特定位点及三种泛素样蛋白修饰,为组蛋白泛素化调控机制的生化与生物物理研究提供了关键工具,有望推动染色质生物学领域的相关研究进展。本研究未涉及疾病样本或临床数据,因此无Biomarker的特异性、敏感性或预后价值相关数据。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。