CD24(+)LCN2(+) liver progenitor cells in ductular reaction contributed to macrophage inflammatory responses in chronic liver injury
CD24(+)LCN2(+)肝脏祖细胞在胆管反应中促进了慢性肝损伤中的巨噬细胞炎症反应。
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2023 | 起止号: | 2023 Oct 2;13(1):184 |
| doi: | 10.1186/s13578-023-01123-2 | 靶点: | LCN2、CD24、CD2 |
| 研究方向: | 炎症/感染、细胞生物学、毒理研究、免疫/内分泌 | 疾病类型: | 肝损伤 |
| 细胞类型: | 巨噬细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:CD24⁺ LCN2⁺ liver progenitor cells in ductular reaction contributed to macrophage inflammatory responses in chronic liver injury;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:慢性肝损伤与肝脏祖细胞功能研究(肝脏病学、干细胞生物学交叉领域)。
肝脏是人体具备强大再生潜能的器官,在慢性肝损伤(如肝纤维化、非酒精性脂肪性肝炎NASH)进程中,常伴随胆管反应的发生,即胆管反应性细胞的病理性增殖与扩张,这类细胞表达肝胆谱系中间标志物,被认为是兼性肝脏祖细胞(LPCs)激活的体现。领域共识:过去二十年间,谱系追踪技术的发展明确了肝细胞、胆管上皮细胞(BECs)均可在慢性损伤后转化为LPCs,参与肝组织修复与再生,但不同来源LPCs的功能差异及其在胆管反应中的具体作用一直存在争议。当前研究热点聚焦于明确不同LPCs亚群的身份、来源与功能,以及其在肝损伤修复中的调控机制,而未解决的核心问题包括:驻留LPCs(如Hering管内的干细胞样细胞)的功能特性尚不明确,不同来源LPCs对慢性肝损伤进程的影响存在差异,且LPCs与免疫细胞的互作机制未被充分揭示。
本研究正是针对上述研究空白,结合遗传谱系追踪与体外小分子重编程技术,系统定义了来源于肝脏实质和非实质组织的LPCs亚群,重点探讨了CD24⁺LCN2⁺LPCs在慢性肝损伤中的作用及其与巨噬细胞的互作机制,为慢性肝病的治疗靶点开发提供了新的理论依据。
2. 文献综述解析
作者对现有研究的分类维度为肝脏祖细胞(LPCs)的来源,包括肝细胞来源、胆管上皮细胞(BECs)来源、驻留LPCs来源三类,通过梳理不同来源LPCs的研究进展,明确当前领域的争议点与研究空白。
现有研究的关键结论显示,肝细胞在慢性肝损伤后可通过去分化转化为LPCs,进而促进肝实质的再生;BECs在肝细胞再生受抑制的条件下,可转分化为肝细胞参与修复;驻留LPCs被认为是肝脏中的潜在干细胞群,但由于缺乏特异性标志物,其功能与来源一直存在争议。技术方法方面,谱系追踪技术可精准追踪细胞的来源与命运,小分子重编程技术可在体外扩增LPCs,为功能研究提供了工具支持,但现有研究的局限性在于,缺乏对不同来源LPCs的直接功能比较,尤其是驻留LPCs的功能研究较为匮乏,且未揭示LPCs在慢性肝损伤中调控炎症反应的具体机制。
本研究的创新价值在于,首次通过体外小分子重编程技术成功获得三种不同来源的LPCs(肝细胞来源、BECs来源、驻留LPCs来源),并系统比较了其增殖、分化等功能特性;首次鉴定出CD24⁺LCN2⁺LPCs作为驻留LPCs激活后的特异性亚群,明确其在胆管反应中的核心作用;首次揭示了CD24⁺LCN2⁺LPCs通过分泌LCN2介导巨噬细胞M1极化,进而加重慢性肝损伤的分子机制,填补了领域内对驻留LPCs功能及LPCs-免疫细胞互作机制的研究空白。
3. 研究思路总结与详细解析
本研究的整体研究目标为明确不同来源肝脏祖细胞(LPCs)的身份与功能差异,揭示CD24⁺LCN2⁺LPCs在慢性肝损伤中的作用及调控机制;核心科学问题包括不同来源LPCs的谱系偏向性与功能特性,以及CD24⁺LCN2⁺LPCs与巨噬细胞的互作机制;技术路线遵循“细胞分离与诱导→体外功能鉴定→标志物筛选→体内功能验证→机制解析”的闭环逻辑,结合谱系追踪、小分子重编程、转录组分析、单细胞测序、体内移植等多种技术手段,系统解析了CD24⁺LCN2⁺LPCs的功能与机制。
3.1 不同来源肝脏祖细胞的分离与体外诱导培养
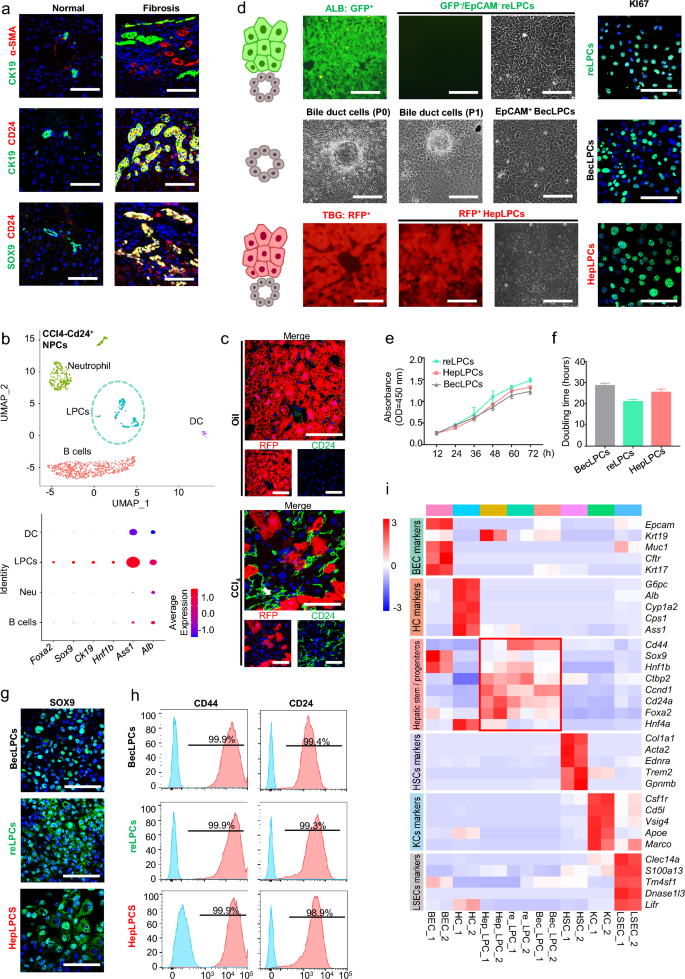
实验目的为从肝脏实质与非实质组织中分离不同来源的细胞,通过小分子鸡尾酒诱导转化为可稳定增殖的LPCs,并鉴定其祖细胞特性。方法细节上,研究人员从AAV8-Tbg-Cre介导重组的ROSA26tdTomato小鼠中分离tdTom⁺肝细胞,从野生型小鼠肝内胆管分离EpCAM⁺胆管上皮细胞,从AlbCreERT/R26GFP小鼠中分离ALB/GFP⁻EpCAM⁻细胞(驻留LPCs来源),随后使用包含EGF、HGF、Y27632等成分的过渡扩增培养基(TEM)进行体外培养,诱导细胞转化为LPCs。通过CCK-8实验、细胞计数检测细胞增殖能力,免疫荧光染色检测Ki67(增殖标志物)、SOX9(祖细胞标志物)的表达,流式细胞术检测CD24、CD44等表面标志物,转录组分析比较三种LPCs与其他肝脏细胞的基因表达谱。
结果解读显示,三种来源的细胞在TEM培养基中均成功转化为LPCs,具有相似的增殖能力,倍增时间无显著差异(n=3,P>0.05),免疫荧光染色显示三种LPCs均高表达Ki67与SOX9,流式细胞术检测显示其均表达CD24、CD44等祖细胞标志物,而不表达CD34、CD45等造血细胞标志物;转录组分析显示三种LPCs的基因表达谱与肝细胞、BECs、肝星状细胞等其他肝脏细胞存在明显差异,共同表达干细胞相关通路基因。
产品关联:文献未提及具体实验产品,领域常规使用流式细胞分选仪、免疫荧光染色试剂盒、CCK-8增殖检测试剂盒、转录组测序平台等。
3.2 不同来源肝脏祖细胞的功能差异分析
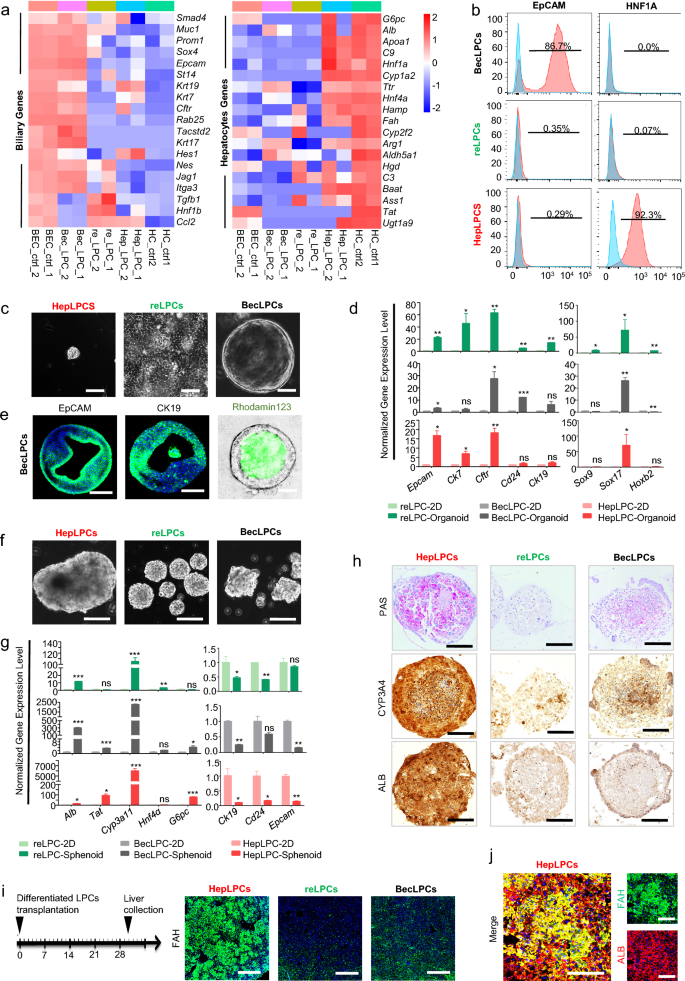
实验目的为比较三种来源LPCs的分化潜能与功能特性,明确其谱系偏向性。方法细节上,通过RNA-seq分析三种LPCs的基因表达谱,比较肝胆谱系标志物的表达差异;使用Matrigel 3D培养系统诱导胆管样类器官形成,通过免疫荧光染色检测EpCAM、CK19等胆管标志物的表达;使用3D球体培养系统诱导肝细胞分化,通过糖原染色、免疫组化染色检测CYP3A4、ALB等肝细胞功能标志物;将三种LPCs分别移植到Fah⁻/⁻小鼠体内,通过免疫荧光染色检测细胞的定植与成熟情况。
结果解读显示,RNA-seq分析表明,肝细胞来源的LPCs(HepLPCs)持续表达肝细胞谱系基因,BECs来源的LPCs(BecLPCs)表达胆管相关基因,而驻留LPCs来源的LPCs不表达这两类谱系基因;3D培养显示,BecLPCs可形成典型的胆管样类器官,高表达EpCAM与CK19(n=3,P<0.001),而HepLPCs的3D球体更易积累糖原,且CYP3A4、ALB的表达水平显著高于其他两组(n=3,P<0.01);体内移植实验显示,只有HepLPCs可在Fah⁻/⁻小鼠体内定植并成熟为功能性肝细胞,表达FAH与ALB。
产品关联:文献未提及具体实验产品,领域常规使用Matrigel基质胶、实时荧光定量PCR试剂盒、免疫组化染色试剂盒、动物活体成像系统等。
3.3 CD24⁺LCN2⁺肝脏祖细胞的特异性标志物鉴定与体内验证
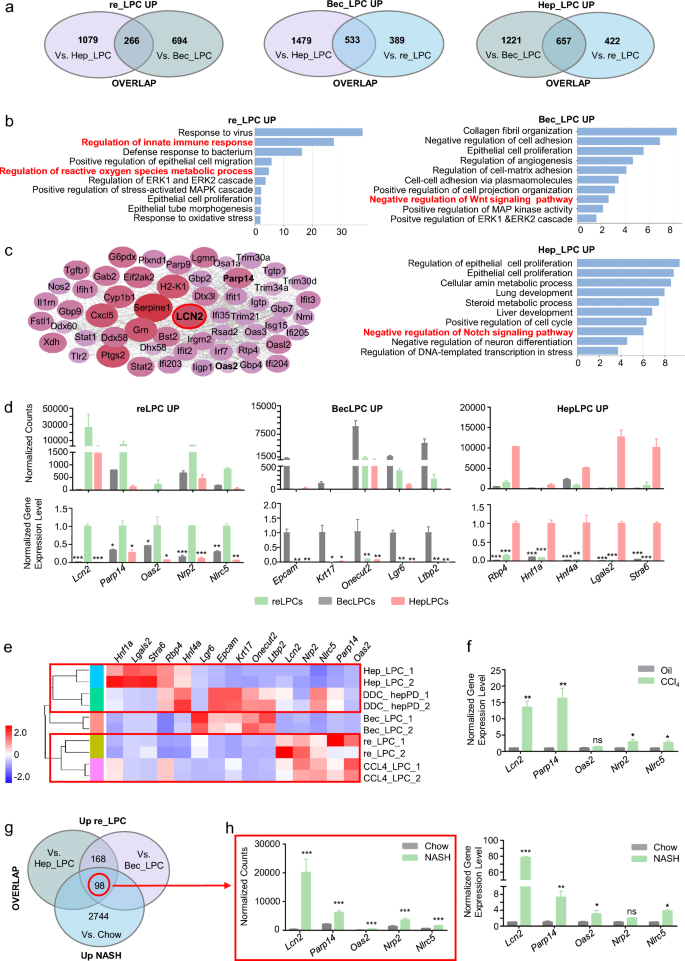
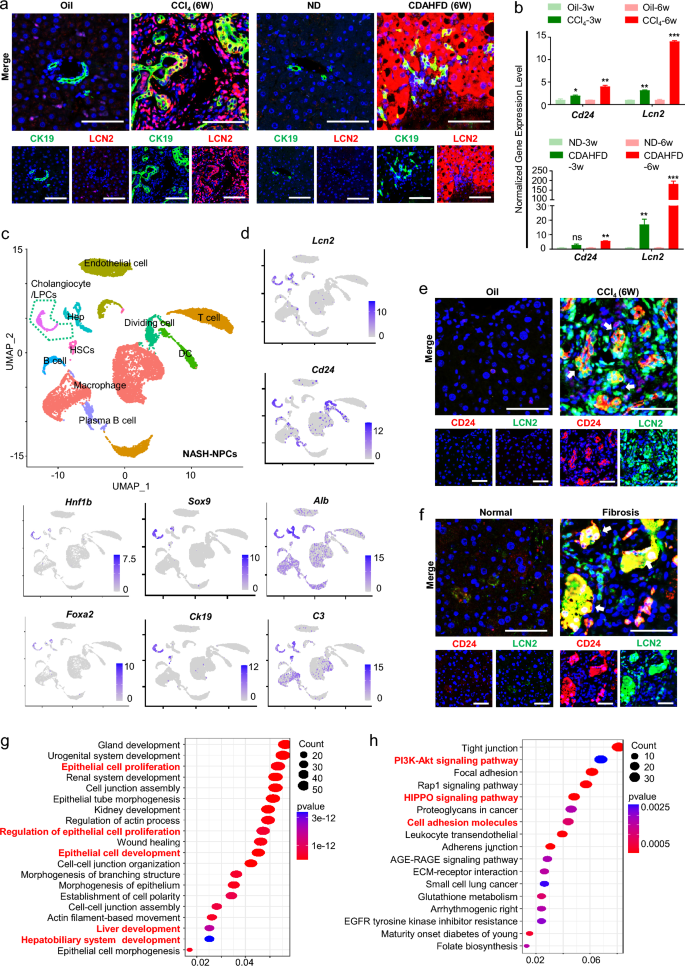
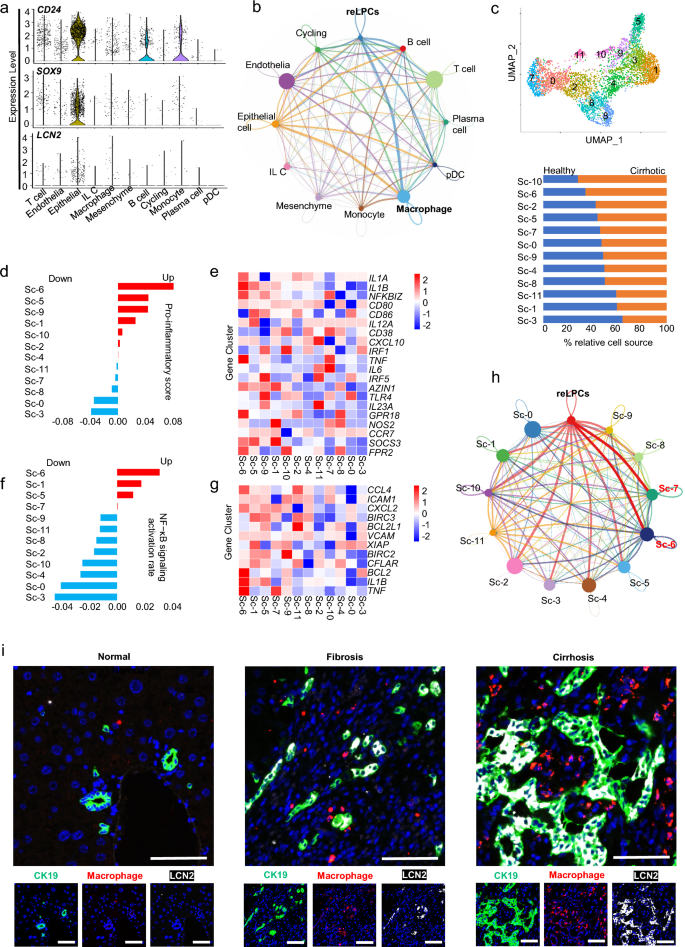
实验目的为筛选驻留LPCs来源LPCs的特异性标志物,并验证其在体内慢性肝损伤模型中的存在与分布。方法细节上,通过转录组差异分析筛选三种LPCs的特异性基因,利用GO、KEGG分析其功能通路;通过STRING数据库构建LCN2的蛋白互作网络,分析其功能关联;比较体外培养LPCs与体内胆管反应细胞的基因表达谱,验证体外细胞与体内细胞的一致性;通过单细胞RNA测序分析NASH模型小鼠肝脏非实质细胞的基因表达,结合免疫荧光染色,在CCl₄诱导的肝纤维化模型、CDAHFD诱导的NASH模型及人肝纤维化组织中检测CD24与LCN2的表达。
结果解读显示,转录组分析发现驻留LPCs来源的LPCs高表达Lcn2基因,GO分析显示其基因富集于先天免疫、炎症反应等通路;STRING分析显示LCN2与多个免疫炎症相关基因存在互作;基因表达谱比较显示,体外培养的CD24⁺LCN2⁺LPCs与体内胆管反应中的CD24⁺LPCs基因表达谱高度相似;单细胞测序与免疫荧光染色显示,在慢性肝损伤模型小鼠的胆管反应区域及人肝纤维化组织中,均存在大量CD24⁺LCN2⁺LPCs,且其数量随肝损伤程度加重而增加。
产品关联:文献未提及具体实验产品,领域常规使用单细胞测序平台、免疫荧光染色试剂盒、生物信息学分析软件(Seurat、CellChat、STRING)等。
3.4 CD24⁺LCN2⁺肝脏祖细胞对巨噬细胞炎症反应的调控作用
实验目的为探讨CD24⁺LCN2⁺LPCs在慢性肝损伤中对巨噬细胞的调控作用及分子机制。方法细节上,将GFP/荧光素酶标记的CD24⁺LCN2⁺LPCs移植到CCl₄处理的小鼠体内,通过血清生化检测(ALT、AST)、组织染色(H&E、Sirius Red)、免疫荧光染色(α-SMA、CK19、F4/80)评估肝损伤与纤维化程度;通过CellChat工具分析单细胞测序数据中CD24⁺LCN2⁺LPCs与其他细胞的互作网络;通过Transwell实验检测LPCs条件培养基对骨髓来源巨噬细胞(BMDMs)的趋化作用;通过条件培养基培养BMDMs,实时荧光定量PCR检测M1、M2巨噬细胞标志物的表达;通过沉默Lcn2基因,验证LCN2在调控巨噬细胞反应中的作用。
结果解读显示,移植CD24⁺LCN2⁺LPCs后,小鼠血清ALT、AST水平显著升高(n=3,P<0.001),肝纤维化面积增加(n=3,P<0.001),F4/80⁺巨噬细胞浸润明显增多;CellChat分析显示CD24⁺LCN2⁺LPCs与M1巨噬细胞的互作强度最高;Transwell实验显示CD24⁺LCN2⁺LPCs的条件培养基对BMDMs的趋化作用显著强于对照组(n=3,P<0.01);BMDMs在CD24⁺LCN2⁺LPCs条件培养基中培养后,M1标志物IL-1b、IL-6、iNOS的表达水平显著升高(n=3,P<0.001);沉默Lcn2基因后,CD24⁺LCN2⁺LPCs对BMDMs的趋化作用及M1极化诱导作用均显著减弱(n=3,P<0.05)。
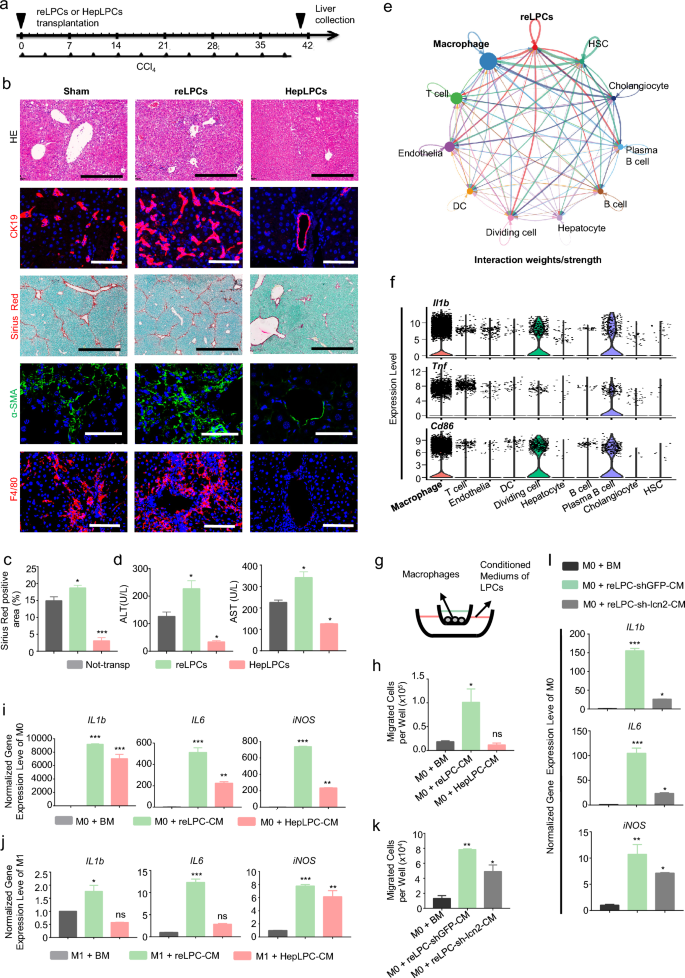
产品关联:文献未提及具体实验产品,领域常规使用慢病毒载体(基因沉默)、Transwell小室、实时荧光定量PCR试剂盒、血清生化检测试剂盒等。
4. Biomarker研究及发现成果解析
本研究鉴定的核心Biomarker为CD24⁺LCN2⁺肝脏祖细胞(LPCs),属于细胞型Biomarker,其筛选与验证逻辑为:通过体外转录组差异分析筛选驻留LPCs来源LPCs的特异性标志物LCN2,结合已知的LPCs标志物CD24,通过单细胞RNA测序在体内模型中验证其表达,最终在人肝纤维化组织中确认其临床相关性,形成“体外筛选→体内模型验证→临床样本确认”的完整逻辑链条。
Biomarker的来源为慢性肝损伤模型小鼠的肝脏组织及人肝纤维化、肝硬化患者的肝组织,验证方法包括单细胞RNA测序检测基因表达、免疫荧光染色检测蛋白表达、实时荧光定量PCR检测mRNA表达水平。特异性方面,CD24⁺LCN2⁺LPCs仅在慢性肝损伤的胆管反应区域大量存在,正常肝组织中几乎检测不到;敏感性方面,其数量随肝损伤程度加重而显著增加,在NASH模型中的表达水平高于CCl₄诱导的肝纤维化模型(文献未提供ROC曲线数据,基于图表趋势推测)。
核心成果提炼显示,CD24⁺LCN2⁺LPCs的功能关联为:通过分泌LCN2,趋化巨噬细胞并诱导M1极化,进而加重肝脏炎症与纤维化,在CCl₄诱导的肝纤维化模型中,移植CD24⁺LCN2⁺LPCs后,肝纤维化面积显著增加(n=3,P<0.001),血清ALT水平显著升高(n=3,P<0.001)。其创新性在于,首次发现CD24⁺LCN2⁺LPCs是慢性肝损伤中胆管反应的主要细胞亚群之一,首次揭示其通过LCN2介导巨噬细胞炎症反应的分子机制,为慢性肝病的治疗提供了新的潜在靶点,同时LCN2也可作为慢性肝损伤炎症程度的潜在分子标志物。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。