Thymidine kinase 1 through the ages: a comprehensive review
胸苷激酶1的历史:全面综述
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2020 | 起止号: | 2020 Nov 27;10(1):138 |
| doi: | 10.1186/s13578-020-00493-1 | 研究方向: | 信号转导 |
文献解析
1. 领域背景与文献引入
文献英文标题:Thymidine kinase 1 through the ages: a comprehensive review;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肿瘤生物标志物与细胞增殖调控
细胞增殖标志物是肿瘤诊断、预后评估及治疗监测的核心工具,传统标志物如增殖细胞核抗原(PCNA)、Ki-67虽已广泛应用,但存在表达稳定性不足、检测标准化程度低等局限性。胸苷激酶1(TK1)作为DNA补救途径的关键酶,参与胸腺核苷的磷酸化以支持DNA合成与损伤修复,早在20世纪60年代就被发现其在肿瘤组织中活性异常升高,后续研究证实血清TK1水平与肿瘤分期、预后密切相关,且其在S期的表达峰值更能精准反映肿瘤细胞的DNA合成速率,具有优于传统标志物的应用潜力。然而,现有研究多聚焦于TK1的临床检测方法,对其从DNA到蛋白水平的全层面调控机制、在肿瘤发病机制中的直接作用探讨不足,缺乏系统性综述整合这些核心内容。本综述旨在填补这一空白,全面梳理TK1的发现历史、分子调控机制、临床应用价值及最新肿瘤发病机制研究,为其作为生物标志物与治疗靶点的转化应用提供理论支撑。
2. 文献综述解析
本综述以TK1的研究历程为时间轴,以分子调控机制、临床应用、肿瘤发病机制为核心维度,系统整合了近60年的研究成果,重点突出了TK1在肿瘤领域的前沿进展,弥补了以往综述侧重检测方法、缺乏机制整合的局限性。
作者将现有研究分为三个核心方向:一是TK1的基础生物学研究,涵盖发现历史、分子特征、细胞周期调控;二是TK1的临床应用研究,包括血清检测方法、作为肿瘤生物标志物的诊断与预后价值;三是TK1在肿瘤发病机制中的作用研究,涉及最新细胞实验与生物信息学分析。现有研究的关键结论显示,TK1在S期表达峰值,活性与细胞增殖高度相关;血清TK1水平在肺癌、乳腺癌、前列腺癌等多种肿瘤中显著升高,与肿瘤分期、不良预后呈正相关;现有检测方法分为基于酶活性的检测(如TK-REA、DiviTum assay)和基于蛋白的免疫检测(如ECL dot blot、AroCell TK-210 ELISA)两类,各有优劣。但现有研究存在明显局限性:以往综述多聚焦临床检测方法,对TK1的全层面调控机制缺乏系统梳理;对TK1在肿瘤发病机制中的直接作用研究较少,多停留在生物标志物层面;临床应用缺乏标准化检测方法,限制了其广泛推广。
本综述的创新价值在于,首次全面整合了TK1的发现历史、从DNA到蛋白的全层面调控机制、肿瘤发病机制的最新研究成果,同时系统总结了其作为生物标志物的检测方法与治疗靶点潜力,构建了完整的TK1知识体系,填补了以往综述的核心空白,为后续基础研究与临床转化提供了清晰的方向。
3. 研究思路总结与详细解析
本综述采用系统性文献回顾方法,以TK1的研究进展为主线,从发现历史、分子调控机制、临床检测方法到肿瘤发病机制新发现逐步深入,构建了涵盖基础到临床的完整知识框架,为TK1的进一步研究与应用提供了全面参考。
3.1 TK1的发现与分子特征解析
实验目的:梳理TK1的发现历程,明确其与同工酶TK2的分子特征差异,为后续机制研究奠定基础。
方法细节:作者整合了1960年代至今的经典生化纯化实验、染色体定位分析、细胞周期表达研究等文献,系统对比TK1与TK2的分子特征。
结果解读:20世纪60年代首次鉴定出催化胸腺核苷磷酸化的酶,后续研究发现两种同工酶TK1与TK2:TK1定位于17号染色体(17q25.3),在细胞质中表达,且表达受细胞周期调控,S期达到活性峰值;TK2定位于16号染色体(16q21),在线粒体中表达,不受细胞周期调控。TK1的晶体结构为四聚体,包含α/β结构域与锌结合结构域,关键活性位点包括Glu98、Phe128、Tyr181等,负责胸腺核苷的结合与磷酸化。作者通过时间线图直观展示了TK1的重要发现节点。
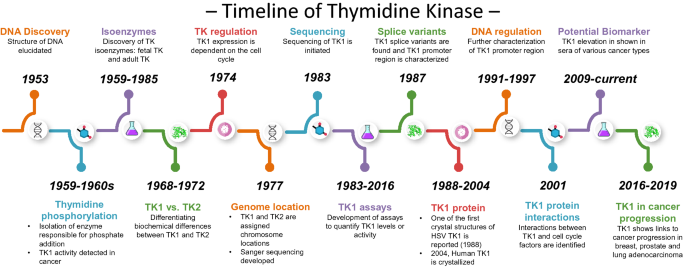
产品关联:文献未提及具体实验产品,领域常规使用蛋白纯化试剂盒、染色体荧光原位杂交(FISH)试剂盒、细胞周期分析流式细胞仪等。
3.2 TK1的多层面调控机制解析
实验目的:系统梳理TK1从DNA、mRNA到蛋白水平的调控网络,明确其细胞周期特异性表达的分子基础。
方法细节:作者整合了基因测序、启动子活性分析、转录因子调控研究、蛋白翻译后修饰研究等多方面文献,全面解析TK1的调控机制。
结果解读:在DNA水平,TK1基因启动子区域包含TATAA、CCAAT、G-C元件,其中反向CCAAT重复序列是转录因子CP1的结合位点,调控S期的转录激活;同时p53-DREAM通路可通过结合TK1启动子的E2F位点抑制其转录。在mRNA水平,TK1的表达受Rb-E2F通路调控,G1/S期转换时Rb磷酸化释放E2F,激活TK1转录。在蛋白水平,TK1的C末端40个氨基酸序列在S期稳定蛋白,在G2/M期通过泛素-蛋白酶体途径降解;癌症细胞中C末端的突变或缺失会导致TK1失去细胞周期调控,持续表达并保持酶活性。作者通过转录本变体图展示了TK1的5种蛋白编码剪接体,通过启动子调控区域图展示了关键转录调控元件。
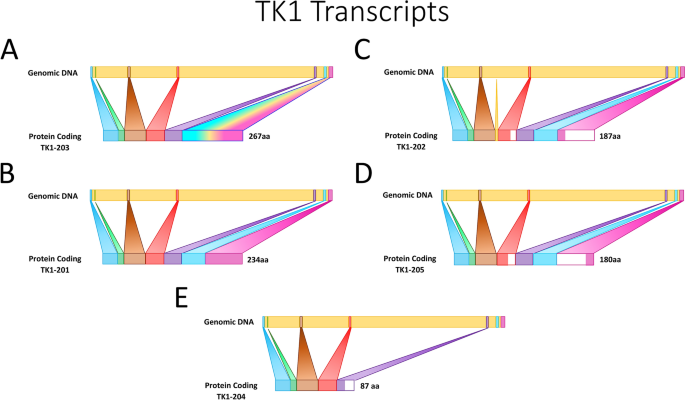
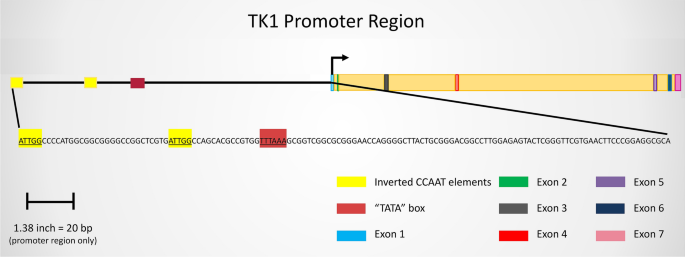
产品关联:文献未提及具体实验产品,领域常规使用基因克隆试剂盒、荧光素酶报告基因检测系统、蛋白免疫印迹(Western blot)试剂盒等。
3.3 TK1作为肿瘤生物标志物的检测方法解析
实验目的:系统总结现有TK1血清检测方法的原理、优缺点及临床应用现状,为标准化检测方法开发提供参考。
方法细节:作者分类整理了基于酶活性与基于蛋白的两类检测方法的相关文献,对比各方法的检测原理、灵敏度、特异性与临床应用场景。
结果解读:基于酶活性的检测方法直接反映TK1的功能活性,如[³H]-脱氧胸腺核苷磷酸化 assay曾被视为“金标准”,但因使用放射性标记限制临床应用;TK-Liaison assay(Diasorin®)与DiviTum™ assay(Biovica®)为非放射性方法,适用于批量检测,但检测的是总TK活性(含TK1与TK2)。基于蛋白的免疫检测方法直接检测TK1蛋白水平,如基于鸡IgY抗体的ECL dot blot可检测到0.1pg的TK1蛋白,AroCell TK-210 ELISA(AroCell®)可特异性检测血清中的TK1蛋白,避免TK2干扰,但部分方法存在检测结果重叠问题,如ECL dot blot在部分健康人群与术前患者中结果难以区分。目前TK1检测缺乏标准化方法,不同方法结果难以比较,限制了其临床广泛应用。
产品关联:实验所用关键产品:Diasorin®的TK-Liaison assay、Biovica®的DiviTum™ assay、AroCell®的TK-210 ELISA、基于鸡IgY抗体的ECL dot blot检测系统。
3.4 TK1在肿瘤发病机制中的新发现解析
实验目的:梳理TK1在肿瘤发病机制中的直接作用研究,探讨其作为治疗靶点的潜力。
方法细节:作者整合了最新的细胞实验(shRNA/siRNA敲低)、动物实验与生物信息学研究文献,分析TK1在肿瘤增殖、侵袭、转移中的作用机制。
结果解读:最新研究证实TK1不仅是肿瘤增殖的生物标志物,还直接参与肿瘤发病机制:在肺腺癌中,敲低TK1可通过降低GDF15表达抑制肿瘤生长与转移;在乳腺癌中,TK1是网络调控的关键节点,敲低TK1可抑制肿瘤细胞的增殖、侵袭与迁移;在甲状腺癌中,TK1通过调控上皮间质转化(EMT)标志物(波形蛋白、N-钙粘蛋白)促进肿瘤侵袭,且miR-34a-5p可靶向抑制TK1表达。生物信息学研究显示,TK1是肾上腺皮质癌与前列腺癌的枢纽基因,与肿瘤预后不良相关。这些研究表明TK1具有作为肿瘤治疗靶点的潜力,为后续药物开发提供了理论基础。
产品关联:文献未提及具体实验产品,领域常规使用shRNA/siRNA转染试剂盒、裸鼠肿瘤模型构建工具、生物信息学分析平台(如GEO、TIMER)等。
4. Biomarker研究及发现成果解析
核心信息段
本综述系统总结了TK1作为肿瘤生物标志物的研究成果,明确了其早期诊断、预后评估、治疗监测的核心价值,同时梳理了其在肿瘤发病机制中的直接作用,为其从生物标志物向治疗靶点的转化提供了关键依据。
Biomarker定位:TK1是细胞增殖相关的肿瘤生物标志物,其筛选逻辑始于1960年代发现的肿瘤组织TK1活性升高,后续通过临床样本验证血清TK1水平与肿瘤分期、预后的关联,再通过大规模临床研究验证其诊断与预后价值,最新研究进一步揭示了其在肿瘤发病机制中的直接调控作用,拓展了其作为治疗靶点的潜力。
研究过程详述:TK1的样本来源包括肿瘤组织、血清、胸腔积液等;验证方法涵盖免疫组化(检测肿瘤组织TK1表达)、血清酶活性检测、血清蛋白免疫检测等;特异性与敏感性方面,在乳腺癌中,癌前病变(如硬化性腺病)中TK1阳性率已升高,提示其可作为早期诊断标志物;在前列腺癌中,血清TK1水平与Gleason评分相关,而传统标志物PSA无此相关性;在恶性胸腔积液中,TK1的诊断准确性高于神经元特异性烯醇化酶(NSE)、癌胚抗原(CEA)、细胞角蛋白片段19(CYFRA21-1)等标志物(文献未明确提供AUC数值,基于图表趋势推测);在慢性淋巴细胞白血病中,血清TK1水平≥10 U/L的患者对联合治疗的应答率仅45%,而<10 U/L的患者应答率达83%(n=188,P<0.05)。
核心成果提炼:TK1是肿瘤发生的早期事件标志物,血清水平与肿瘤分期、不良预后呈正相关,可用于治疗监测(如肺癌化疗后TK1升高提示治疗失败);与其他标志物联合使用可显著提高诊断准确性;最新研究发现TK1直接参与肿瘤增殖、侵袭、转移的调控机制,具有作为治疗靶点的潜力;统计学结果显示,慢性淋巴细胞白血病中高TK1水平患者应答率显著低于低水平患者(n=188,P<0.05),乳腺癌癌前病变中硬化性腺病样本TK1阳性率升高(文献未明确样本量与P值),肺癌化疗后TK1升高与治疗失败相关(文献未明确样本量与P值)。推测:TK1作为治疗靶点的研究有望为肿瘤精准治疗提供新方向,需进一步的体内实验与临床试验验证其有效性与安全性。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。