Role of extracellular vesicle-associated proteins in the progression, diagnosis, and treatment of hepatocellular carcinoma
细胞外囊泡相关蛋白在肝细胞癌的进展、诊断和治疗中的作用
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2024 | 起止号: | 2024 Sep 3;14(1):113 |
| doi: | 10.1186/s13578-024-01294-6 | 研究方向: | 细胞生物学、肿瘤 |
文献解析
1. 领域背景与文献引入
文献英文标题:Role of extracellular vesicle-associated proteins in the progression, diagnosis, and treatment of hepatocellular carcinoma;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:肿瘤学-肝细胞癌-细胞外囊泡生物学
2020年全球原发性肝癌居恶性肿瘤发病率第6位、死亡率第3位,其中肝细胞癌(HCC)占75%-85%,其起病隐匿,超50%患者确诊时已达晚期,错失手术根治机会。领域共识:当前肝细胞癌治疗面临异质性高、术后复发率高、早期诊断标志物敏感性不足(如甲胎蛋白AFP敏感性仅25%-65%)、晚期靶向治疗选择有限等核心问题。细胞外囊泡(EVs)作为细胞来源的脂质双层膜结构囊泡,可携带蛋白质、核酸等 cargo 介导细胞间通讯,在肿瘤微环境(TME)调控、转移、耐药等过程中发挥关键作用,成为肝癌研究热点,但EV相关蛋白在肝癌发生发展、诊断治疗中的具体作用及机制仍需系统梳理,这也是本文的研究初衷——全面总结EV相关蛋白在肝癌中的功能、作为生物标志物的潜力及治疗应用前景,为肝癌研究提供新的视角和方向。
2. 文献综述解析
作者对领域现有研究的分类维度为:EV的生物发生与特征、EV相关蛋白在肝癌进展(包括肿瘤微环境交互、血管生成、转移)中的作用、EV相关蛋白作为诊断生物标志物的研究、EV相关蛋白在肝癌治疗中的应用四个核心方向。
现有研究的关键结论显示,EV可通过携带不同蛋白双向调控肝癌细胞增殖,同时在免疫微环境重塑、血管生成及转移过程中发挥核心介导作用;EV相关蛋白具有作为肝癌诊断生物标志物的潜力,部分标志物的诊断效能优于传统标志物AFP;EV可通过工程化改造实现靶向药物递送,或直接携带功能性蛋白发挥抗肿瘤作用。技术方法优势方面,现有研究整合了蛋白质组学、细胞共培养、动物模型及临床样本验证等多种技术,部分研究采用多组学联合分析提升结果可靠性;局限性主要体现在多数治疗相关研究处于细胞或动物实验阶段,缺乏大规模临床验证,且EV分离纯化技术尚未标准化,不同研究结果可比性不足,部分蛋白的功能机制研究不够深入,缺乏上下游通路的系统验证。
本研究的创新价值在于首次系统整合了EV相关蛋白在肝癌进展、诊断、治疗全链条的研究进展,明确了EV相关蛋白在肝癌不同阶段的功能差异,提出了未来研究的关键方向,为领域内后续研究提供了全面的参考框架,弥补了现有综述缺乏系统性整合的空白,同时为肝癌的早期诊断和精准治疗提供了新的思路。
3. 研究思路总结与详细解析
整体框架概括:本研究的核心目标是全面阐述EV相关蛋白在肝细胞癌发生发展、诊断及治疗中的作用,核心科学问题聚焦于EV相关蛋白如何调控肝癌细胞与肿瘤微环境的交互、影响肝癌进展,以及其作为生物标志物和治疗靶点的可行性,技术路线采用“EV基础生物学概述→EV相关蛋白在肝癌进展中的功能解析→EV相关蛋白作为诊断标志物的研究总结→EV相关蛋白在治疗中的应用前景→未来研究方向展望”的递进式逻辑框架。
3.1 细胞外囊泡基础生物学特征解析
实验目的:明确EV的分类、生物发生过程及鉴定方法,为后续功能研究奠定基础。
方法细节:综述了EV的分类(小EVs、大EVs、外泌体等),重点阐述了外泌体的生物发生过程,包括内体形成、多泡体(MVB)生成及分泌的ESCRT依赖和非依赖途径;鉴定方法包括透射电子显微镜(TEM)观察形态、纳米颗粒跟踪分析(NTA)检测粒径和浓度,以及CD9、CD63、CD81等四跨膜蛋白的免疫标记。
结果解读:EV的生物发生存在两种主要途径,ESCRT依赖途径通过ESCRT-0至ESCRT-III等一系列复合物介导泛素化蛋白分选,非依赖途径依赖神经酰胺、LBPA等脂质分子;TEM可观察到EV的杯状脂质双层结构,NTA可定量分析EV的粒径分布,四跨膜蛋白是EV的常用标记物但不具有亚型特异性。
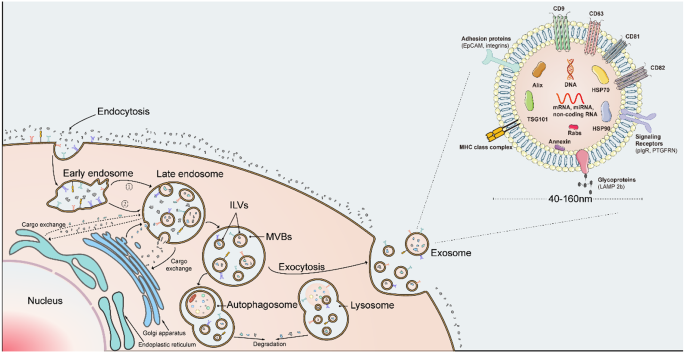
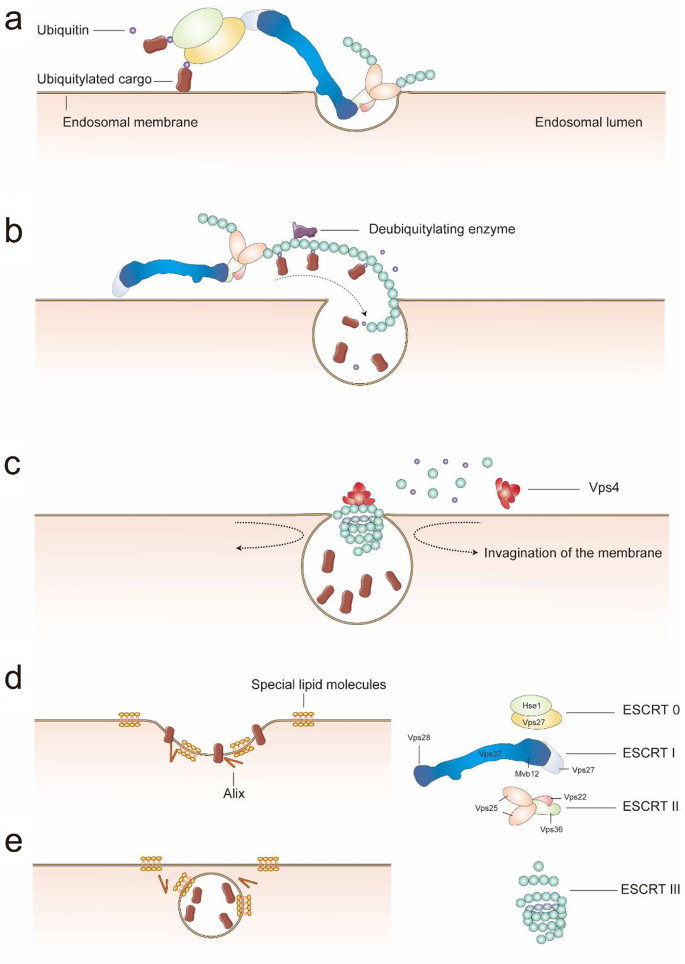
产品关联:文献未提及具体实验产品,领域常规使用透射电子显微镜、纳米颗粒跟踪分析仪,以及CD9、CD63、CD81等抗体进行EV鉴定。
3.2 EV相关蛋白在肝癌进展中的功能解析
实验目的:系统梳理EV相关蛋白在肝癌细胞增殖、肿瘤微环境交互、血管生成、转移中的作用。
方法细节:整合了大量细胞实验、动物模型及临床样本研究,按功能分为肿瘤增殖调控、免疫微环境调控、血管生成调控、转移调控四个方向。
结果解读:EV相关蛋白具有双向调控肝癌增殖的作用,如EV携带的cathelicidin抗菌肽(CAMP)可抑制细胞增殖,而 sonic hedgehog(SHH)可促进肝癌进展及癌干细胞形成;在免疫微环境中,EV相关蛋白可调控巨噬细胞极化(如ALKBH5促进M2极化,FTCD促进M1极化)、NK细胞功能、T细胞耗竭及Breg细胞积累;血管生成方面,CLTA、DDX55等EV相关蛋白可促进血管内皮细胞增殖及管形成,而CLEC3B可抑制血管生成;转移过程中,EV相关蛋白可通过诱导上皮间质转化(EMT)、增强肿瘤干细胞特性、形成预转移微环境等促进肝癌转移,如pIgR可激活Akt/β-catenin轴增强癌干细胞特性,NID1可促进肺预转移微环境形成。
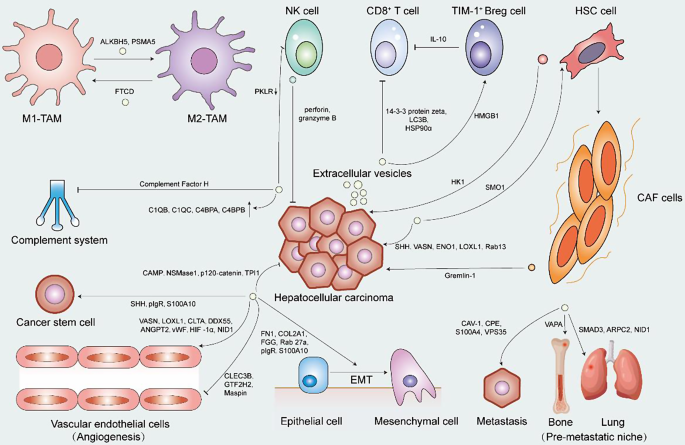
产品关联:文献未提及具体实验产品,领域常规使用细胞共培养模型、免疫组化(IHC)、蛋白质印迹法(WB)等技术检测蛋白表达及功能。
3.3 EV相关蛋白作为肝癌诊断生物标志物的研究解析
实验目的:总结EV相关蛋白作为肝癌诊断、预后及治疗反应预测标志物的研究进展。
方法细节:整合了血清、尿液等体液EV蛋白的检测研究,包括单标志物、联合标志物及EV亚群评分的诊断效能分析。
结果解读:EV相关蛋白GPC-3在区分肝癌与肝硬化患者中的效能优于AFP;AnnexinV+EpCAM+ASGPR1+ EVs区分肝癌与肝硬化的曲线下面积(AUC)为0.732;HSP90α+LC3B+ EVs区分肝癌与非肝癌对照的AUC为0.960;基于三种EV亚群的ECG评分在验证队列中区分早期肝癌与肝硬化的AUC达0.93;CCT8和cofilin-1联合AFP的AUC达0.84,优于单独AFP;部分EV相关蛋白可预测治疗反应,如高EV-GPX3/ACTR3、低EV-ARHGAP1B与SIRT联合索拉非尼治疗的高疗效相关(AUC=1)。
产品关联:文献未提及具体实验产品,领域常规使用荧光纳米颗粒跟踪分析(F-NTA)、流式细胞术(FACS)、蛋白质组学等技术检测EV蛋白标志物。
3.4 EV相关蛋白在肝癌治疗中的应用解析
实验目的:探讨EV相关蛋白在肝癌治疗中的潜力,包括药物递送载体、肿瘤疫苗、直接抗肿瘤作用等。
方法细节:整合了EV工程化改造、CRISPR-Cas9递送、肿瘤疫苗开发等研究。
结果解读:通过工程化改造EV表面蛋白(如LAMP2B、CD47)可实现靶向药物递送,增强索拉非尼诱导的铁死亡或光动力-化疗联合治疗的疗效;EV可作为CRISPR-Cas9核糖核蛋白(RNP)的递送载体,靶向编辑KAT5基因抑制肝癌生长;EV相关蛋白可用于开发肿瘤疫苗,如HMGN1修饰的EV可激活树突状细胞(DC),诱导抗肿瘤免疫反应;EV携带的TRAIL可与索拉非尼协同诱导肝癌细胞凋亡。
产品关联:文献未提及具体实验产品,领域常规使用基因转染、电穿孔等技术工程化改造EV,使用细胞培养、动物模型验证治疗效果。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究涉及的Biomarker类型包括EV膜蛋白(如GPC-3、EpCAM、ASGPR1、LC3B)、EV cargo蛋白(如CCT8、cofilin-1、HSP90α)、EV亚群组合标志物(ECG评分);筛选/验证逻辑为:细胞系蛋白质组学筛选→临床样本验证(血清、尿液)→诊断效能分析(AUC、敏感性、特异性),部分标志物还进行了治疗反应预测的验证。
研究过程详述:Biomarker来源包括肝癌细胞系EV、患者血清/尿液EV;验证方法包括荧光纳米颗粒跟踪分析、流式细胞术、蛋白质组学、组织芯片等;特异性与敏感性数据方面,GPC-3在区分肝癌与肝硬化患者中效能优于AFP;HSP90α+LC3B+ EVs区分肝癌与非肝癌对照的AUC为0.960;ECG评分区分早期肝癌与肝硬化的AUC达0.93;CCT8和cofilin-1联合AFP的AUC达0.84;高EV-GPX3/ACTR3、低EV-ARHGAP1B预测SIRT联合索拉非尼疗效的AUC=1。
核心成果提炼:EV相关蛋白作为肝癌生物标志物具有稳定性高、特异性强的优势,部分标志物的诊断效能优于传统标志物AFP,可用于早期诊断、预后评估及治疗反应预测;创新性在于首次系统总结了EV相关蛋白在肝癌诊断中的应用,提出了EV亚群组合评分的诊断策略,为肝癌的非侵入性诊断提供了新的方向;目前多数标志物的临床验证仍需大规模队列研究支持,部分标志物的特异性及敏感性需进一步优化,推测:未来结合多组学技术的EV标志物筛选将成为肝癌早期诊断的重要方向。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。