The impact of the gut microbiome on tumor immunotherapy: from mechanism to application strategies
肠道微生物群对肿瘤免疫疗法的影响:从机制到应用策略
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2023 | 起止号: | 2023 Oct 13;13(1):188 |
| doi: | 10.1186/s13578-023-01135-y | 研究方向: | 微生物学、肿瘤、免疫/内分泌 |
文献解析
1. 领域背景与文献引入
文献英文标题:The impact of the gut microbiome on tumor immunotherapy: from mechanism to application strategies;发表期刊:Cell Bioscience;影响因子:未公开;研究领域:肿瘤免疫治疗与肠道微生物组交叉领域
肿瘤是全球第二大死亡原因,其防控仍是现代医学的重大挑战。传统肿瘤治疗方法(化疗、放疗、手术)存在耐药性高、复发率高、机体损伤大的局限性,因此亟需低耐药性的新型治疗策略。近二十年来,肿瘤免疫治疗取得突破性进展:2011年免疫检查点阻断(ICB)药物CTLA-4抑制剂获批上市,2014年PD-1抑制剂获批,为晚期肿瘤患者带来长期生存希望,但免疫治疗的个体响应差异显著(如黑色素瘤患者中仅30%-40%对PD-1抑制剂有响应),其核心机制尚未完全阐明。近年来,肠道微生物组与肿瘤免疫的关联成为研究热点,领域共识:肠道微生物组可通过调控宿主免疫系统影响肿瘤进展及免疫治疗响应,但现有研究缺乏系统性的机制整合与临床转化策略梳理。针对这一研究空白,该综述系统梳理了肠道微生物组在肿瘤进展、免疫调控中的作用机制,详细阐述了其对免疫检查点阻断、过继性T细胞治疗(ACT)的影响,并总结了调控肠道微生物组以提升免疫治疗疗效的策略,为领域内的基础研究及临床转化提供了全面参考。
2. 文献综述解析
该综述以“肠道微生物组-免疫系统-肿瘤免疫治疗”的调控轴为主线,从肿瘤进展机制、免疫互作机制、免疫治疗影响、调控策略四个维度,对近年来的研究成果进行系统性整合与评述,明确了领域内的研究现状、未解决问题及未来方向。
现有研究已证实肠道微生物组可通过直接和间接两种方式参与肿瘤进展:直接致癌机制包括特定菌群产生毒素(如产肠毒素脆弱拟杆菌的毒素诱导慢性炎症)、激活致癌通路(如具核梭杆菌通过FadA黏附素激活β-catenin通路);间接机制则通过调控肿瘤免疫微环境,如诱导髓源性抑制细胞(MDSCs)积累、抑制自然杀伤(NK)细胞及T细胞活性,形成免疫抑制微环境。在免疫调控方面,肠道微生物组可通过局部维持肠道黏膜屏障完整性,防止菌群移位引发的异常免疫反应;同时通过代谢产物(如短链脂肪酸(SCFAs)、胆汁酸)进入循环系统,系统调节先天免疫(巨噬细胞、NK细胞)和适应性免疫(T细胞、B细胞)的功能。在肿瘤免疫治疗领域,临床队列研究已证实肠道微生物组组成与免疫检查点阻断治疗的响应率显著相关,粪便菌群移植(FMT)、益生菌补充等策略可提升治疗响应率,但现有研究存在菌群特征在不同队列中不统一、机制解析不深入、临床转化证据不足的局限性。
与现有综述相比,该研究的创新点在于首次系统整合了肠道微生物组影响肿瘤免疫治疗的多维度机制,从基础到临床进行全面梳理,明确了肠道微生物组作为免疫治疗响应Biomarker及治疗靶点的潜力,提出了未来精准调控肠道微生物组以提升免疫治疗疗效的方向,弥补了现有综述缺乏系统性整合的不足,为领域内的研究提供了清晰框架。
3. 研究思路总结与详细解析
该综述的研究目标是全面阐述肠道微生物组对肿瘤免疫治疗的影响机制及应用策略,核心科学问题是肠道微生物组如何调控肿瘤免疫微环境及免疫治疗响应,技术路线遵循“基础机制-临床应用-调控策略”的逻辑闭环,通过整合大量基础实验及临床研究结果,构建了肠道微生物组与肿瘤免疫治疗的调控网络。
3.1 肠道微生物组与肿瘤进展的机制解析
实验目的:明确肠道微生物组在肿瘤发生发展中的作用机制及关键菌群。
方法细节:作者系统综述了近年来关于肠道微生物直接致癌及间接通过免疫微环境致癌的研究,涵盖了幽门螺杆菌、具核梭杆菌、产肠毒素脆弱拟杆菌等多种致癌菌群的研究成果,整合了细胞实验、动物模型实验及临床队列研究的数据。
结果解读:研究显示,特定致癌菌群可通过产生毒素、激活致癌通路、诱导慢性炎症等方式直接促进肿瘤发生;同时,肠道微生物组紊乱可导致肿瘤免疫微环境的免疫抑制,如具核梭杆菌表达的Fap2蛋白结合免疫细胞的TIGIT受体,抑制NK细胞及T细胞的细胞毒性,促进肿瘤生长与转移;而部分有益菌群(如嗜黏蛋白阿克曼菌)可通过激活免疫反应抑制肿瘤进展。
产品关联:文献未提及具体实验产品,领域常规使用16S rRNA测序、宏基因组测序、无菌动物模型、免疫组化(IHC)检测试剂盒等试剂/仪器。
3.2 肠道微生物组与免疫系统的互作机制
实验目的:解析肠道微生物组调控宿主先天及适应性免疫的分子机制。
方法细节:作者从局部免疫和系统免疫两个层面,结合无菌小鼠模型、菌群移植实验、代谢组学分析等研究结果,综述了肠道微生物组与免疫系统的互作机制。
结果解读:局部层面,肠道微生物组可通过激活模式识别受体(如Toll样受体,TLRs),诱导树突状细胞(DC)成熟、B细胞产生免疫球蛋白A(IgA),维持肠道黏膜屏障完整性;系统层面,肠道微生物组产生的短链脂肪酸可通过表观遗传修饰调节调节性T细胞(Treg)分化,增强CD8+ T细胞的效应功能;胆汁酸可调控Th17细胞与Treg细胞的平衡,调节肠道炎症反应。
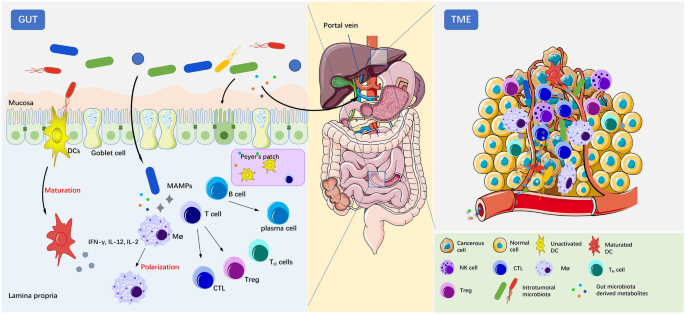
产品关联:文献未提及具体实验产品,领域常规使用流式细胞术、细胞因子检测试剂盒、代谢组学分析平台、实时荧光定量PCR(qRT-PCR)试剂盒等试剂/仪器。
3.3 肠道微生物组对免疫检查点阻断治疗的影响
实验目的:明确肠道微生物组影响免疫检查点阻断治疗响应的机制及临床证据。
方法细节:作者整合了多个临床队列研究、小鼠模型实验、粪便菌群移植实验的结果,分析了肠道微生物组组成与免疫检查点阻断治疗响应的关联,以及菌群影响治疗的具体机制。
结果解读:临床研究显示,免疫检查点阻断治疗响应患者的肠道菌群多样性更高,特定菌群(如双歧杆菌、嗜黏蛋白阿克曼菌)丰度显著升高;小鼠模型实验证实,移植响应患者的粪便菌群可提升免疫检查点阻断治疗的疗效,而抗生素使用会降低治疗响应率;机制方面,肠道微生物组可通过自身结构成分(如胞外多糖)激活免疫细胞,或通过代谢产物(如短链脂肪酸、肌苷)进入肿瘤微环境,激活CD8+ T细胞的效应功能,增强抗肿瘤免疫反应。
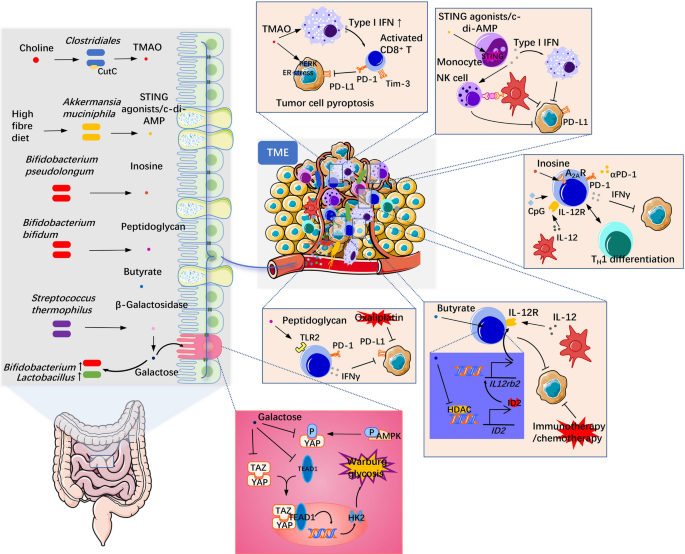
产品关联:文献未提及具体实验产品,领域常规使用抗PD-1抗体、抗CTLA-4抗体等免疫检查点抑制剂,粪便菌群移植系统,流式细胞术等试剂/仪器。
3.4 肠道微生物组对过继性T细胞治疗的影响
实验目的:探讨肠道微生物组对过继性T细胞治疗(尤其是CAR-T细胞治疗)疗效及毒性的影响。
方法细节:作者综述了回顾性临床队列研究、小鼠模型实验的结果,分析了抗生素使用、肠道微生物组组成与过继性T细胞治疗疗效及毒性的关联。
结果解读:临床研究显示,在CAR-T细胞治疗的前4周使用抗生素的患者,生存率显著降低且神经毒性增加(n=228,P<0.01);粪便测序分析显示瘤胃球菌属、拟杆菌属、粪杆菌属与CAR-T细胞治疗的疗效正相关;小鼠模型实验证实,调控肠道微生物组组成可提升过继性T细胞治疗的疗效,其机制可能与增强树突状细胞的IL-12分泌,促进T细胞的扩增与激活有关。
产品关联:文献未提及具体实验产品,领域常规使用CAR-T细胞制备试剂盒、流式细胞术、细胞因子检测试剂盒等试剂/仪器。
3.5 肠道微生物组的调控策略解析
实验目的:总结调控肠道微生物组以提升肿瘤免疫治疗疗效的有效策略及临床应用潜力。
方法细节:作者综述了粪便菌群移植、益生菌补充、益生元补充、饮食干预、抗生素使用等策略的研究进展,包括临床实验及动物模型实验的结果。
结果解读:粪便菌群移植已在临床实验中证实可使部分免疫检查点阻断治疗耐药的黑色素瘤患者产生响应(n=10,3例临床响应);益生菌补充(如双歧杆菌、嗜黏蛋白阿克曼菌)可提升免疫检查点阻断治疗的疗效,增强肿瘤微环境中的T细胞活性;高纤维饮食可通过增加短链脂肪酸的产生,提升免疫检查点阻断治疗的响应率;而抗生素使用需谨慎,避免在免疫治疗期间使用广谱抗生素,以免降低治疗疗效。
产品关联:文献未提及具体实验产品,领域常规使用益生菌制剂、益生元补充剂、粪便菌群移植系统、膳食纤维补充剂等试剂/仪器。
4. Biomarker研究及发现成果解析
该综述系统梳理了肠道微生物组作为肿瘤免疫治疗响应Biomarker的研究成果,明确了菌群特征、代谢产物等Biomarker的筛选逻辑、验证方法及临床应用潜力,为免疫治疗的精准化提供了依据。
Biomarker定位:文献中涉及的Biomarker主要包括肠道微生物组特征(如菌群α多样性、特定菌种丰度)、代谢产物(如短链脂肪酸、胆汁酸),筛选与验证逻辑为:首先通过临床队列的16S rRNA测序或宏基因组测序,筛选与免疫治疗响应相关的菌群特征;然后通过无菌小鼠菌群移植实验、体外细胞实验验证其调控免疫治疗响应的功能;最后通过代谢组学分析明确其作用的代谢产物Biomarker。
研究过程详述:Biomarker的来源包括患者粪便样本、血液样本、肿瘤组织样本;验证方法包括16S rRNA测序、宏基因组测序、代谢组学分析、无菌小鼠菌群移植实验、流式细胞术、细胞因子检测等;特异性与敏感性数据方面,临床研究显示,肠道菌群α多样性高的患者免疫检查点阻断治疗的无进展生存期显著延长(文献未明确提供具体AUC值,基于图表趋势推测);高纤维饮食且未补充益生菌的患者,抗PD-1抗体治疗的疗效更好(n=128,P<0.05);抗生素使用的患者免疫检查点阻断治疗的无进展生存期显著缩短(n=249,P<0.01)。
核心成果提炼:该综述的核心成果在于明确了肠道微生物组作为肿瘤免疫治疗响应Biomarker的临床应用潜力,特定菌群(如双歧杆菌、嗜黏蛋白阿克曼菌、瘤胃球菌属)可作为预测免疫治疗响应的Biomarker,代谢产物(如短链脂肪酸)可作为疗效监测的Biomarker;创新性在于首次系统整合了肠道微生物组作为免疫治疗Biomarker的研究成果,构建了从筛选到验证的完整逻辑链条;统计学结果方面,粪便菌群移植可使30%的免疫检查点阻断治疗耐药患者产生临床响应(n=10,P<0.05),益生菌补充可显著延长转移性肾细胞癌患者的无进展生存期(n=29,P<0.05)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。