Roles of bile acids signaling in neuromodulation under physiological and pathological conditions
胆汁酸信号在生理和病理条件下神经调控中的作用
| 期刊: | Cell and Bioscience | 影响因子: | 6.200 |
| 时间: | 2023 | 起止号: | 2023 Jun 12;13(1):106 |
| doi: | 10.1186/s13578-023-01053-z | 研究方向: | 信号转导 |
文献解析
1. 领域背景与文献引入
文献英文标题:Roles of bile acids signaling in neuromodulation under physiological and pathological conditions;发表期刊:Cell & Bioscience;影响因子:未公开;研究领域:神经科学-胆汁酸神经调节与神经退行性疾病
领域共识:胆汁酸是胆固醇代谢产生的经典消化相关分子,传统认知中主要通过肠肝循环参与营养吸收与外周代谢稳态调控。近年来随着神经代谢与肠-脑轴研究的兴起,胆汁酸跨血脑屏障(BBB)进入中枢神经系统(CNS)的现象逐渐受到关注,成为神经科学与代谢交叉领域的研究热点。领域发展关键节点包括:2000年后发现脑内存在独立的胆汁酸合成通路(CYP46A1介导胆固醇代谢),2010年后陆续揭示胆汁酸通过激活核受体、膜受体调节神经功能,2020年后聚焦于胆汁酸在神经退行性疾病中的致病与保护作用。当前研究热点包括胆汁酸-肠-脑轴的调控机制、不同胆汁酸亚型的特异性神经效应、胆汁酸作为神经疾病Biomarker与治疗靶点的潜力。未解决的核心问题包括:脑内胆汁酸合成的细胞特异性调控机制、不同胆汁酸亚型跨BBB的转运特异性、间接信号通路在脑内的具体功能效应、胆汁酸Biomarker的大规模临床验证不足。这篇综述旨在系统整合近年来胆汁酸代谢、脑-外周对话、神经功能的研究成果,明确胆汁酸信号在脑内生理病理条件下的核心作用,为神经疾病的机制研究与治疗策略提供全景式参考。
2. 文献综述解析
作者以胆汁酸的“代谢-信号-功能”逻辑为核心分类维度,系统梳理了生理状态下胆汁酸的脑内外代谢与信号通路,以及病理状态下胆汁酸作为致病因子或神经保护因子的作用机制,同时整合了临床样本与基础实验的多维度研究证据。
现有研究的关键结论包括:生理状态下胆汁酸不仅通过肠肝循环维持外周代谢稳态,还可通过被动扩散或转运体跨BBB进入脑内,直接激活核受体(法尼醇X受体FXR)、膜受体(G蛋白偶联胆汁酸受体TGR5),或调节N-甲基-D-天冬氨酸(NMDA)、γ-氨基丁酸A型(GABAA)等神经递质受体的功能,同时通过外周FXR-成纤维细胞生长因子15/19(FGF15/19)、TGR5-胰高血糖素样肽-1(GLP-1)通路间接向脑传递信号,参与摄食、觉醒等神经功能调控;病理状态下,肝性脑病(HE)、阿尔茨海默病(AD)、帕金森病(PD)等神经疾病中存在胆汁酸谱的异常改变,次级疏水胆汁酸(如石胆酸LCA、脱氧胆酸DCA)可能通过诱导神经炎症、氧化应激参与致病,而亲水胆汁酸(如熊去氧胆酸UDCA、牛磺熊去氧胆酸TUDCA)则通过多机制发挥神经保护作用。现有研究的技术方法优势在于结合了代谢组学、分子生物学、动物模型等多维度技术,首次揭示了胆汁酸-脑轴的存在;局限性在于脑内胆汁酸合成的精准调控、不同胆汁酸亚型的神经效应差异、间接信号通路在脑内的功能验证还不够深入,缺乏大规模临床队列验证胆汁酸Biomarker的临床价值,以及UDCA/TUDCA治疗神经疾病的临床疗效数据有限。
这篇综述的创新价值在于首次系统整合了胆汁酸从代谢到神经功能的全链条研究,明确了脑-外周胆汁酸对话的多通路机制,同时总结了UDCA/TUDCA在不同神经疾病中的神经保护机制,填补了领域内对胆汁酸神经调节作用全景式梳理的空白,为后续研究提供了清晰的方向框架。
3. 研究思路总结与详细解析
本综述以“代谢基础-信号通路-生理功能-病理效应-治疗潜力”为整体研究框架,核心科学问题是明确胆汁酸信号在脑内生理与病理条件下的作用机制及临床转化价值,技术路线为整合已发表的基础实验、临床样本分析、动物模型研究成果,进行系统梳理与总结。
3.1 胆汁酸外周与脑内代谢通路梳理
实验目的:明确胆汁酸在肝脏、肠道的经典合成与肠肝循环机制,以及脑内胆汁酸的合成与排泄途径,为后续神经功能研究奠定代谢基础。
方法细节:整合已有的分子生物学研究(如酶基因敲除/过表达动物模型)、代谢组学分析(如胆汁酸亚型定量),梳理肝脏经典/替代合成通路、肠道微生物介导的次级胆汁酸转化、脑内CYP46A1与CYP27A1介导的胆固醇代谢通路,以及胆汁酸跨BBB的转运方式。
结果解读:肝脏中经典通路以胆固醇7α-羟化酶(CYP7A1)为关键酶合成胆酸(CA)与鹅去氧胆酸(CDCA),替代通路以固醇27-羟化酶(CYP27A1)为关键酶合成CDCA;肠道微生物通过去羟基化等反应将初级胆汁酸转化为次级胆汁酸;脑内通过固醇24-羟化酶(CYP46A1)将胆固醇转化为24(S)-羟胆固醇(24S-OHC),跨BBB进入肝脏合成CDCA,这是脑内胆固醇排泄的主要途径;胆汁酸可通过被动扩散(疏水亚型)或转运体(如顶端钠依赖胆汁酸转运体ASBT、钠牛磺胆酸共转运多肽NTCP,结合型亚型)跨BBB进入脑内。
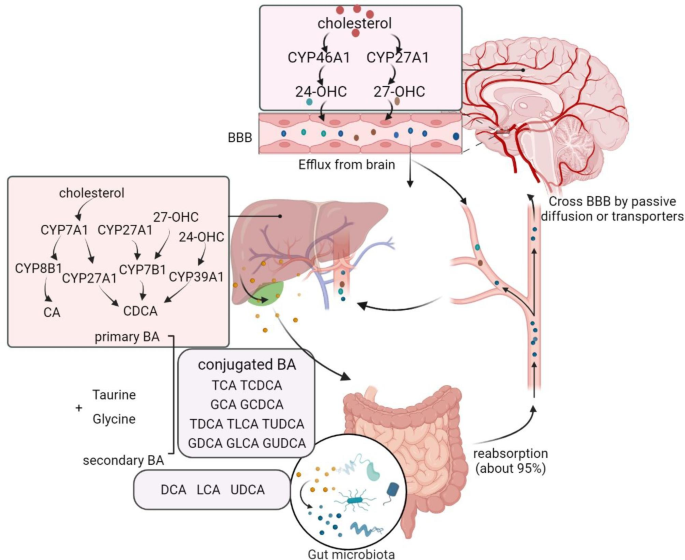
产品关联:文献未提及具体实验产品,领域常规使用高效液相色谱-质谱联用(LC-MS/MS)进行胆汁酸亚型定量、基因编辑工具构建酶基因修饰动物模型、免疫印迹(WB)检测代谢酶表达。
3.2 脑-外周胆汁酸信号通路解析
实验目的:梳理胆汁酸向中枢神经系统传递信号的直接与间接通路,明确其神经调节的分子机制。
方法细节:整合细胞实验(如神经元/胶质细胞受体激活实验)、动物模型研究(如受体敲除小鼠行为学分析)、代谢组学与转录组学联合分析,总结直接通路(脑内受体激活、神经递质受体调节)与间接通路(外周FXR-FGF15/19、TGR5-GLP-1)的功能效应。
结果解读:直接通路中,胆汁酸可激活脑内FXR、TGR5受体,调节神经递质释放与神经元兴奋性;还可作为NMDA、GABAA受体的拮抗剂,影响神经元活动(如UDCA通过阻断GABAA受体促进觉醒)。间接通路中,外周胆汁酸激活肠道FXR诱导FGF15/19分泌,FGF15/19跨BBB进入脑内激活成纤维细胞生长因子受体4(FGFR4),参与糖代谢与能量稳态调控;激活肠道L细胞TGR5诱导GLP-1分泌,GLP-1通过迷走神经-脑干-下丘脑通路传递信号,抑制摄食。
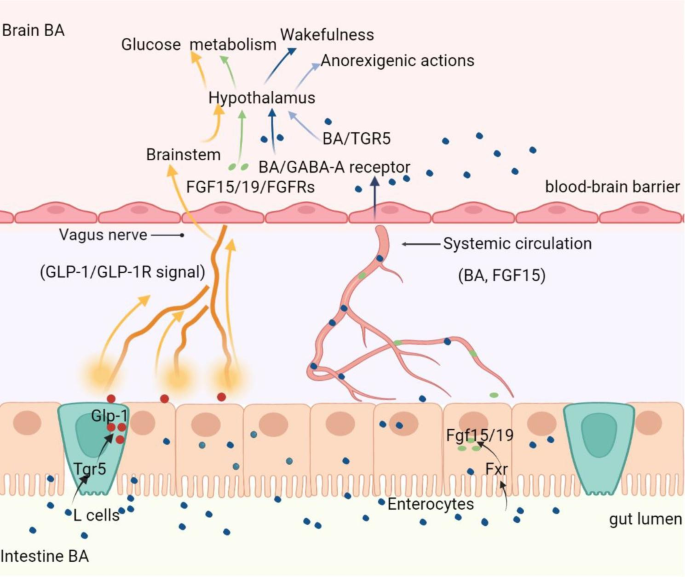
产品关联:文献未提及具体实验产品,领域常规使用受体激动剂/拮抗剂进行功能验证、行为学分析系统检测动物神经行为、酶联免疫吸附实验(ELISA)检测FGF15/19、GLP-1等细胞因子水平。
3.3 病理状态下胆汁酸的作用机制总结
实验目的:明确胆汁酸在神经疾病中的致病作用与神经保护机制,为疾病诊断与治疗提供依据。
方法细节:整合临床样本代谢组学分析(如HE、AD患者脑脊液/血清胆汁酸谱检测)、动物模型研究(如AD模型APP/PS1小鼠、PD模型MPTP小鼠)、细胞实验(如胶质细胞炎症实验、神经元凋亡实验),总结胆汁酸在不同神经疾病中的异常改变及功能效应。
结果解读:致病作用方面,HE患者脑脊液中结合型胆汁酸(如甘氨熊去氧胆酸GUDCA、甘氨胆酸GCA)显著升高,脑内LCA积累诱导神经炎症;AD患者血清与脑内次级胆汁酸(如DCA、甘氨脱氧胆酸GDCA)水平升高,其与初级胆汁酸的比值与淀粉样蛋白沉积、脑萎缩正相关;PD患者血浆中结合型与游离型胆汁酸水平升高,前驱期小鼠血清中ω-鼠胆酸(MCA-Ω)、TUDCA、UDCA下调。神经保护作用方面,UDCA/TUDCA可通过抑制核因子κB(NF-κB)、丝裂原活化蛋白激酶(MAPK)通路减少胶质细胞激活与炎症因子释放,抑制线粒体凋亡通路减少神经元凋亡,激活核因子E2相关因子2(Nrf2)通路减轻氧化应激,还可作为分子伴侣抑制内质网应激,在AD、PD、脊髓损伤等疾病中发挥保护作用。
产品关联:文献未提及具体实验产品,领域常规使用脂多糖(LPS)诱导胶质细胞炎症模型、β-淀粉样蛋白(Aβ)诱导神经元凋亡模型、流式细胞术检测细胞凋亡率。
4. Biomarker研究及发现成果解析
文献中涉及的Biomarker包括神经疾病中的异常胆汁酸亚型(致病型与保护型),筛选与验证逻辑为临床样本代谢组学筛选→动物模型验证→细胞实验机制研究,覆盖了肝性脑病、阿尔茨海默病、帕金森病等多种神经疾病。
Biomarker定位:致病型Biomarker包括HE患者脑内的LCA、血清/脑脊液中的结合型胆汁酸(GUDCA、GCA),AD患者血清/脑内的次级胆汁酸(DCA、GDCA)及其与初级胆汁酸的比值,PD患者血浆中的结合型与游离型胆汁酸;保护型Biomarker为UDCA与TUDCA,其筛选逻辑是基于临床样本中胆汁酸谱的异常改变,结合动物模型与细胞实验验证其功能效应。
研究过程详述:Biomarker来源包括临床患者的血清、脑脊液、脑组织样本,以及疾病动物模型的组织样本;验证方法包括靶向代谢组学检测胆汁酸亚型水平、相关性分析(如AD中胆汁酸比值与脑影像学、脑脊液生物标志物的关联)、动物模型干预实验(如HE模型中胆汁酸螯合剂降低脑内胆汁酸水平改善神经症状);特异性与敏感性数据方面,HE患者脑脊液中GUDCA升高93倍、GCA升高241倍(文献未明确样本量与P值),AD患者血清中GDCA:CA比值与淀粉样蛋白沉积正相关(文献未明确AUC值),PD前驱期小鼠血清中MCA-Ω、TUDCA、UDCA下调,联合检测可区分模型小鼠与对照小鼠(文献未明确敏感性与特异性数值)。
核心成果提炼:致病型胆汁酸亚型可作为神经疾病的潜在风险Biomarker,如AD中次级胆汁酸比值可反映疾病进展程度;UDCA/TUDCA可作为神经疾病的治疗Biomarker,其功能关联包括通过抗炎、抗凋亡等多机制改善神经症状,创新性在于首次系统总结了胆汁酸在多种神经疾病中的Biomarker潜力,以及作为治疗靶点的多维度作用;统计学结果方面,部分相关性研究未明确标注P值与样本量,部分动物实验结果显示胆汁酸干预可显著改善神经症状(如HE模型中胆汁酸螯合剂延迟神经衰退,文献未明确具体P值)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。