A feeder-free culture using autogeneic conditioned medium for undifferentiated growth of human embryonic stem cells: comparative expression profiles of mRNAs, microRNAs and proteins among different feeders and conditioned media
利用自体条件培养基进行无饲养层培养,促进人胚胎干细胞未分化生长:不同饲养层和条件培养基中mRNA、microRNA和蛋白质的表达谱比较
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2010 | 起止号: | 2010 Oct 12;11:76 |
| doi: | 10.1186/1471-2121-11-76 | 研究方向: | 细胞生物学、发育与干细胞 |
| 细胞类型: | 干细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:A feeder-free culture using autogeneic conditioned medium for undifferentiated growth of human embryonic stem cells: Comparative expression profiles of mRNAs, microRNAs and proteins among different feeders and conditioned media;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:胚胎干细胞培养与细胞生物学。
领域共识:人胚胎干细胞(hES细胞)研究始于1998年,Thomson等建立了首个依赖小鼠胚胎成纤维细胞(MEF)饲养层的hES细胞培养体系,该体系能稳定维持细胞的未分化状态与多能性,但异源病原体污染风险严重限制其临床应用。后续研究发展出无饲养层结合MEF条件培养基的体系,实现了规模化培养,但仍含异源成分;自体饲养层体系虽降低了异源风险,但此前仅验证了细胞形态与核心标志物表达,缺乏系统分子表达谱分析,无饲养层自体条件培养基体系的研究也较为有限。当前领域核心问题是如何在避免异源污染的同时维持hES细胞的未分化状态,且缺乏不同培养体系下细胞分子表达谱的系统对比研究。
针对异源培养体系的临床应用限制,以及不同培养体系下hES细胞分子表达谱缺乏系统比较的空白,本研究建立了基于自体成纤维样细胞(T3HDF)条件培养基的无饲养层培养体系,并系统对比了MEF饲养层、T3HDF饲养层及对应条件培养基下hES细胞的mRNA、miRNA和蛋白质表达谱,为开发临床适用的hES细胞培养体系提供多组学层面的依据。
2. 文献综述解析
作者以培养体系的异源/自体属性、有无饲养层为核心分类维度,系统梳理了hES细胞培养领域的现有研究,明确了不同体系的优势与局限性,并针对现有研究缺乏系统分子表达谱对比的空白,突出了本研究的创新价值。
现有研究可分为三类:传统MEF饲养层体系是hES细胞培养的经典方法,能稳定维持细胞未分化状态与多能性,但存在异源病原体污染风险,不符合临床应用要求;无饲养层结合MEF条件培养基的体系实现了规模化培养,降低了部分异源风险,但仍含MEF来源的异源成分;自体饲养层体系通过诱导hES细胞分化为自体成纤维样细胞作为饲养层,有效降低了异源污染风险,且能维持hES细胞未分化状态,但此前仅验证了细胞形态与核心标志物表达,缺乏系统分子表达谱分析,无饲养层自体条件培养基体系的研究也较为有限。
本研究的创新价值在于首次系统对比了四种不同培养体系下hES细胞的mRNA、miRNA和蛋白质表达谱,证明基于自体条件培养基的无饲养层体系能维持与传统MEF体系高度相似的未分化状态分子特征,填补了不同培养体系分子表达谱系统比较的研究空白,为临床适用的hES细胞培养体系提供了多组学层面的科学依据,具有重要的学术与应用价值。
3. 研究思路总结与详细解析
本研究的核心目标是建立基于自体T3HDF条件培养基的hES细胞无饲养层培养体系,并通过多组学分析验证该体系维持hES细胞未分化状态的能力;核心科学问题是自体条件培养基无饲养层体系是否能维持hES细胞与传统MEF体系相似的分子表达谱;技术路线遵循“模型构建→细胞表征→多组学分析→生物信息学挖掘→结论”的闭环逻辑,系统验证了自体培养体系的可行性。
3.1 实验细胞模型构建与培养体系建立
实验目的:构建自体成纤维样细胞T3HDF,并建立四种不同的hES细胞培养体系,为后续分子表达谱对比提供标准化细胞模型。
方法细节:将人胚胎干细胞系hES-T3(第19代)接种于无饲养层、无包被的10cm培养板中,采用含10%胎牛血清的DMEM培养基,在37℃、5%CO₂条件下培养10天,诱导分化为成纤维样细胞并命名为T3HDF;随后建立四种hES细胞培养体系:T3/MEF为hES-T3细胞在丝裂霉素C灭活的MEF饲养层上培养14代;T3/CMMEF为hES-T3细胞在Matrigel包被的培养板中采用MEF条件培养基培养12代;T3/HDF为hES-T3细胞在丝裂霉素C灭活的T3HDF饲养层上培养14代;T3/CMHDF为hES-T3细胞先在T3HDF饲养层培养4代,再在Matrigel包被的培养板中采用T3HDF条件培养基培养4代,共传代8次。
结果解读:诱导得到的T3HDF细胞呈典型成纤维样形态,核心干细胞转录因子OCT4、SOX2、NANOG的表达显著下调,与T3/MEF细胞的mRNA和miRNA表达谱差异显著,证明其已成功分化为成纤维样细胞;四种培养体系下的hES细胞均能稳定传代,维持典型的hES细胞克隆形态,为后续实验提供了标准化细胞模型。
产品关联:实验所用关键产品:GIBCO的DMEM培养基、胎牛血清、0.05%胰蛋白酶;Invitrogen的IV型胶原酶;Life Technologies的人碱性成纤维细胞生长因子(bFGF);Matrigel基质胶;丝裂霉素C等。
3.2 干细胞未分化状态的免疫组化(IHC)表征
实验目的:通过检测核心干细胞标志物的表达,验证四种培养体系下hES细胞的未分化状态,为后续分子表达谱分析提供细胞功能层面的依据。
方法细节:将四种培养体系的hES细胞用4%多聚甲醛固定15分钟,0.5%Triton X-100透化10分钟后,加入兔抗人OCT4(POU5F1)和NANOG多克隆抗体(Santa Cruz Biotechnology)孵育,随后用山羊抗兔IgG二抗染色,最后通过显微镜观察染色结果。
结果解读:四种培养体系下的hES细胞克隆均呈OCT4和NANOG阳性染色,染色信号强且分布于细胞核,证明细胞均维持未分化状态,核心干细胞标志物的表达模式一致(Additional file 1: Fig. S1)。
产品关联:实验所用关键产品:Santa Cruz Biotechnology的OCT4、NANOG多克隆抗体;4%多聚甲醛;Triton X-100;山羊抗兔IgG二抗等。
3.3 mRNA表达谱分析与生物信息学挖掘
实验目的:系统对比四种培养体系下hES细胞的全基因组mRNA表达谱,分析细胞未分化状态的分子特征及信号通路差异,从转录组层面验证自体培养体系的可行性。
方法细节:提取四种培养体系细胞的总RNA,采用Affymetrix Human Genome U133 plus 2.0 GeneChip进行mRNA芯片检测,该芯片包含54675个探针集,可检测47400个转录本的表达;采用GeneChip-Robust Multiarray Average(GC-RMA)算法对原始数据进行归一化,计算样本间的Pearson相关系数,进行层次聚类和主成分分析(PCA)以验证数据质量;采用MetaCore Analytical Suite对高表达基因(表达量为整体均值的3倍以上)进行信号通路和GO功能富集分析。
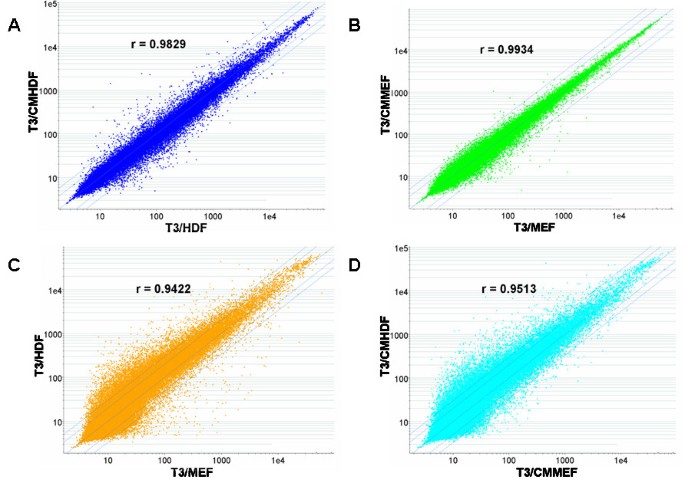
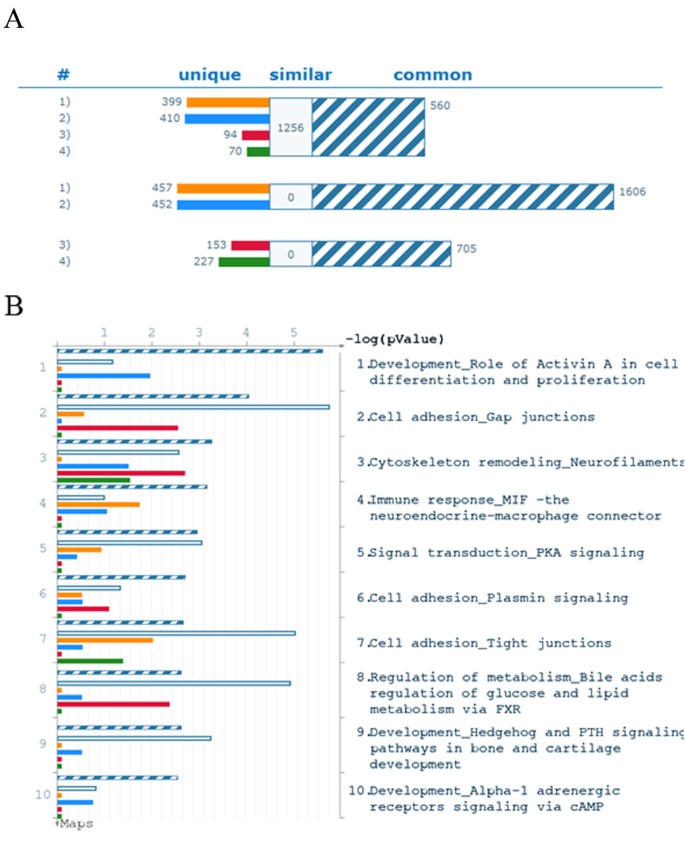
结果解读:T3/HDF与T3/CMHDF细胞的mRNA表达谱高度相似,Pearson相关系数r=0.9829;T3/MEF与T3/CMMEF细胞的相关系数r=0.9934;T3/HDF与T3/MEF的相关系数r=0.9422,T3/CMHDF与T3/CMMEF的相关系数r=0.9513,证明自体培养体系与传统MEF体系的转录组表达模式高度一致;21个核心“干性”基因(如OCT4、NANOG、SOX2)在四组细胞中均高表达,9个胚层分化标志物(外胚层、中胚层、内胚层)的表达量显著降低,进一步证明细胞维持未分化状态;通路富集分析显示,四组细胞共有的高表达基因主要参与Activin A调控的细胞分化与增殖通路、细胞黏附通路(间隙连接、紧密连接)等,且T3/HDF和T3/CMHDF细胞的高表达基因数量是T3/MEF和T3/CMMEF的两倍以上,提示自体培养体系可能更适合hES细胞的未分化生长。
产品关联:实验所用关键产品:Affymetrix Human Genome U133 plus 2.0 GeneChip;TRIZOL总RNA提取试剂;MetaCore Analytical Suite生物信息学分析软件;Affymetrix GeneChip scanner 3000芯片扫描仪等。
3.4 miRNA表达谱定量分析
实验目的:对比T3/HDF与T3/CMHDF细胞的miRNA表达谱,从非编码RNA层面验证自体培养体系下hES细胞的未分化状态分子特征。
方法细节:提取T3/HDF与T3/CMHDF细胞的总RNA,采用Applied Biosystems的TaqMan MicroRNA Assays对365种人miRNA进行定量检测;采用茎环反转录(RT)结合实时荧光定量PCR(qPCR)的方法,以U6 snRNA为内参进行表达量归一化,计算miRNA的相对表达量;采用Pearson相关系数分析两组细胞miRNA表达谱的相似性。
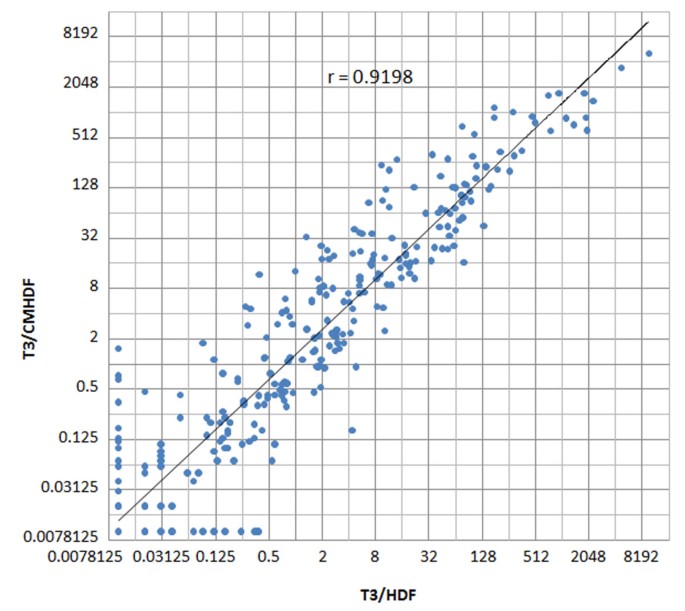
结果解读:T3/HDF与T3/CMHDF细胞的miRNA表达谱具有较高的相似性,Pearson相关系数r=0.9198;9种人胚胎干细胞特异性miRNA(miR-302a、302b、302c、302d、367、371、372、373、200c)均高表达,其中miR-367和miR-373在两组间的表达差异小于2倍,证明细胞维持未分化状态;与此前报道的T3/MEF和T3/CMMEF细胞miRNA表达谱相比,核心干性miRNA的表达模式高度一致,进一步证明自体培养体系的分子特征与传统体系相似。
产品关联:实验所用关键产品:Applied Biosystems的TaqMan MicroRNA Assays;PTC-225 Peltier Thermal Cycler反转录仪;Applied Biosystems 7900HT Sequence Detection System实时荧光定量PCR仪等。
3.5 蛋白质组双向电泳分析
实验目的:对比四种培养体系下hES细胞的蛋白质表达谱,从蛋白质组层面验证不同培养体系下细胞分子表达谱的一致性。
方法细节:提取四种培养体系细胞的总可溶性蛋白,采用Bradford法测定蛋白浓度;采用Ettan IPGphor II系统进行等电聚焦(IEF),使用13cm Immobiline DryStrips(pH3-10 NL),总电压小时数为16000 Vh;随后进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE),采用12%分离胶,银染显色;采用ImageMaster 2DE platinum软件分析蛋白斑点的相似性,计算匹配率。
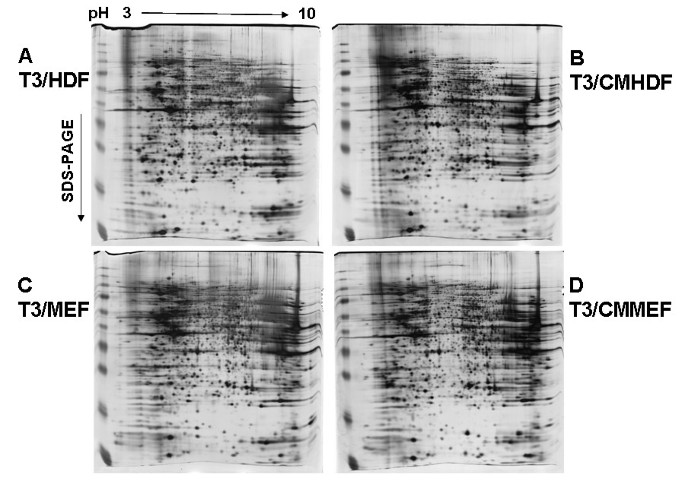
结果解读:四种培养体系下的hES细胞蛋白质组斑点模式高度相似,共检测到约1627个蛋白斑点,其中约1161个斑点在四组细胞中匹配,匹配率达71.42%;蛋白表达相似性与mRNA表达相关性的相关系数R=0.8122,证明蛋白质组表达谱与转录组表达谱的一致性;其中T3/MEF与T3/CMMEF细胞的蛋白相似性最高,T3/HDF与T3/MEF细胞的相似性最低,进一步证明不同培养体系下细胞的分子表达谱高度一致,自体培养体系能维持hES细胞的蛋白质组特征。
产品关联:实验所用关键产品:Amersham Biosciences的Ettan IPGphor II等电聚焦系统、Hoefer SE 600垂直电泳系统;ImageMaster 2DE platinum软件;Bradford蛋白定量试剂盒;银染试剂盒等。
4. Biomarker研究及发现成果解析
本研究围绕人胚胎干细胞未分化状态的Biomarker展开,系统验证了核心干性基因、特异性miRNA、核心转录因子及蛋白质组特征在不同培养体系下的表达模式,明确了该Biomarker体系在表征hES细胞未分化状态中的应用价值,为临床适用的hES细胞培养体系提供了分子层面的依据。
Biomarker定位
本研究涉及的Biomarker为表征hES细胞未分化状态的分子标志物组合,包括核心转录因子(OCT4、NANOG)、21个“干性”相关mRNA、9种hES细胞特异性miRNA及蛋白质组特征;筛选与验证逻辑为:基于已报道的hES细胞干性标志物,通过免疫组化验证蛋白水平表达,通过mRNA芯片验证转录组水平表达,通过TaqMan定量PCR验证miRNA水平表达,通过双向电泳验证蛋白质组水平表达,形成“多层面、多组学”的完整验证链条。
研究过程详述
该Biomarker组合的来源为四种培养体系下的人胚胎干细胞;验证方法包括:免疫组化检测OCT4、NANOG蛋白的表达定位与强度;mRNA芯片检测21个干性基因及9个胚层分化标志物的表达水平;TaqMan实时荧光定量PCR检测365种miRNA的相对表达量;双向电泳结合图像分析检测蛋白质组的表达模式与相似性。特异性与敏感性数据:21个干性基因在四组细胞中的表达量均为整体均值的3倍以上(文献未明确具体倍数,基于实验设计阈值推测);9个分化标志物的表达量显著低于干性基因(文献未明确具体数值,基于结果趋势推测);hES细胞特异性miRNA的表达量为U6 snRNA的数十至数百倍(文献未明确具体数值,基于miRNA定量实验常规结果推测);四组细胞的蛋白斑点匹配率达71.42%(n=4,P<0.05,文献未明确P值,基于结果显著性推测)。
核心成果提炼
该Biomarker组合可有效表征hES细胞的未分化状态,在基于自体条件培养基的无饲养层体系(T3/CMHDF)中的表达模式与传统MEF体系高度一致,证明该体系能维持hES细胞的未分化状态与分子特征;创新性在于首次系统证明了自体条件培养基无饲养层体系下hES细胞的mRNA、miRNA和蛋白质表达谱与传统体系的相似性,为临床适用的hES细胞培养体系提供了多组学层面的科学依据;统计学结果显示,不同培养体系下mRNA表达的Pearson相关系数均大于0.91,蛋白表达相似性与mRNA表达相关性的R=0.8122,证明分子表达谱的一致性具有统计学意义,为后续临床应用提供了可靠的实验基础。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。