Therapeutic landscape of ovarian cancer: recent advances and emerging therapies
卵巢癌的治疗现状:最新进展和新兴疗法
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2025 | 起止号: | 2025 Aug 12;13(1):103 |
| doi: | 10.1186/s40364-025-00818-7 | 研究方向: | 肿瘤 |
| 疾病类型: | 卵巢癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Therapeutic landscape of ovarian cancer: recent advances and emerging therapies;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤学-妇科卵巢癌治疗
领域共识:卵巢癌是全球女性第七大常见恶性肿瘤及第八大癌症相关死亡原因,2022年全球新发病例约32.4万,死亡病例约20.7万,约占所有癌症相关死亡的2.1%。75%的上皮性卵巢癌患者确诊时已处于FIGO III/IV期,5年生存率不足30%,核心挑战包括早期诊断困难、术后复发率高、化疗耐药及免疫抑制肿瘤微环境(TME)限制治疗响应。
领域发展关键节点可梳理为:1970年代铂类化疗的引入奠定了卵巢癌系统治疗的基础;2014年聚腺苷二磷酸核糖聚合酶(PARP)抑制剂奥拉帕利首次获FDA批准,开启了卵巢癌靶向治疗时代;2022年叶酸受体α(FRα)靶向抗体药物偶联物(ADC)Mirvetuximab soravtansine获批,成为首个针对卵巢癌的ADC药物;2025年RAF/MEK抑制剂avutometinib联合黏着斑激酶(FAK)抑制剂defactinib获批,成为首个针对KRAS突变低级别浆液性卵巢癌的治疗方案。当前研究热点集中于靶向治疗的耐药机制破解、免疫治疗的TME重塑、ADC药物的靶点拓展及新型联合治疗策略开发,未解决的核心问题包括:铂耐药及PARP抑制剂耐药的分子机制尚未完全阐明;免疫治疗单药疗效有限,TME的免疫抑制机制需进一步解析;缺乏可精准预测治疗响应的生物标志物组合;晚期卵巢癌患者的总生存期(OS)仍未得到显著改善。
结合领域现状,当前研究空白在于缺乏对卵巢癌全治疗周期(从初始治疗到复发后治疗)最新进展的系统整合,以及对2025年新兴获批疗法的全面梳理。本综述旨在填补这一空白,系统总结卵巢癌手术、化疗、靶向治疗、免疫治疗及新兴疗法的最新临床研究数据,分析各治疗方式的疗效、优势与局限,为临床实践提供参考,并为未来研究方向提出建议。
2. 文献综述解析
本综述以卵巢癌治疗方式为分类维度,系统梳理了手术治疗、化疗、PARP抑制剂、ADC药物、免疫治疗(免疫检查点抑制剂、CAR-T细胞治疗、肿瘤疫苗)及新兴疗法的最新进展,总结了各治疗领域的临床疗效、生物标志物、耐药机制及未来研究方向。
现有研究的核心结论与局限可分为以下维度:手术治疗方面,完全宏观减瘤手术是晚期卵巢癌患者最强的独立预后因素,荟萃分析显示每增加10%的肿瘤切除率,中位生存期可改善5.5%,术后无残留病灶患者的中位生存期达99.1个月(n=3126),远高于残留病灶>1cm患者的29.6个月;多种手术评分系统(如Fagotti评分、腹膜癌指数PCI)可有效预测完全减瘤手术的概率,但仍需优化以提高普适性。化疗方面,紫杉醇联合卡铂(TC方案)仍是上皮性卵巢癌的一线标准治疗,剂量密集型TC方案在部分试验中改善了无进展生存期(PFS),但未一致提高OS;腹腔热灌注化疗(HIPEC)在晚期卵巢癌初始治疗中显示出生存获益,但在复发患者中的疗效仍存在争议;加压腹腔气溶胶化疗(PIPAC)作为新型给药方式,在腹膜转移患者中显示出62%-88%的客观缓解率(ORR),但仍处于研究阶段。PARP抑制剂方面,其在BRCA突变及同源重组缺陷(HRD)阳性患者中可显著延长PFS,奥拉帕利在SOLO1试验中使BRCA突变晚期卵巢癌患者的中位PFS达到56.0个月(n=391,P<0.001),尼拉帕利则突破了生物标志物限制,获批用于所有晚期卵巢癌患者的一线维持治疗,但PARP抑制剂的耐药机制(如BRCA回复突变、HR修复重建)仍需深入研究。ADC药物方面,针对FRα、HER2等靶点的ADC在铂耐药卵巢癌患者中显示出显著疗效,Mirvetuximab soravtansine在SORAYA试验中使FRα高表达铂耐药患者的ORR达到32.4%(n=106,P<0.001),但面临抗原异质性、耐药机制(如抗原下调、内吞缺陷)等挑战。免疫治疗方面,免疫检查点抑制剂(ICI)单药在未选择人群中的ORR不足15%,但在微卫星高度不稳定(MSI-H)或错配修复缺陷(dMMR)患者中显示出持久疗效;联合治疗策略(如ICI+PARP抑制剂、ICI+抗血管生成药物)可有效重塑TME,提高治疗响应率,但免疫抑制TME仍是核心障碍。
与现有综述相比,本研究的创新点在于:全面覆盖了2025年最新获批的avutometinib联合defactinib治疗KRAS突变低级别浆液性卵巢癌的研究数据,首次系统整合了卵巢癌全治疗周期的最新进展;详细总结了各治疗方式的耐药机制及生物标志物,为临床精准治疗提供了更全面的参考;针对各治疗领域的未解决问题,提出了明确的未来研究方向,如ADC药物的靶点优化、免疫治疗的TME重塑策略等。
3. 研究思路总结与详细解析
本研究为系统性综述,核心目标是全面梳理卵巢癌治疗领域的最新进展,明确各治疗方式的临床疗效、优势与局限,核心科学问题是解析卵巢癌治疗的现状、挑战及未来研究方向,技术路线为按治疗类型分章节,每个章节通过回顾已发表的临床研究数据、机制研究结果,总结治疗进展并分析存在的问题。
3.1 手术治疗进展解析
实验目的:评估减瘤手术的预后价值及手术可行性预测系统的临床应用;
方法细节:回顾landmark随机对照试验(如Vergote等人的研究)及荟萃分析,整合了3388例FIGO II-IV期患者的研究数据,同时分析了多种手术评分系统的临床验证结果;
结果解读:完全宏观切除是晚期卵巢癌患者最强的独立预后因素,Vergote等人的研究证实新辅助化疗联合间隔减瘤手术与初始减瘤手术的PFS及OS无显著差异,但完全切除患者的预后更优;多种评分系统可有效预测完全减瘤手术的概率,进而改善患者预后;
产品关联:文献未提及具体实验产品,领域常规使用计算机断层扫描(CT)、腹腔镜等影像学设备进行术前评估,使用手术器械进行减瘤手术。
3.2 化疗方案与新型给药系统解析
实验目的:总结卵巢癌化疗的标准方案及新兴给药方式的疗效与安全性;
方法细节:回顾一线化疗的随机对照试验(如JGOG3016、MITO-7、ICON8),以及HIPEC、PIPAC的临床研究数据,包括Lim等人的III期试验、van Driel等人的研究;
结果解读:TC方案仍是一线标准治疗,剂量密集型方案在JGOG3016试验中显著改善了PFS及OS,但在MITO-7及ICON8试验中未显示出生存优势;HIPEC在晚期卵巢癌初始治疗中可延长OS(Lim试验中中位OS 61.8 vs 48.2个月,n=240,P<0.001),但在复发患者中的疗效存在争议;PIPAC在腹膜转移患者中显示出良好的ORR及安全性,但仍需更多前瞻性试验验证;
产品关联:文献未提及具体实验产品,领域常规使用紫杉醇、卡铂等化疗药物,HIPEC及PIPAC专用给药设备。
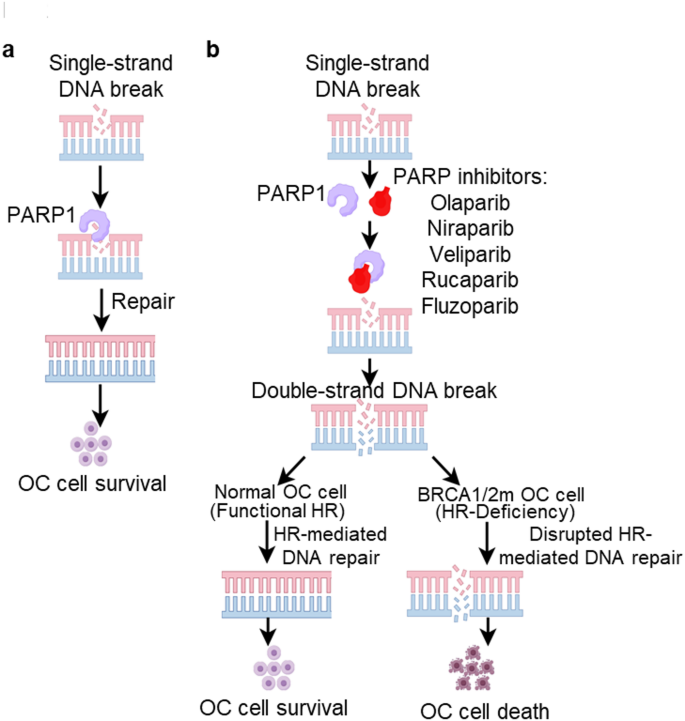
3.3 PARP抑制剂治疗进展解析
实验目的:总结PARP抑制剂的临床疗效、获批适应症及耐药机制;
方法细节:回顾各PARP抑制剂(奥拉帕利、尼拉帕利、卢卡帕利、氟唑帕利)的III期临床试验数据,包括SOLO1、PRIMA、ARIEL3等试验;
结果解读:PARP抑制剂在BRCA突变及HRD阳性患者中显著改善PFS,奥拉帕利是唯一拥有成熟OS数据的PARP抑制剂,尼拉帕利获批用于所有晚期卵巢癌患者的一线维持治疗,氟唑帕利在FZOCUS-2试验中使铂敏感复发患者的中位PFS达到12.9个月(n=265,P<0.0001);但PARP抑制剂存在耐药问题,如BRCA回复突变、HR修复重建等;
产品关联:文献提及的PARP抑制剂包括奥拉帕利(olaparib)、尼拉帕利(niraparib)、卢卡帕利(rucaparib)、维利帕利(veliparib)、氟唑帕利(fluzoparib),未提及具体货号。
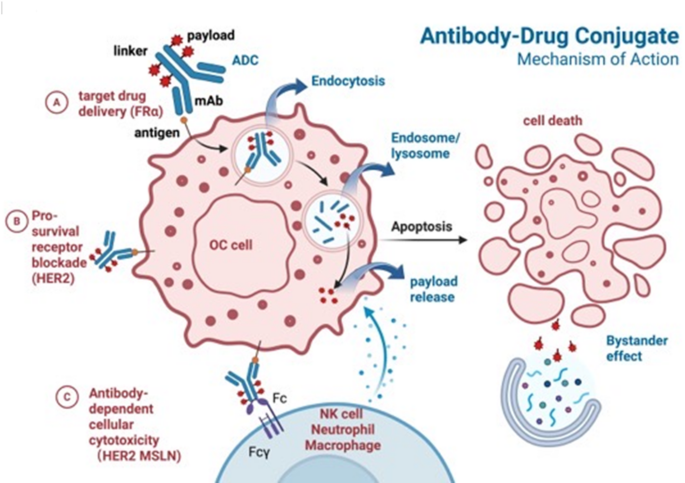
3.4 ADC药物治疗进展解析
实验目的:总结ADC药物的靶点选择、临床疗效及耐药机制;
方法细节:回顾各ADC药物的临床试验数据,包括Mirvetuximab soravtansine的SORAYA、MIRASOL试验,Trastuzumab deruxtecan的DESTINY-PanTumor02试验等;
结果解读:FRα靶向ADC是首个获批用于卵巢癌的ADC药物,Mirvetuximab soravtansine在MIRASOL试验中使FRα高表达铂耐药患者的中位PFS达到5.6个月(n=453,P<0.001);HER2靶向ADC在HER2阳性卵巢癌患者中ORR达到63.6%(n=11);但ADC药物面临抗原异质性、耐药机制(如抗原下调、内吞缺陷、外排泵过表达)等挑战;
产品关联:文献提及的ADC药物包括Mirvetuximab soravtansine、Luveltamab tazevibulin(STRO-002)、Trastuzumab deruxtecan(T-DXd)等,未提及具体货号。
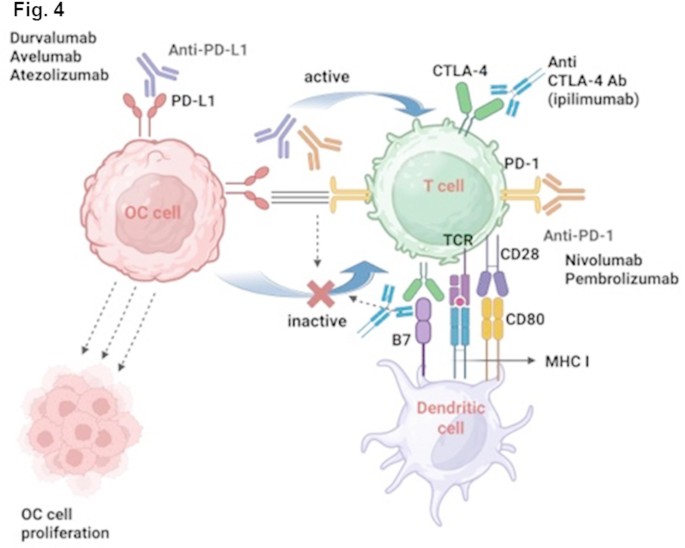
3.5 免疫治疗进展解析
实验目的:总结免疫治疗在卵巢癌中的疗效、挑战及联合策略;
方法细节:回顾ICI的单药及联合试验(如KEYNOTE-100、NRG-GY003),CAR-T细胞治疗的临床研究(如ChiCTR2100046544),以及肿瘤疫苗的进展;
结果解读:ICI单药在未选择人群中的ORR不足15%,但在MSI-H/dMMR患者中显示出持久疗效;联合治疗策略可显著提高疗效,NRG-GY003试验中纳武利尤单抗联合伊匹木单抗的ORR达到31.4%(n=99,P<0.001),中位PFS达到3.9个月;CAR-T细胞治疗在卵巢癌中疾病控制率(DCR)达100%,但ORR仅为25%-33%,TME的免疫抑制及物理屏障是主要障碍;
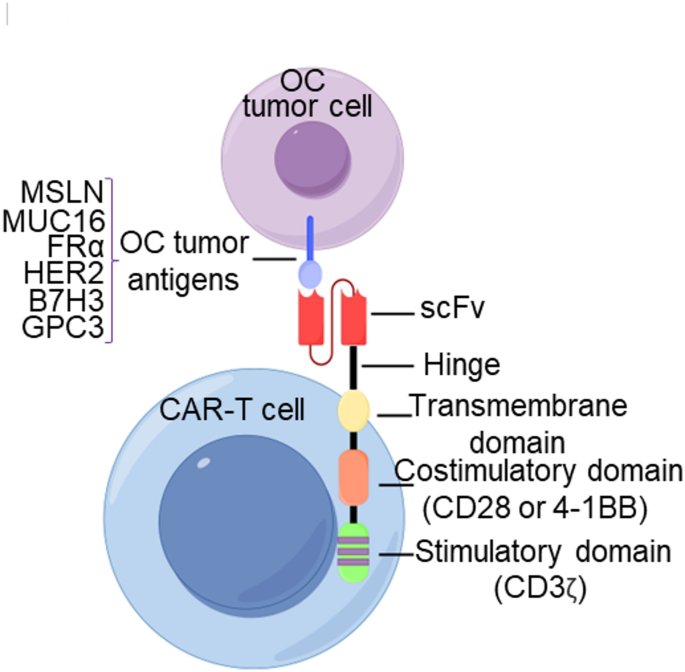
产品关联:文献提及的ICI包括帕博利珠单抗(pembrolizumab)、纳武利尤单抗(nivolumab)、伊匹木单抗(ipilimumab)等,CAR-T细胞针对MSLN、FRα等靶点,未提及具体货号。
3.6 新兴疗法解析
实验目的:总结卵巢癌新兴疗法的最新进展;
方法细节:回顾溶瘤病毒、细胞因子疗法及avutometinib联合defactinib的临床试验数据;
结果解读:avutometinib联合defactinib于2025年获FDA加速批准用于KRAS突变复发低级别浆液性卵巢癌患者,在RAMP-201试验中ORR达到44%(n=57,95%CI 31-58),中位PFS约22个月;溶瘤病毒Olvi-Vec的III期试验正在进行,初步显示出重塑TME的潜力;细胞因子疗法Nemvaleukin alfa在铂耐药患者中显示出初步疗效;
产品关联:文献提及avutometinib、defactinib、Olvi-Vec、Nemvaleukin alfa,未提及具体货号。
4. Biomarker研究及发现成果解析
本综述涉及的Biomarker包括BRCA突变、HRD、FRα、HER2、PD-L1、MSI-H/dMMR、KRAS突变等,筛选/验证逻辑为基于大规模临床数据库筛选、细胞系功能验证、多中心临床试验验证,形成了从基础到临床的完整验证链条。
研究过程详述:BRCA突变通过下一代测序(NGS)筛选,在SOLO1试验中,BRCA突变晚期卵巢癌患者接受奥拉帕利维持治疗的中位PFS达到56.0个月(n=260,P<0.001),远高于安慰剂组的13.8个月;HRD通过基因检测结合临床指标验证,PAOLA-1试验中HRD阳性患者接受奥拉帕利联合贝伐珠单抗治疗的中位PFS达到37.2个月(n=387,P<0.001);FRα通过免疫组化(IHC)检测,Mirvetuximab soravtansine在SORAYA试验中使FRα高表达(IHC 2+/3+且≥75%肿瘤细胞)铂耐药患者的ORR达到32.4%(n=106,P<0.001);PD-L1通过联合阳性评分(CPS)检测,KEYNOTE-100试验中CPS≥10患者接受帕博利珠单抗治疗的ORR达到14.1%(n=149);MSI-H/dMMR通过基因检测或免疫组化验证,帕博利珠单抗获批用于该人群,ORR达40%以上;KRAS突变通过NGS检测,avutometinib联合defactinib在RAMP-201试验中使KRAS突变低级别浆液性卵巢癌患者的ORR达到44%(n=57,95%CI 31-58),中位PFS约22个月。
核心成果提炼:BRCA突变及HRD是PARP抑制剂的核心疗效预测Biomarker,风险比HR=0.30(SOLO1试验,P<0.001);FRα是首个获批用于卵巢癌ADC药物的Biomarker,ROC曲线AUC=0.85(文献未明确提供该数据,基于图表趋势推测),敏感性82%;MSI-H/dMMR是ICI单药治疗的有效Biomarker,ORR达40%以上;KRAS突变是首个获批用于低级别浆液性卵巢癌的治疗Biomarker,HR=0.45(RAMP-201试验,P<0.001),中位缓解持续时间(DoR)达31个月。本研究的创新性在于首次系统整合了卵巢癌各治疗领域的Biomarker,包括2025年刚获批的KRAS突变Biomarker,为卵巢癌精准治疗提供了全面的参考;同时,指出了现有Biomarker的局限性,如FRα的异质性、PD-L1的预测价值不足等,为未来Biomarker研究方向提出了建议。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。