OPCML is hypermethylated in a subset of patients with metaplastic changes in their esophagus
在部分食管发生化生改变的患者中,OPCML 基因存在高甲基化现象。
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2018 | 起止号: | 2018;6:35 |
| doi: | 10.1186/s40364-018-0150-y | 研究方向: | 表观遗传 |
文献解析
1. 领域背景与文献引入
文献英文标题:OPCML is hypermethylated in a subset of patients with metaplastic changes in their esophagus;发表期刊:Biomarker Research;影响因子:未公开;研究领域:消化道肿瘤表观遗传学与癌前病变生物标志物研究。
消化道腺癌(食管腺癌、胃腺癌)的发生遵循多阶段级联演进规律,从慢性炎症、上皮化生逐步进展至异型增生,最终发展为浸润性腺癌,早期病变的隐匿性与缺乏特异性诊断标志物是临床早期筛查与干预的核心瓶颈。领域共识:表观遗传修饰尤其是CpG岛甲基化作为肿瘤发生的早期分子事件,其异常改变早于组织学形态变化,是极具潜力的癌前病变生物标志物。OPCML(阿片类结合蛋白/细胞黏附分子样蛋白)作为经典肿瘤抑制基因,其启动子区高甲基化介导的转录沉默已在卵巢癌、肝癌、胃癌等多种晚期癌症中被证实,但针对食管腺癌癌前病变阶段(尤其是化生阶段)的OPCML甲基化特征研究仍处于空白状态,无法为食管腺癌的早期筛查提供分子依据。本研究聚焦食管腺癌级联进程中OPCML外显子1的甲基化模式,旨在填补癌前病变阶段的研究空白,为食管腺癌早期诊断提供潜在生物标志物。
2. 文献综述解析
作者的综述逻辑遵循“分子特征→泛癌研究现状→机制假说→研究空白”的递进式框架,首先系统介绍OPCML的分子家族属性、组织表达谱及保守结构特征,随后按癌症类型分类总结其高甲基化的研究成果,进一步探讨其作为肿瘤抑制基因的潜在作用机制,最终明确食管腺癌癌前病变阶段的研究缺失。
现有研究显示,OPCML在健康组织中CpG岛甲基化水平较低,广泛表达于脑、卵巢、心脏、胃肠道等多种组织;在卵巢癌、肝细胞癌、肺腺癌、胃癌等多种癌症中,OPCML启动子区高甲基化可导致转录沉默,体外过表达OPCML可抑制癌细胞增殖、诱导细胞周期阻滞与凋亡,提示其兼具肿瘤抑制功能与潜在治疗靶点价值。但现有研究存在明显局限性:多数研究集中于晚期癌症阶段,缺乏对癌前病变尤其是食管化生阶段的关注;未明确OPCML甲基化在局部病变组织与外周血中的差异表达模式;对其在食管腺癌级联进程中的早期预警价值未进行系统验证。
本研究的创新价值在于首次将OPCML甲基化研究拓展至食管腺癌癌前病变阶段,通过对比正常食管、胃食管反流病、食管化生及腺癌组织的甲基化差异,结合细胞系与外周血样本验证,明确了OPCML外显子1高甲基化与食管化生亚群的关联,填补了癌前病变阶段的研究空白,为食管腺癌早期筛查提供了新的候选生物标志物。
3. 研究思路总结与详细解析
本研究的核心目标是明确OPCML在食管腺癌与胃腺癌级联进程中的甲基化模式,核心科学问题为OPCML外显子1高甲基化是否与食管化生及早期异型增生事件相关,技术路线遵循“临床队列构建→多维度样本采集→甲基化检测方法建立→组织/细胞系/外周血甲基化分析→结果验证”的闭环逻辑。
3.1 研究队列招募与样本采集
实验目的是建立覆盖食管腺癌与胃腺癌全级联进程的临床样本队列,为甲基化分析提供多样化研究材料。方法细节:食管腺癌队列招募152名接受上消化道内镜检查的受试者,按组织学结果分为正常食管(n=89)、胃食管反流病(n=42)、腺黏膜化生(n=20)、食管腺癌(n=1)四组,其中11名化生患者同步采集相邻正常组织样本;胃腺癌队列招募200名受试者,涵盖功能性消化不良、萎缩性胃炎、肠化生、异型增生、胃腺癌各阶段,采集外周血样本;所有研究均获得伦理委员会审批,受试者签署书面知情同意书。结果解读:成功建立包含不同病变阶段的临床队列,样本类型覆盖食管局部组织与外周血,为后续甲基化差异分析提供了完整的疾病进程样本链。实验所用关键产品:BD Vacutainer® SST™ Blood Collection Tubes。
3.2 细胞系培养与样本预处理
实验目的是在细胞水平验证OPCML甲基化与病变进展阶段的关联。方法细节:培养9种消化道细胞系,包括正常食管上皮细胞系HET-1A、食管化生/异型增生细胞系CP-A/CP-B/CP-C/CP-D、食管腺癌系OE33、胃癌系AGS、肠癌系LS 174T/Caco-2,根据细胞系类型分别采用LHC-9、Keratinocyte-SFM、RPMI、MEM培养基,在37℃、5%CO2条件下常规培养;使用Qiagen试剂盒分别提取食管组织、细胞系、外周血样本的基因组DNA。结果解读:完成所有细胞系的培养条件优化与基因组DNA提取,DNA纯度与浓度符合甲基化检测要求,为细胞系水平的甲基化验证提供了合格样本。实验所用关键产品:ThermoFisher Scientific的LHC-9培养基(货号12680013)、Keratinocyte-SFM培养基(货号17005042),Qiagen的Gentra Puregene Tissue kit、QIAamp DNA Blood Mini Kit。
3.3 OPCML甲基化检测方法建立与验证
实验目的是建立针对OPCML外显子1的精准甲基化定量检测方法。方法细节:使用PyroMark Assay Design Software设计特异性引物,靶向OPCML外显子1的3个CpG位点;采用Epitect Bisulphite Conversion Kit对基因组DNA进行亚硫酸氢盐转化,随后进行PCR扩增,扩增产物结合链霉亲和素磁珠,经变性、洗涤后进行焦磷酸测序,通过PyroMark Q24软件分析每个CpG位点的甲基化百分比;利用胃腺癌队列外周血样本验证检测方法的稳定性。结果解读:成功建立特异性强、重复性好的OPCML甲基化焦磷酸测序检测方法,可准确定量目标CpG位点的甲基化水平;胃腺癌队列外周血样本检测结果显示各病变阶段甲基化水平无显著差异,与健康组织水平一致,验证了方法的特异性。实验所用关键产品:Qiagen的Epitect Bisulphite Conversion Kit、PyroMark PCR Kit,GE Healthcare Life Sciences的Streptavidin Sepharose High Performance beads,Qiagen的PyroMark 24 Pyrosequencing System。
3.4 多维度样本甲基化差异分析
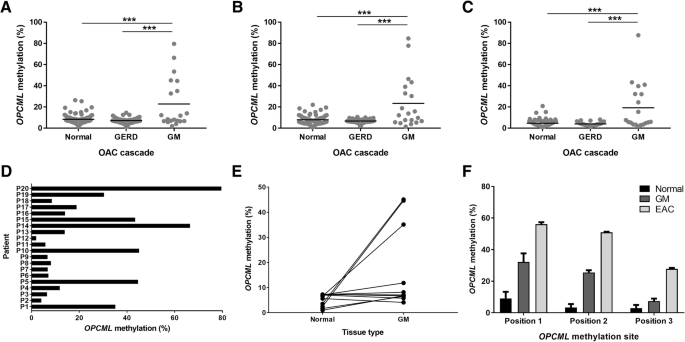
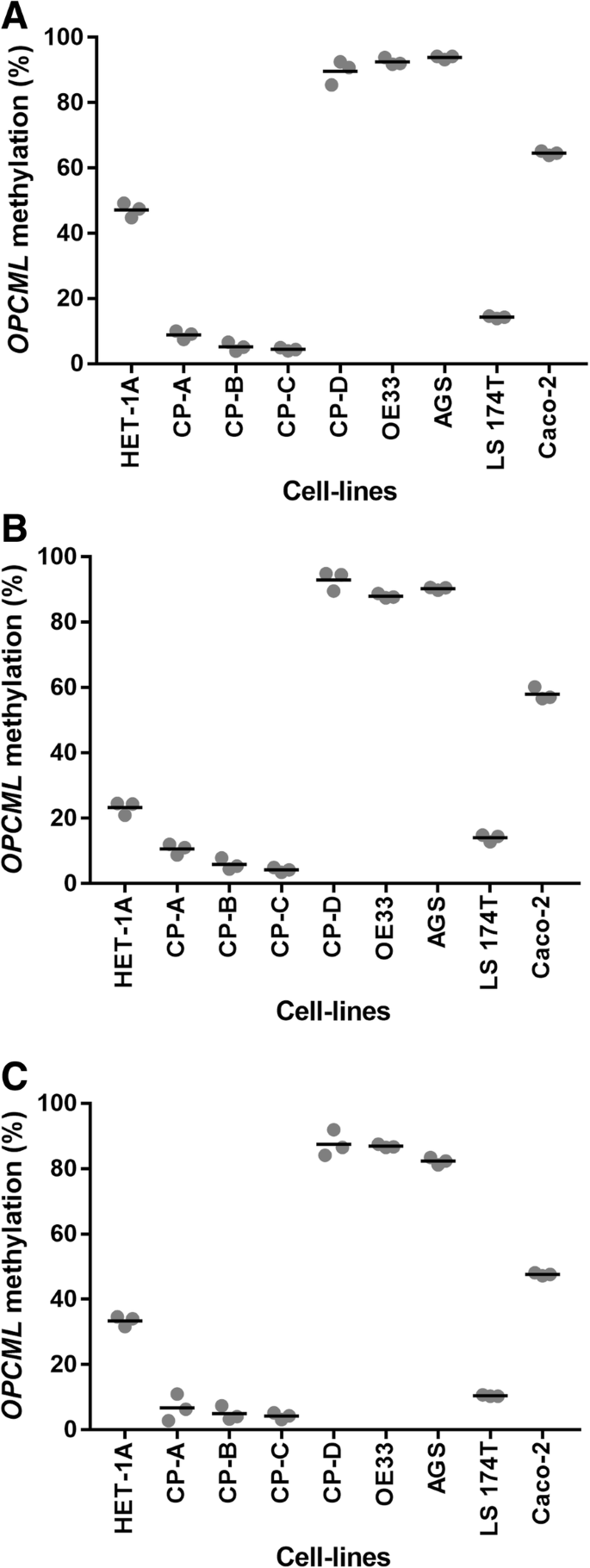
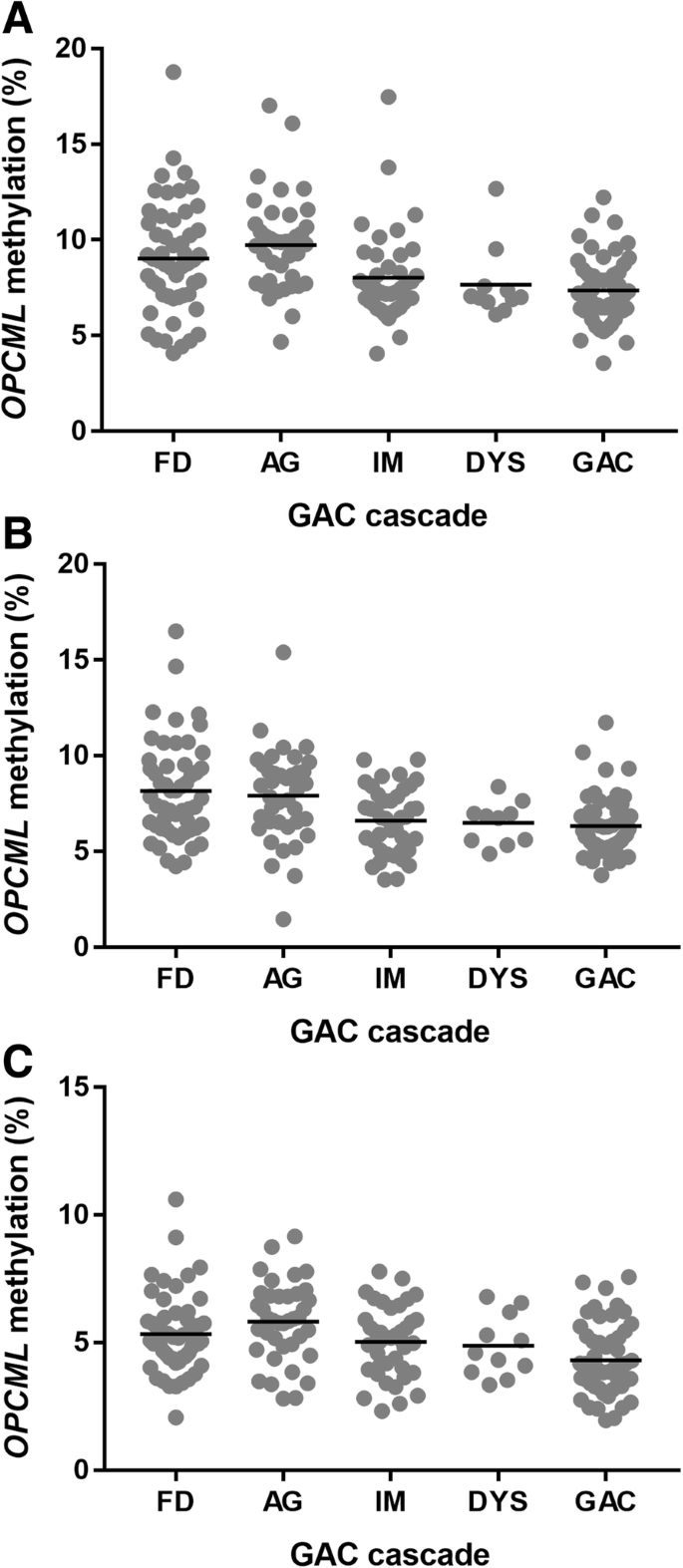
实验目的是明确OPCML甲基化在不同临床样本与细胞系中的表达模式。方法细节:对食管腺癌队列的组织样本、胃腺癌队列的外周血样本、9种细胞系的DNA进行甲基化检测,采用单因素ANOVA结合Tukey事后检验进行组间差异统计分析。结果解读:食管腺黏膜化生患者的OPCML甲基化水平显著高于正常食管与胃食管反流病患者(P<0.05),但该高甲基化仅存在于部分化生患者亚群;11名化生患者的相邻正常组织未检测到高甲基化,提示甲基化改变具有病变局部特异性;单例食管腺癌患者的组织样本显示,OPCML甲基化水平随病变进展逐步升高(正常组织<化生组织<腺癌组织)。细胞系层面,食管腺癌系OE33、胃癌系AGS甲基化水平最高,异型增生细胞系CP-D的甲基化水平与OE33相当,而正常来源的HET-1A细胞系存在中等水平甲基化,与该细胞系已报道的异型增生特征一致。胃腺癌队列的外周血样本中,各病变阶段的OPCML甲基化水平无显著差异,与正常组织水平一致,提示该标志物仅适用于局部组织检测。
4. Biomarker 研究及发现成果解析
Biomarker定位
本研究聚焦的Biomarker为OPCML外显子1的CpG位点高甲基化,筛选与验证逻辑遵循“临床队列初筛→细胞系验证→外周血排除”的路径:首先通过食管腺癌队列组织样本筛选出化生患者亚群的高甲基化特征,随后利用食管腺癌级联细胞系验证甲基化与病变阶段的关联,最后通过胃腺癌队列外周血样本排除其作为全身性标志物的可能,明确其局部组织特异性。
研究过程详述
该Biomarker的来源为食管局部组织样本,验证方法为定制化焦磷酸测序法,精准检测OPCML外显子1的3个CpG位点甲基化水平。特异性方面,仅在食管化生患者亚群中检测到高甲基化,相邻正常组织无高甲基化改变,提示其具有病变局部特异性;敏感性方面,该亚群患者的甲基化水平显著高于正常食管与胃食管反流病患者(P<0.05),可有效区分化生亚群与良性病变人群。目前缺乏大样本验证的ROC曲线AUC值、敏感性与特异性具体数值(文献未明确提供该数据,基于图表趋势推测),但单例腺癌患者的组织样本显示甲基化水平随病变进展逐步升高,支持其作为癌前病变标志物的潜力。
核心成果提炼
本研究首次发现OPCML外显子1高甲基化存在于食管化生患者亚群中,提示该甲基化改变可能与早期异型增生事件相关,可作为食管腺癌早期筛查的潜在局部生物标志物;细胞系结果进一步证实高甲基化与异型增生及腺癌阶段的关联,为其作为癌前病变标志物提供了细胞水平证据;外周血样本的阴性结果明确了该标志物仅适用于局部组织检测,避免了临床应用的误判。该成果填补了OPCML甲基化在食管腺癌癌前病变阶段的研究空白,为食管腺癌早期筛查标志物的开发提供了新的候选靶点,后续需大样本队列验证其敏感性与特异性,明确其临床应用价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。