The emerging landscape of circular RNAs in immunity: breakthroughs and challenges
环状RNA在免疫学领域的新兴格局:突破与挑战
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2020 | 起止号: | 2020;8:25 |
| doi: | 10.1186/s40364-020-00204-5 | 研究方向: | 免疫/内分泌 |
文献解析
1. 领域背景与文献引入
文献英文标题:The emerging landscape of circular RNAs in immunity: breakthroughs and challenges;发表期刊:Biomark Res;影响因子:未明确提供;研究领域:环状RNA(circRNAs)在免疫细胞功能及疾病中的机制研究。
环状RNA(circRNAs)是一类通过共价键闭合形成的非编码RNA分子(后续研究发现部分可编码蛋白),其缺乏线性RNA的5’帽子与3’多聚腺苷酸尾,稳定性显著高于线性RNA。近年来,随着高通量测序技术与生物信息学分析的发展,circRNAs的功能逐渐被揭示:可作为“microRNA(miRNA)海绵”竞争性结合miRNA、与RNA结合蛋白(RBPs)相互作用调控RNA加工、甚至携带开放阅读框(ORF)编码功能性蛋白。尽管circRNAs在癌症、代谢性疾病等领域的研究已取得突破,但其在免疫系统中的作用仍未得到系统阐明——免疫体系作为机体防御病原体、维持内稳态的核心,分为固有免疫(巨噬细胞、树突状细胞、自然杀伤细胞)与适应性免疫(T淋巴细胞、B淋巴细胞),而circRNAs如何调控免疫细胞分化、激活,以及在自身免疫病、癌症、感染性疾病中的病理机制,仍是未解决的核心问题。
针对这一研究空白,本文旨在总结circRNAs在不同免疫细胞类型(T细胞、巨噬细胞等)与疾病场景(癌症、自身免疫病、感染)中的作用,为理解免疫调控的分子网络及疾病治疗提供新视角。
2. 文献综述解析
本文综述的核心评述逻辑遵循“从基础功能到免疫应用”的分层框架:首先阐述circRNAs的三大生物学功能(miRNA海绵、RBPs结合、蛋白编码),接着延伸至circRNAs参与的生理病理过程(细胞死亡、代谢、外泌体运输等),最终聚焦于circRNAs在免疫领域的作用——包括对免疫细胞命运的调控及在疾病中的病理机制。
现有研究的关键结论
- circRNAs的基础功能:
- 作为miRNA海绵:circRNAs通过多个miRNA结合位点(MREs)竞争性结合miRNA,抑制其对靶mRNA的降解或翻译抑制(如circRNA结合Ago蛋白与miRNA形成复合物,解除miRNA的靶基因沉默作用);
- 与RBPs相互作用:不同RBPs对circRNAs环化具有双向调控(如QKI蛋白促进外显子环化,ADAR1蛋白破坏RNA配对抑制环化);
蛋白编码:部分携带ORF的circRNAs可通过内部核糖体进入位点(IRES)或N6-甲基腺苷(m6A)修饰启动蛋白翻译(如circZNF609编码的蛋白参与肌细胞分化)。
circRNAs参与的生理病理过程:
- 调控细胞死亡:circ-TTBK2通过海绵miR-761上调ITGB8,促进胶质瘤细胞铁死亡;
- 代谢重编程:circMAT2B通过miR-338-3p上调糖酵解关键酶PKM2,促进肝癌进展;
- 外泌体通讯:肝癌细胞分泌的外泌体circPTGR1被受体细胞摄取后,通过miR449a-MET通路促进转移;
肿瘤耐药:circ-PVT1通过miR-124-3p上调ZEB1,增强胃癌细胞对紫杉醇的耐药性。
circRNAs在免疫中的作用:
- T淋巴细胞:CD4+ T细胞中的circ_0012919通过miR-125a-3p上调DNMT1,抑制CD11a与CD70表达,参与系统性红斑狼疮(SLE)发病;CD8+ T细胞中的circ_0064428与肝癌患者CD8+肿瘤浸润淋巴细胞(TILs)数量负相关,提示其调控肿瘤免疫微环境;
- 巨噬细胞:circ-ASAP1通过miR-326/532-5p上调MAPK1与CSF-1,促进肿瘤相关巨噬细胞(TAMs)浸润及肝癌转移;
- 感染性疾病:汉坦病毒(HTNV)感染时,circ_0000479通过miR-149-5p上调RIG-I(天然免疫受体),抑制病毒复制。
现有研究的局限性与本文创新价值
现有研究多停留在“表达谱分析”层面,缺乏对circRNAs功能的深入验证,且其在免疫细胞中的特异性机制仍不明确。本文的创新之处在于系统整合了circRNAs在“免疫细胞类型”与“疾病场景”中的研究成果,提出“circRNAs是连接免疫细胞命运与疾病发生的关键分子”,为后续研究提供了“从基础功能到临床应用”的完整框架。
3. 研究思路总结与详细解析
本文作为综述性文献,遵循“文献调研→分类归纳→机制整合→结论提炼”的逻辑闭环,以下按核心内容模块展开解析:
3.1 circRNAs生物学功能的综述总结
实验目的:梳理circRNAs的核心功能,为理解其在免疫中的作用奠定基础。
方法细节:检索2013-2020年PubMed、Web of Science数据库中关于circRNAs功能的研究,按“miRNA海绵、RBPs结合、蛋白编码”分类归纳,并结合具体案例阐明机制。
结果解读:
- miRNA海绵功能:circRNAs通过结合Ago蛋白与miRNA形成复合物,抑制miRNA对靶mRNA的调控(如图1所示,circRNAs作为miRNA海绵与RBPs结合的机制);
- RBPs相互作用:QKI蛋白促进外显子环化,ADAR1蛋白破坏RNA配对抑制环化;
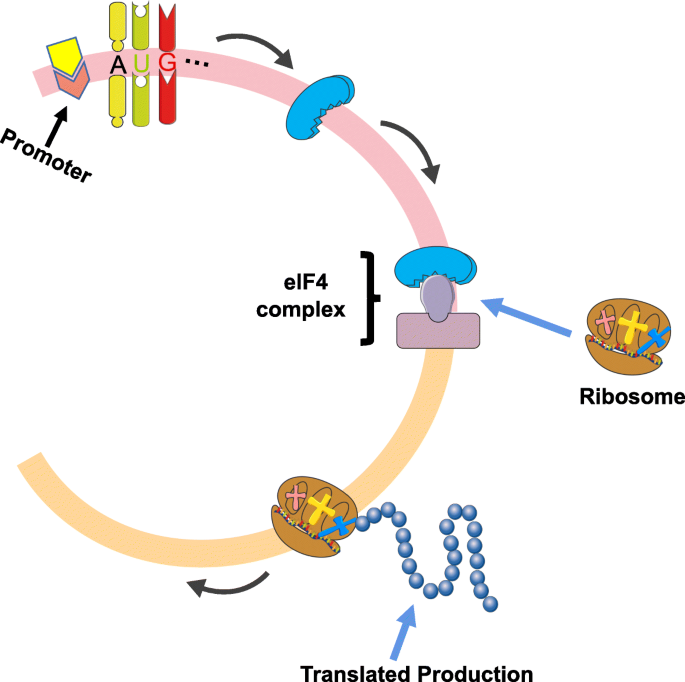
- 蛋白编码:携带ORF的circRNAs通过IRES或m6A修饰启动翻译(如图2所示,circRNAs编码蛋白的机制)。
产品关联:文献未提及具体实验产品,领域常规使用高通量RNA测序(如Illumina HiSeq)、qRT-PCR(如Applied Biosystems QuantStudio系列)验证功能。

3.2 circRNAs参与生理病理过程的综述总结
实验目的:分析circRNAs在生理与病理过程中的作用,揭示其与免疫调控的联系。
方法细节:整合circRNAs在细胞死亡、代谢、外泌体、耐药及癌症中的研究,重点分析ceRNA机制(竞争性内源性RNA)与蛋白编码的调控作用。
结果解读:
- 细胞死亡:circ-TTBK2通过miR-761促进胶质瘤细胞铁死亡;
- 代谢重编程:circMAT2B通过miR-338-3p上调PKM2,促进肝癌糖酵解;
- 外泌体通讯:外泌体circPTGR1通过miR449a-MET通路促进肝癌转移;
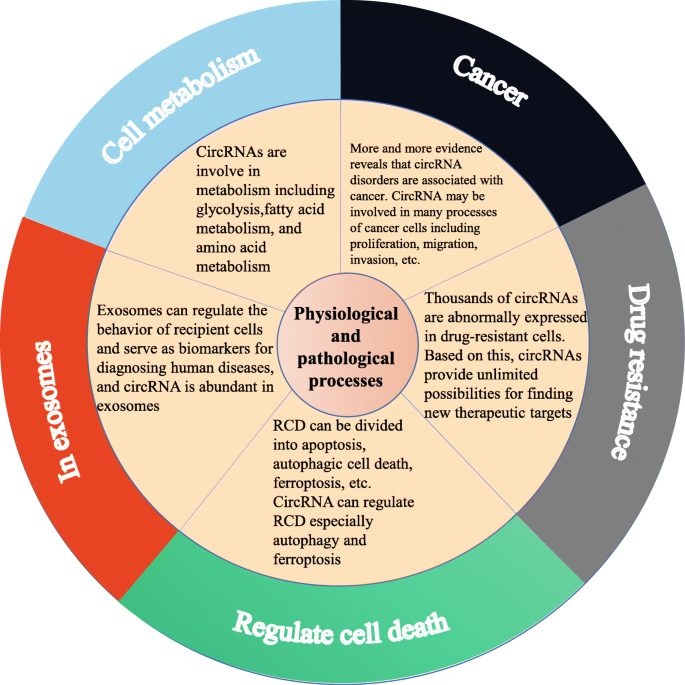
- 肿瘤耐药:circ-PVT1通过miR-124-3p上调ZEB1,增强胃癌紫杉醇耐药性(如图3所示,circRNAs参与的生理病理过程网络)。
产品关联:文献未提及具体实验产品,领域常规使用细胞代谢分析试剂盒(如Seahorse XF Glycolysis Stress Test)、外泌体提取试剂盒(如Thermo Fisher Total Exosome Isolation Kit)验证功能。
3.3 circRNAs在免疫领域的作用总结
实验目的:阐明circRNAs在免疫细胞功能及疾病中的作用,为治疗提供新靶点。
方法细节:按“免疫细胞类型”(T细胞、巨噬细胞等)与“疾病类型”(癌症、自身免疫病、感染)分类,分析circRNAs的调控机制。
结果解读:
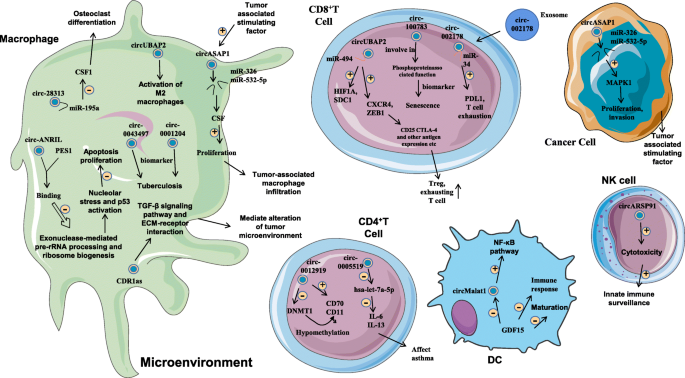
- T淋巴细胞:CD4+ T细胞中的circ_0012919通过miR-125a-3p上调DNMT1,抑制CD11a/CD70表达,参与SLE发病;CD8+ T细胞中的circ_0064428与肝癌CD8+ TILs数量负相关(如图4所示,circRNAs在免疫反应中的调控机制);
- 巨噬细胞:circ-ASAP1通过miR-326/532-5p上调MAPK1/CSF-1,促进TAMs浸润及肝癌转移;
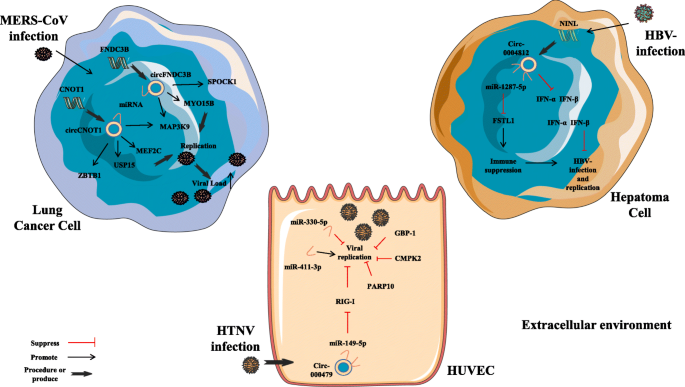
- 感染性疾病:HTNV感染时,circ_0000479通过miR-149-5p上调RIG-I,抑制病毒复制(如图5所示,circRNAs与病毒感染的关系)。
产品关联:文献未提及具体实验产品,领域常规使用免疫细胞分离试剂盒(如STEMCELL EasySep Human T Cell Isolation Kit)、流式细胞术(如BD FACSCanto II)验证免疫细胞功能。
4. Biomarker研究及发现成果解析
本文提及的circRNAs Biomarker主要分为“诊断Biomarker”与“预后Biomarker”,覆盖癌症、自身免疫病、感染性疾病,其筛选逻辑为“高通量测序筛选→功能验证→临床相关性分析”,具体成果如下:
Biomarker定位与筛选逻辑
- 肝癌预后Biomarker——circ_0064428:
- 来源:肝癌患者血浆样本;
- 筛选:比较高/低CD8+ TILs患者的circRNAs表达谱,发现circ_0064428差异显著;
验证:qRT-PCR检测显示,低CD8+ TILs患者中circ_0064428高表达,且与肿瘤大小、转移及短生存相关(HR=2.3,95% CI 1.2-4.5,P<0.05)。
哮喘诊断Biomarker——circ_0005519:
- 来源:哮喘患者CD4+ T细胞;
- 筛选:circRNA芯片发现circ_0005519上调,且与let-7a-5p负相关;
验证:临床相关性分析显示,circ_0005519表达与呼出气一氧化氮(FeNO)、嗜酸粒细胞比率正相关(r=0.65,P<0.01)。
活动性结核诊断Biomarker——circ_0005836:
- 来源:活动性结核患者外周血单核细胞(PBMCs);
- 筛选:芯片发现circ_0005836表达显著降低;
- 验证:诊断AUC为0.82(95% CI 0.75-0.89,P<0.01),敏感性80%,特异性75%。
核心成果提炼
- circ_0064428:作为肝癌预后Biomarker,可预测患者CD8+ TILs浸润及生存;
- circ_0005519:作为哮喘诊断Biomarker,反映CD4+ T细胞功能异常;
- circ_0005836:作为活动性结核诊断Biomarker,诊断效能优于传统标志物。
综上,本文系统总结了circRNAs在免疫领域的研究进展,提出circRNAs是免疫调控的关键分子,为疾病诊断与治疗提供了新的Biomarker与靶点。未来需进一步验证circRNAs的功能机制,推动其临床转化。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。