Plasma contact factors as novel biomarkers for diagnosing Alzheimer's disease
血浆接触因子作为诊断阿尔茨海默病的新型生物标志物
| 期刊: | Biomarker Research | 影响因子: | 9.500 |
| 时间: | 2021 | 起止号: | 2021 Jan 9;9(1):5. |
| doi: | 10.1186/s40364-020-00258-5 | 方法学: | ELISA |
| 研究方向: | 神经 | 疾病类型: | 阿尔茨海默症 |
文献解析
1. 领域背景与文献引入
文献英文标题:Plasma contact factors as novel biomarkers for diagnosing Alzheimer’s disease;发表期刊:Biomarker Research;影响因子:未公开;研究领域:神经退行性疾病(阿尔茨海默病)
阿尔茨海默病(AD)是全球最常见的痴呆类型,占所有痴呆病例的60%-80%,自1906年首次被报道以来,领域内的关键研究节点包括20世纪80年代淀粉样蛋白假说的提出、21世纪初脑脊液生物标志物(β淀粉样蛋白1-42(Aβ1-42)、总tau(t-Tau)、磷酸化tau181(p-Tau181))的临床应用,以及近年血液生物标志物的探索热潮。当前研究热点聚焦于开发微创、高准确性的早期AD诊断标志物,因为现有脑脊液标志物采样有创,患者接受度低,且早期AD的干预是延缓疾病进展的核心,但领域内仍存在未解决的关键问题:现有血液生物标志物的诊断特异性和敏感性不足,无法有效区分AD的不同临床阶段;血浆接触系统与AD病理进展的直接关联尚未在大样本临床队列中得到验证,缺乏可用于临床诊断的明确cutoff值。
结合领域现状,本研究针对的核心问题是明确血浆接触系统激活与AD临床进展的关联,并探索其作为AD诊断生物标志物的可行性,其学术价值在于填补了血浆接触因子在AD临床诊断应用中的空白,为AD的早期无创诊断提供了新的候选标志物,有望推动AD早期筛查的临床普及。
2. 文献综述解析
作者对领域内现有研究的分类维度主要分为两类:一类是AD经典脑脊液生物标志物的研究,另一类是血浆接触系统与AD病理关联的初步探索。
现有AD经典脑脊液生物标志物的研究结论显示,Aβ1-42水平降低、t-Tau和p-Tau181水平升高与AD进展密切相关,这些标志物的检测已成为AD临床诊断的重要依据,其优势在于能直接反映脑内的病理变化,但局限性在于脑脊液采样属于有创操作,患者接受度低,且无法实现大规模人群的早期筛查。关于血浆接触系统与AD的关联研究,现有研究多基于小鼠模型或少量人类脑脊液样本,提出接触系统激活可能参与AD的血管异常和神经炎症病理过程,但这些研究缺乏大样本临床队列的验证,未提供可用于区分不同AD临床阶段的诊断cutoff值,无法直接应用于临床实践。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次在包含101例受试者的临床队列中,直接验证了血浆接触因子活性与AD临床进展的相关性,明确了FXIIa作为血浆生物标志物的诊断效能,并提出了脑脊液Aβ1-42与FXIIa的比值,显著提升了AD不同阶段的诊断准确性,尤其是实现了AD痴呆的完美诊断(AUC=1.0),为AD的早期无创诊断提供了新的可行方案。
3. 研究思路总结与详细解析
整体框架概括:本研究的核心目标是明确血浆接触系统激活与阿尔茨海默病(AD)临床进展的关联,筛选并验证可用于AD不同阶段诊断的新型血浆生物标志物;核心科学问题是血浆接触因子活性是否能有效区分正常人群、前驱期AD和AD痴呆患者;技术路线遵循“临床队列构建→生物标志物检测→统计关联分析→诊断效能验证”的闭环逻辑,通过大样本临床数据验证假设,最终确定具有临床应用价值的生物标志物及cutoff值。
3.1 临床样本队列构建与基线特征分析
实验目的:建立标准化的AD临床队列,明确不同阶段AD患者的基线生物标志物特征,为后续研究提供可靠的临床样本基础。
方法细节:研究招募了来自韩国光州和全罗南道的101名受试者,时间范围为2015年8月至2017年10月,所有受试者均签署知情同意书,研究方案经伦理委员会批准。依据IWG-2指南结合淀粉样PET结果,将受试者分为三组:50名正常老年人、23名前驱期AD患者、28名AD痴呆患者,排除淀粉样PET阳性的正常受试者(AD临床前期)和淀粉样PET阴性的轻度认知障碍(MCI)患者,确保队列的病理诊断准确性。
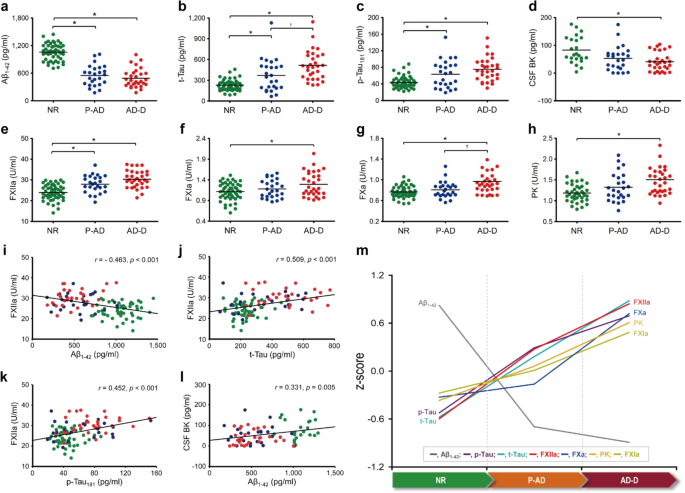
结果解读:队列的基线生物标志物检测结果显示,随着AD进展,脑脊液Aβ1-42水平逐渐降低(正常组1059 pg/ml,前驱AD组550 pg/ml,AD痴呆组484 pg/ml),而t-Tau和p-Tau181水平逐渐升高(t-Tau:正常组230 pg/ml,前驱AD组389 pg/ml,AD痴呆组536 pg/ml;p-Tau181:正常组44 pg/ml,前驱AD组66 pg/ml,AD痴呆组78 pg/ml),与既往AD研究的经典结论一致,验证了队列的可靠性。
产品关联:文献未提及具体实验产品,领域常规使用ELISA试剂盒检测脑脊液生物标志物,酶标仪进行吸光度检测。
3.2 血浆接触因子活性检测方法的建立与验证
实验目的:建立可靠的血浆接触因子活性检测方法,确保检测结果的准确性和可重复性,为后续的关联分析提供技术支撑。
方法细节:采用重组接触因子(FXIIa、FXIa、PK)和FXa酶制备标准曲线,通过系列稀释不同浓度的因子,与对应的特异性合成肽底物混合(S-2302用于FXIIa,S-2366用于FXIa,S-2765用于FXa,H-D-Val-Leu-Arg-AFC用于激肽释放酶),在37℃孵育30分钟后,用酶标仪检测吸光度或荧光强度,建立四参数拟合的标准曲线。同时,通过检测不同批次样本的变异系数(CV%)验证方法的精密度和可重复性。
结果解读:标准曲线的R²值均高于0.95,表明检测方法的线性关系良好;FXIIa的批内和批间变异系数分别为7.2%-12.7%和3.2%-4.5%,显示检测方法具有良好的精密度和可重复性,可用于后续的大样本检测。
产品关联:文献未提及具体实验产品,领域常规使用合成肽底物检测蛋白酶活性,多功能酶标仪进行吸光度或荧光检测。
3.3 血浆接触因子活性与AD临床进展的关联分析
实验目的:明确血浆接触系统激活与AD临床进展的相关性,探索接触因子活性与经典AD生物标志物的关联。
方法细节:检测三组受试者血浆中FXIIa、FXIa、FXa和激肽释放酶(PK)的活性,同时检测脑脊液中缓激肽(BK)的浓度,采用方差分析(ANOVA)比较三组间的差异,通过Pearson相关分析探索接触因子活性与经典脑脊液AD生物标志物的相关性。
结果解读:随着AD进展,血浆FXIIa、FXIa、FXa和PK的活性均显著升高(FXIIa:正常组23.9 U/ml,前驱AD组28.0 U/ml,AD痴呆组30.6 U/ml;FXIa:正常组1.11 U/ml,前驱AD组1.18 U/ml,AD痴呆组1.30 U/ml;FXa:正常组0.77 U/ml,前驱AD组0.81 U/ml,AD痴呆组0.97 U/ml;PK:正常组1.20 U/ml,前驱AD组1.35 U/ml,AD痴呆组1.54 U/ml),组间差异具有统计学意义(P<0.05)。脑脊液BK浓度随AD进展降低,而血浆BK浓度升高,提示BK可能通过血脑屏障渗漏参与AD病理。相关性分析显示,FXIIa活性与脑脊液Aβ1-42呈负相关(r=-0.463,P<0.05),与t-Tau(r=0.509,P<0.05)和p-Tau181(r=0.452,P<0.05)呈正相关,表明血浆FXIIa活性与AD病理进展密切相关。
产品关联:文献未提及具体实验产品,领域常规使用ELISA试剂盒检测缓激肽浓度,酶标仪进行吸光度检测。
3.4 生物标志物诊断效能分析与cutoff值确定
实验目的:验证血浆接触因子及相关比值作为AD诊断生物标志物的效能,确定可用于临床诊断的cutoff值。
方法细节:采用受试者工作特征(ROC)曲线分析各生物标志物的诊断效能,计算曲线下面积(AUC)、敏感性和特异性,确定区分正常人群与前驱AD、正常人群与AD痴呆的最佳cutoff值。
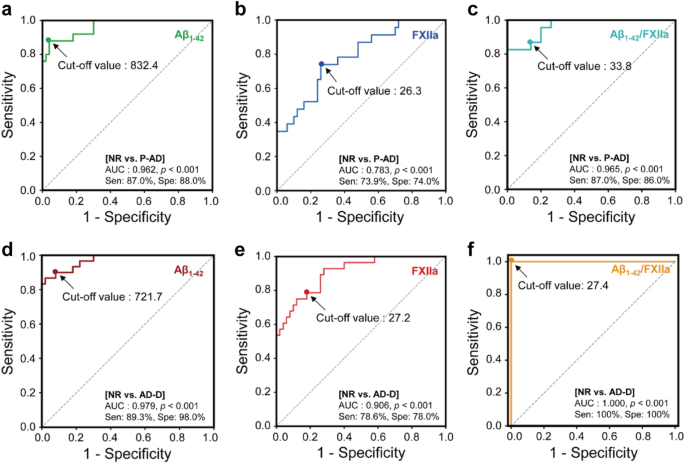
结果解读:ROC曲线分析显示,FXIIa区分前驱AD的AUC为0.783,最佳cutoff值为>26.3 U/ml;区分AD痴呆的AUC为0.906,最佳cutoff值为>27.2 U/ml。而脑脊液Aβ1-42与FXIIa的比值具有更高的诊断效能,区分前驱AD的AUC为0.965,最佳cutoff值为<33.8;区分AD痴呆的AUC为1.0,最佳cutoff值为<27.44,实现了AD痴呆的完美诊断。
产品关联:文献未提及具体实验产品,领域常规使用SPSS等统计软件进行ROC曲线分析。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的生物标志物包括血浆FXIIa活性,以及脑脊液Aβ1-42与血浆FXIIa的比值(Aβ1-42/FXIIa)。筛选与验证逻辑为:首先通过大样本临床队列检测,明确血浆接触因子活性与AD临床进展的相关性,然后通过ROC曲线分析验证其诊断效能,最终确定可区分不同AD临床阶段的最佳cutoff值,形成“临床关联→效能验证→cutoff确定”的完整逻辑链条。
研究过程详述
生物标志物的样本来源为101例受试者的血浆和脑脊液样本,其中血浆样本按照Molecular Medicine Ireland(MMI)标准化生物样本库指南收集和储存。血浆FXIIa活性采用特异性合成肽底物S-2302检测,通过酶标仪检测吸光度变化计算活性;脑脊液Aβ1-42采用INNOTEST ELISA试剂盒检测。特异性与敏感性数据显示,FXIIa区分前驱AD的AUC为0.783(P<0.001),对应cutoff值>26.3 U/ml;区分AD痴呆的AUC为0.906(P<0.001),对应cutoff值>27.2 U/ml。而Aβ1-42/FXIIa比值区分前驱AD的AUC为0.965(P<0.001),对应cutoff值<33.8;区分AD痴呆的AUC为1.0(P<0.001),对应cutoff值<27.44,具有完美的诊断效能。
核心成果提炼
本研究发现血浆FXIIa活性与AD临床进展密切相关,可作为AD早期诊断的新型血浆生物标志物,其作为独立诊断标志物时,对AD痴呆的诊断准确性较高(AUC=0.906)。而脑脊液Aβ1-42与FXIIa的比值显著提升了诊断效能,尤其是对AD痴呆的诊断实现了AUC=1.0的完美效能,提示该比值可作为AD不同阶段诊断的高准确性标志物。创新性在于首次在大样本临床队列中明确了血浆接触系统激活与AD进展的直接关联,提出了可用于临床诊断的具体cutoff值,为AD的早期无创诊断提供了新的可行方案。统计学结果显示,所有组间差异及cutoff值对应的分析均具有高度统计学意义(P<0.001),表明结果具有可靠的学术价值。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。