Advancement in Multi-omics approaches for Uterine Sarcoma
子宫肉瘤多组学方法的研究进展
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2024 | 起止号: | 2024 Oct 29;12(1):129 |
| doi: | 10.1186/s40364-024-00673-y | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Advancement in Multi-omics approaches for Uterine Sarcoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:子宫肉瘤的多组学研究。
子宫肉瘤(Uterine Sarcoma, US)是女性生殖系统罕见的恶性肿瘤,占女性生殖道恶性肿瘤的1%、子宫肿瘤的3%~7%。其临床挑战突出:缺乏特异性生物标志物,术前影像学(超声、CT、PET-CT)难以区分良性子宫平滑肌瘤(ULM)与恶性US,约0.5%的ULM手术患者术后才确诊为US,可能导致“肿瘤腹膜种植”;复发率高(53%~71%),预后极差(5年生存率仅15%~25%,中位生存时间约10个月);治疗以手术为主,放化疗作为辅助或姑息治疗,但效果有限。
随着“组学”概念与下一代测序(NGS)、高分辨率质谱等技术的进步,生命科学研究从传统单一组学(如基因组)转向多组学整合——通过基因组、表观组、转录组、蛋白组、代谢组的系统分析,结合计算机技术解析致病基因、关键通路及分子标志物,为精准诊断与个性化治疗提供依据。针对US临床诊断与治疗的痛点,研究人员尝试用多组学技术绘制其分子景观,本文旨在总结多组学在US中的最新进展,讨论挑战与前景。
2. 文献综述解析
本文综述的核心逻辑是按US病理亚型(子宫平滑肌肉瘤uLMS、子宫内膜间质肉瘤ESS、未分化子宫肉瘤UUS、腺肉瘤AS)与多组学类型(基因组、表观组、转录组、蛋白组、代谢组)分类,系统评述现有研究的成果与不足。
现有研究的关键结论
- 病理亚型的分子特征:uLMS常见TP53、RB1、ATRX基因突变及TERT、C-MYC拷贝数扩增;低级别ESS(LG-ESS)存在JAZF1-SUZ12基因融合,高级别ESS(HG-ESS)存在YWHAE-FAM22A/B融合;UUS常出现BRG1/SMARCA4突变;AS存在8q13扩增、MYBL1拷贝数变异。
- 多组学的应用价值:基因组学揭示US的基因突变与拷贝数变化;表观组学发现uLMS的DNA甲基化模式异于其他肉瘤,miR-10b-5p等非编码RNA调控细胞增殖;转录组学将uLMS分为低级别(平滑肌功能基因过表达)与高级别(EMT相关基因过表达)亚型;蛋白组学发现MVP、RCN1等差异蛋白;代谢组学识别醋酸盐、甘油三酯等预后标志物。
现有研究的优势与不足
优势:多组学技术深入揭示了US的分子机制,为分子分型与生物标志物(Biomarker)发现提供了基础;不足:样本量小(US罕见)、单组学研究多、多组学整合少,部分Biomarker缺乏大规模临床验证,单细胞与空间组学应用有限。
文献的创新价值
本文整合了多组学在US中的最新应用,涵盖基因组、表观组、转录组、蛋白组、代谢组,同时讨论了单细胞组学、空间组学及人工智能(AI)的潜力,弥补了现有研究中“多组学整合不足”的短板,为US的精准医学研究提供了全面参考框架。
3. 研究思路总结与详细解析
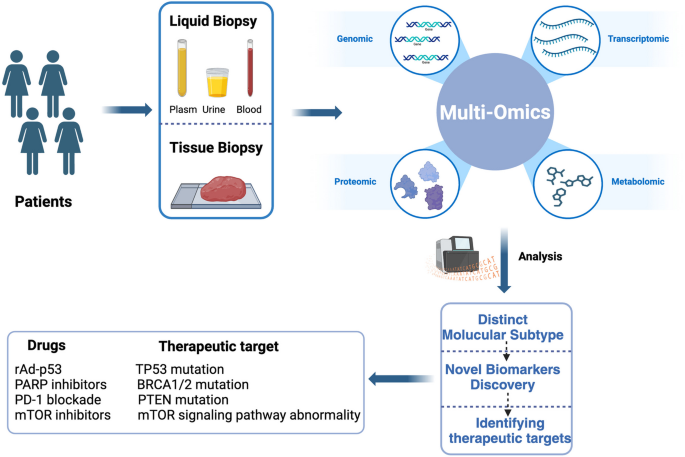
本文作为综述,总结了现有US多组学研究的核心思路:样本收集→多组学测序→数据分析→结果应用(分子分型、Biomarker筛选、治疗靶点发现)。以下按关键实验环节解析:
3.1 样本来源与制备
实验目的:获取US患者的生物样本,为多组学分析提供材料。
方法细节:样本主要来自手术切除的子宫组织(新鲜冷冻FF或福尔马林固定石蜡包埋FFPE样本),部分来自液体活检(外周血、胸腔积液的循环游离DNA cfDNA、循环肿瘤DNA ctDNA)。
结果解读:FF/FFPE样本用于基因组、转录组等组学分析;液体活检作为非侵入性方法,可动态监测肿瘤进展。
产品关联:文献未提及具体实验产品,领域常规使用样本保存试剂(如RNAlater)、cfDNA提取试剂盒(如Qiagen QIAamp Circulating Nucleic Acid Kit)等。
3.2 基因组学测序分析
实验目的:解析US的基因突变、拷贝数变异(CNV)与基因融合事件。
方法细节:采用全基因组测序(WGS)、全外显子测序(WES)等技术分析US样本的基因组变异。
结果解读:
- uLMS:发现TP53(56%)、RB1(51%)、ATRX(31%)等基因突变,TERT(5p15.33)、C-MYC(8q24.21)等拷贝数扩增,及ACTG2-ALK融合基因;
- LG-ESS:常见t(7;17)(p15;q21)易位导致JAZF1-SUZ12融合;
- HG-ESS:存在YWHAE-FAM22A/B、ZC3H7B-BCOR融合及BCOR内部串联重复(ITD);
- UUS:发现BRG1/SMARCA4突变;
- AS:存在8q13扩增、MYBL1拷贝数变异。
这些结果明确了US不同亚型的基因组特征,为分子分型提供了依据。
产品关联:文献未提及具体实验产品,领域常规使用基因组测序仪(如Illumina NovaSeq)、PCR试剂盒(如TaKaRa Ex Taq)等。

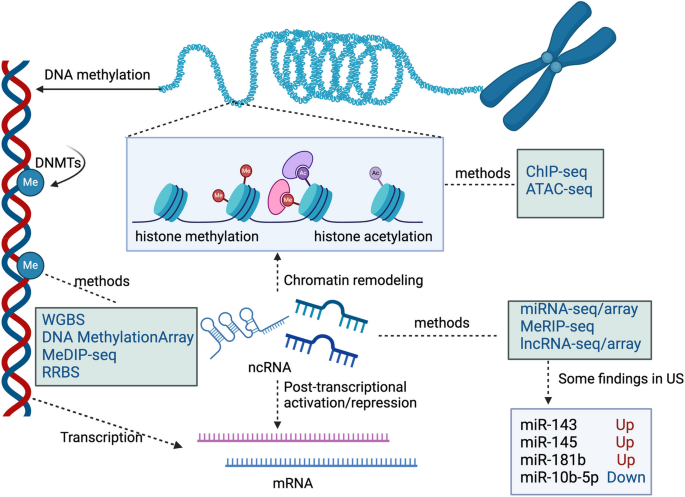
3.3 表观组学分析
实验目的:研究US的DNA甲基化与非编码RNA变化。
方法细节:采用DNA甲基化阵列(如Illumina Infinium HumanMethylation450 BeadChip)分析甲基化模式,采用miRNA测序(miRNA-seq)分析非编码RNA表达。
结果解读:
- DNA甲基化:TCGA数据显示uLMS的甲基化模式异于其他软组织肉瘤;复发的平滑肌肿瘤不确定恶性潜能(STUMPs)表现为CpG岛(CGIs)普遍低甲基化,与基因组不稳定性相关;
- 非编码RNA:miR-10b-5p在uLMS中表达下调,过表达可抑制肉瘤细胞增殖、阻滞G1→G2/M期;miR-143、miR-145在uLMS中高表达,与平滑肌功能相关。
这些结果揭示了表观遗传调控在US发生中的作用。
产品关联:文献未提及具体实验产品,领域常规使用甲基化阵列试剂盒(如Illumina Infinium)、miRNA提取试剂盒(如Qiagen miRNeasy Mini Kit)等。
3.4 转录组学分析
实验目的:识别US的差异表达基因与分子亚型。
方法细节:采用RNA测序(RNA-seq)分析US样本的转录组谱。
结果解读:
- uLMS:分为两个分子亚型——低级别亚型过表达平滑肌功能基因(LMOD1、SLMAP),高级别亚型过表达EMT与肿瘤发生基因(CDK6、MAPK13),且对化疗反应不同;
- ESS:发现GREB1-NCOA2、GREB1-NR4A3等新融合基因,与性激素通路相关;
- UUS:部分携带NTRK改变的UUS被重新分类为HG-ESS。
这些结果提高了US的诊断准确性。
产品关联:文献未提及具体实验产品,领域常规使用RNA-seq试剂盒(如Illumina TruSeq Stranded mRNA Library Prep Kit)、测序仪(如Illumina HiSeq)等。
3.5 蛋白组与代谢组分析
实验目的:发现US的差异蛋白与代谢标志物。
方法细节:采用质谱(MS)、液相色谱-质谱(LC-MS)分析蛋白与代谢物表达。
结果解读:
- 蛋白组:主要穹窿蛋白(MVP)在uLMS中表达,免疫组化显示其区分uLMS与ULM的敏感性50%、特异性100%;RCN1与阿霉素耐药相关,下调RCN1可增强阿霉素的细胞毒性;CD70在uLMS中过表达,可作为抗体-药物偶联物(ADC)的治疗靶点;
- 代谢组:分析软组织肉瘤样本发现,醋酸盐、甘油三酯、低密度脂蛋白-2(LDL-2)及红细胞计数可预测2年生存率,敏感性84.4%、特异性84.6%。
这些结果为US的诊断与治疗提供了新Biomarker。
产品关联:文献未提及具体实验产品,领域常规使用质谱仪(如Thermo Fisher Q Exactive)、蛋白提取试剂盒(如Thermo Fisher Pierce RIPA Buffer)等。
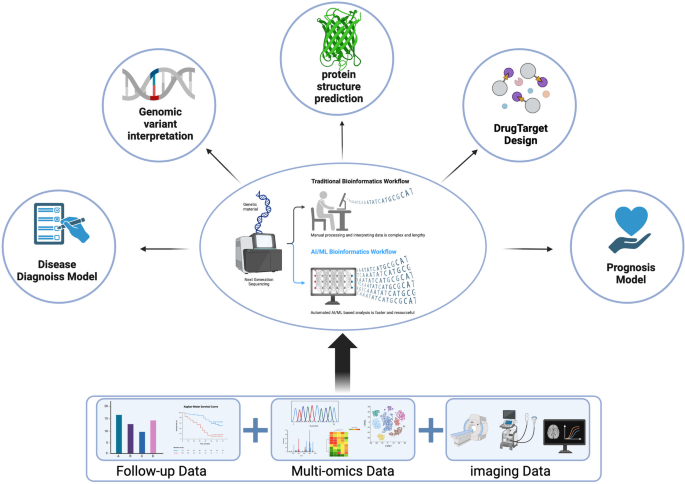
3.6 人工智能与多组学整合
实验目的:利用AI算法整合多组学数据,提高分析效率与准确性。
方法细节:采用机器学习(ML)算法(如LASSO、SVM-RFE)分析基因表达数据,采用深度学习(DL)算法分析医学影像(如MRI)。
结果解读:
- 基因表达分析:通过LASSO与SVM-RFE识别DPP6、MFAP5作为uLMS的诊断Biomarker,与免疫浸润相关;
- 影像组学:利用MRI与ML算法开发术前区分US与ULM的诊断模型,准确性较高。
这些结果展示了AI在多组学整合中的潜力。
产品关联:文献未提及具体实验产品,领域常规使用AI分析软件(如Python的scikit-learn库)、影像分析工具(如ITK-SNAP)等。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本文涉及的Biomarker覆盖基因组、表观组、转录组、蛋白组、代谢组:
- 基因组:TP53、RB1、ATRX突变,JAZF1-SUZ12、YWHAE-FAM22A/B融合;
- 表观组:miR-10b-5p;
- 蛋白组:MVP、RCN1、CD70;
- 代谢组:醋酸盐、甘油三酯、LDL-2。
筛选逻辑:数据库挖掘(如TCGA)→ 细胞系验证→ 临床样本验证。
研究过程与核心成果
- 基因组Biomarker:
- TP53突变:来自TCGA的WES数据,107例uLMS中突变率56%(n=107),免疫组化验证p53蛋白表达与突变相关,是uLMS的不良预后标志物;
JAZF1-SUZ12融合:来自LG-ESS的FISH分析,多个研究验证其为LG-ESS的特异性分子特征。
表观组Biomarker:
miR-10b-5p:来自uLMS与ULM的miRNA-seq,qRT-PCR验证其在uLMS中下调(n=3,P<0.05),细胞实验显示过表达可抑制增殖,是uLMS的潜在诊断标志物。
蛋白组Biomarker:
- MVP:来自uLMS与ULM的蛋白组分析,免疫组化验证其区分uLMS与ULM的敏感性50%、特异性100%(文献未明确样本量);
CD70:来自uLMS的蛋白组分析,细胞实验显示其作为ADC靶点的潜力,为uLMS的靶向治疗提供新方向。
代谢组Biomarker:
- 醋酸盐、甘油三酯等:来自软组织肉瘤的代谢组分析,验证其预测2年生存率的敏感性84.4%、特异性84.6%(文献未明确样本量),是US的预后标志物。
创新与局限
创新点:首次整合多组学解析US的分子景观,发现多个跨组学Biomarker;局限:部分Biomarker(如miR-10b-5p)样本量小,需大规模临床验证;单细胞与空间组学应用有限,未完全揭示肿瘤异质性。
综上,多组学为US的精准诊断与治疗提供了重要依据,但需解决“样本量小、多组学整合难、Biomarker临床转化慢”等问题,未来结合单细胞组学、空间组学与AI技术,有望进一步推动US的精准医学研究。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。