Functions of RNA N(6)-methyladenosine modification in acute myeloid leukemia
RNA N(6)-甲基腺苷修饰在急性髓系白血病中的功能
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2021 | 起止号: | 2021 May 17;9(1):36 |
| doi: | 10.1186/s40364-021-00293-w | 疾病类型: | 白血病 |
文献解析
1. 领域背景与文献引入
文献英文标题:Functions of RNA N⁶-methyladenosine modification in acute myeloid leukemia;发表期刊:Biomark Res;影响因子:未公开;研究领域:急性髓系白血病的RNA表观遗传调控
急性髓系白血病(AML)是成人最常见的急性白血病,以恶性髓系祖细胞浸润骨髓、外周血及其他组织为特征,表现为细胞增殖失控、分化障碍及造血异常。领域共识:尽管现有诊疗技术不断进步,采用标准化疗的AML患者5年生存率仍不足40%,其发病机制中的化疗耐药问题尚未得到充分解析。表观遗传调控作为肿瘤生物学的快速发展领域,通过不改变DNA序列的动态可逆方式调控基因表达,其中DNA甲基化、组蛋白修饰的相关研究已转化为临床治疗方案,如地西他滨等表观药物已用于AML治疗。近年,RNA表观遗传修饰作为新的研究热点逐渐兴起,已发现超过150种RNA修饰类型,其中N⁶-甲基腺苷(m⁶A)是真核生物中最普遍的mRNA内部修饰,参与昼夜节律、脂肪生成等多种生物过程。然而,m⁶A修饰在AML发病机制、白血病干细胞(LSC)自我更新、化疗耐药中的具体调控机制仍不明确,其临床转化应用的潜力也缺乏系统梳理。针对这一研究空白,本综述系统总结了m⁶A RNA甲基化在正常造血、AML发生发展、治疗耐药及LSC干性维持中的最新进展,探讨其作为AML生物标志物及治疗靶点的临床价值。
2. 文献综述解析
作者以m⁶A调控因子的功能类型(写入器、擦除器、读取器)及生物学作用场景(正常造血、AML发生、耐药、LSC干性)为核心分类维度,对领域内现有研究进行结构化评述。现有研究的关键结论显示,m⁶A修饰是一个可逆动态的调控过程,由甲基转移酶(写入器)、去甲基化酶(擦除器)及结合蛋白(读取器)三类蛋白共同调控,通过影响RNA的剪接、稳定性、翻译等过程参与基因表达调控。技术方法层面,MeRIP-seq、miCLIP等测序技术的应用实现了转录组水平m⁶A位点的检测,分辨率从约200核苷酸提升至单核苷酸水平,为解析靶标分子提供了精准工具;但现有研究仍存在局限性,部分调控因子的具体靶标及下游信号通路尚未完全阐明,针对m⁶A调控因子的临床研究多为小样本队列,缺乏大规模多中心验证数据,且除FTO外的其他调控因子的特异性抑制剂仍处于早期研发阶段。
本综述的创新价值在于,首次系统整合了m⁶A从基础分子机制到临床应用的全链条研究成果,重点关联了m⁶A调控因子与AML患者临床特征的相关性,填补了此前综述在临床转化方向的内容空白。通过对比现有研究中未解决的核心问题,如m⁶A调控因子在不同AML亚型中的特异性作用、与基因突变的协同机制等,本综述明确了未来研究的关键方向,为m⁶A作为AML生物标志物及治疗靶点的转化应用提供了系统的理论支撑。
3. 研究思路总结与详细解析
本研究整体框架为:先系统阐述m⁶A RNA甲基化的核心调控系统(写入器、擦除器、读取器)的分子机制,再分别解析其在正常造血、AML发生发展、治疗耐药、LSC干性维持中的生物学功能,最后探讨其在AML中的临床应用潜力,形成从基础到临床的完整逻辑闭环。
3.1 m⁶A调控系统的分子机制解析
实验目的:明确m⁶A RNA甲基化的写入、擦除及读取过程,阐明三类核心调控蛋白的结构与功能。
方法细节:通过总结领域内已发表的结构生物学、分子生物学研究,系统梳理写入器复合物(核心组分METTL3、METTL14、WTAP及辅助蛋白RBM15、VIRMA等)、擦除器(FTO、ALKBH5、ALKBH3)、读取器(YTH家族、HNRNP家族、IGF2BP家族)的蛋白相互作用、亚细胞定位及作用模式。
结果解读:写入器复合物中METTL3为唯一催化亚基,与METTL14形成异二聚体,WTAP增强其催化活性并引导复合物定位至核斑点;擦除器中FTO可同时作用于m⁶A及m⁶Aₘ修饰,ALKBH5特异性作用于m⁶A;读取器通过识别m⁶A位点调控RNA的剪接、稳定性及翻译,如YTHDF2介导靶mRNA降解,YTHDF1促进靶mRNA翻译。
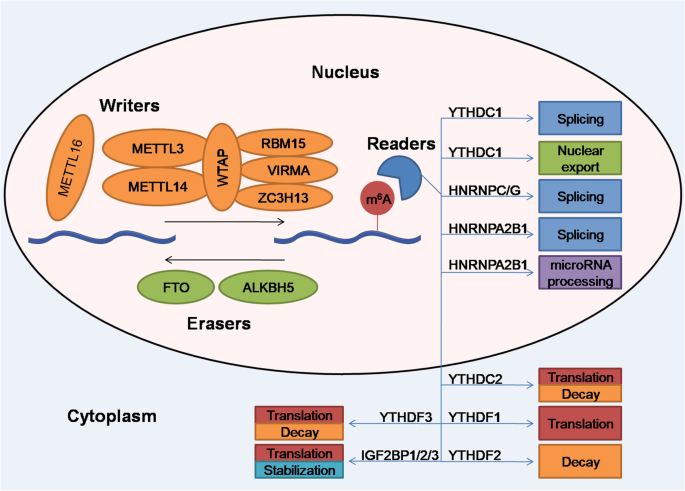
产品关联:文献未提及具体实验产品,领域常规使用m⁶A特异性抗体、高通量测序平台、重组蛋白表达系统等。
3.2 m⁶A在正常造血中的功能验证
实验目的:解析m⁶A修饰对造血干细胞(HSC)静息、增殖及分化的调控作用。
方法细节:整合细胞系实验(人造血干/祖细胞HSPCs的METTL3过表达/敲低)、小鼠模型(METTL3条件性敲除小鼠)及胚胎发育研究(METTL3缺陷胚胎的内皮-造血转化EHT过程分析)的结果。
结果解读:METTL3在HSPCs中高表达,过表达可显著促进HSPCs增殖、增加集落形成数并抑制髓系分化,通过m⁶A修饰MYC、BCL2、PTEN mRNA增强其翻译,维持细胞未分化状态;METTL3缺陷会阻断胚胎期EHT过程,导致HSPC生成障碍;YTHDF2通过降解Wnt靶基因mRNA维持HSC静息状态。
产品关联:文献未提及具体实验产品,领域常规使用造血干细胞分离试剂盒、集落形成实验体系、小鼠异种移植模型等。
3.3 m⁶A在AML发生发展中的机制研究
实验目的:阐明m⁶A调控因子在AML细胞增殖、凋亡、分化中的作用及分子机制。
方法细节:总结细胞系功能实验(METTL3、METTL14、WTAP等基因的敲低/过表达)、小鼠异种移植模型、转录组测序(MeRIP-seq、miCLIP)及核糖体图谱分析的研究数据。
结果解读:METTL3敲低可阻断AML细胞生长、诱导分化及凋亡,通过m⁶A修饰SP1 mRNA促进其翻译,维持白血病细胞未分化状态;METTL14通过增强MYB、MYC mRNA的m⁶A修饰及稳定性,促进AML进展;WTAP通过m⁶A依赖的方式抑制MYC mRNA降解,发挥癌基因作用;FTO过表达通过下调抑癌基因ASB2、RARA的表达,促进AML细胞增殖并抑制分化。
产品关联:文献未提及具体实验产品,领域常规使用AML细胞系、qRT-PCR检测系统、免疫印迹(WB)实验试剂等。
3.4 m⁶A与AML治疗耐药的关联分析
实验目的:明确m⁶A调控因子在AML化疗耐药及靶向药耐药中的作用机制。
方法细节:整合白血病细胞系药物处理实验(柔红霉素、依托泊苷、酪氨酸激酶抑制剂TKI)、基因敲低及下游信号通路分析的结果。
结果解读:WTAP敲低可增强AML细胞对柔红霉素的敏感性,其过表达则导致对依托泊苷耐药;FTO过表达通过m⁶A依赖的方式上调生存增殖基因表达,诱导TKI耐药;IGF2BP1通过增强ALDH1A1、HOXB4等基因的表达,增加AML细胞对化疗药物的耐药性。
产品关联:文献未提及具体实验产品,领域常规使用化疗药物试剂盒、细胞活力检测试剂等。
3.5 m⁶A在白血病干细胞自我更新中的作用研究
实验目的:解析m⁶A调控因子对LSC/LIC干性维持的调控作用。
方法细节:总结患者来源LSC实验、免疫缺陷小鼠模型及分子机制研究的结果。
结果解读:METTL14通过增强MYB、MYC的表达维持LSC自我更新;FTO敲低可降低LSC频率,通过下调MYC、CEBPA的表达抑制LSC干性;ALKBH5通过稳定AXL、TACC3 mRNA,促进LSC的增殖及干性维持;YTHDF2通过降解TNFR2 mRNA保护LSC免受凋亡。
产品关联:文献未提及具体实验产品,领域常规使用患者来源异种移植(PDX)模型、流式细胞术分选系统等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的Biomarker为m⁶A调控因子(METTL3、METTL14、WTAP、FTO、ALKBH5、YTHDF2、IGF2BP1),筛选与验证逻辑为:先通过细胞及动物实验明确其在AML发生发展中的功能,再结合临床样本分析其与AML患者临床特征的相关性,最终验证其作为诊断、预后及治疗反应评估Biomarker的潜力。
研究过程详述
Biomarker来源为AML患者的骨髓或外周血样本,验证方法包括qRT-PCR检测mRNA表达水平、免疫组化(IHC)检测蛋白表达水平。特异性与敏感性数据方面,METTL14在携带t(11q23)、t(15;17)、t(8;21)染色体易位的AML患者中显著高表达;WTAP高表达患者中FLT3-ITD突变比例更高,而t(15;17)亚型比例降低;ALKBH5高表达与AML患者复发率显著升高相关,ROC曲线AUC值等具体敏感性特异性数据文献未明确提供。
核心成果提炼
该类Biomarker的功能关联显示,WTAP、ALKBH5、IGF2BP1高表达提示AML患者不良预后,其中WTAP蛋白水平在完全缓解患者中显著降低,ALKBH5高表达患者的复发时间显著缩短(文献未明确具体HR值及P值);创新性在于首次系统提出m⁶A调控因子可作为AML的多维度Biomarker,覆盖诊断、预后及治疗反应评估。此外,FTO抑制剂如R-2HG、FB23-2在PDX AML小鼠模型中显示出显著的抗白血病效果,提示m⁶A调控因子同时具有作为治疗靶点的潜力。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。