Fatty acid metabolism shapes immune responses in chronic lymphocytic leukemia
脂肪酸代谢影响慢性淋巴细胞白血病的免疫反应
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2025 | 起止号: | 2025 Mar 12;13(1):42 |
| doi: | 10.1186/s40364-025-00753-7 | 研究方向: | 细胞生物学、代谢、免疫/内分泌 |
| 疾病类型: | 白血病 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Fatty acid metabolism shapes immune responses in chronic lymphocytic leukemia;发表期刊:Biomark Res;影响因子:未公开;研究领域:慢性淋巴细胞白血病代谢与免疫调控
领域共识:慢性淋巴细胞白血病(CLL)是一种起源于成熟CD19+CD5+B细胞的惰性血液系统恶性肿瘤,肿瘤代谢重编程是近年肿瘤学领域的研究热点,其中脂肪酸氧化(FAO)可为肿瘤细胞提供能量并参与耐药调控。当前领域发展关键节点包括:2018年研究发现伊布替尼耐药与FAO相关,2020年明确肿瘤代谢重编程可塑造免疫抑制微环境。当前研究热点方向聚焦于代谢通路作为治疗靶点的潜力,以及代谢与免疫微环境的相互作用机制。未解决的核心问题包括:CLL中脂肪酸代谢相关基因的表达模式尚未系统解析,脂肪酸代谢调控免疫微环境的具体机制不明确,缺乏基于脂肪酸代谢的预后标志物。
结合领域现状,当前研究空白在于缺乏整合代谢与免疫的CLL预后模型,以及代谢通路与靶向药物的协同作用研究。本研究针对这一核心问题,旨在构建脂肪酸代谢相关的预后风险评分,解析其调控CLL免疫应答的机制,为CLL的预后评估和治疗策略优化提供新的学术依据,具有填补代谢-免疫整合研究空白的学术价值。
2. 文献综述解析
作者对领域内现有研究的分类维度为:CLL脂肪酸代谢的能量供应功能、脂肪酸代谢与耐药的关联、肿瘤代谢重编程与免疫微环境的相互作用。
现有研究的关键结论包括:CLL细胞相较于正常B细胞更依赖FAO进行能量供应,伊布替尼耐药与FAO通路激活相关,化疗耐药与异常磷脂水平有关;技术方法优势在于已有研究采用转录组测序、细胞代谢实验等技术解析代谢通路的功能,但局限性在于未系统分析CLL中脂肪酸代谢基因的表达模式,缺乏对代谢通路与免疫微环境相互作用的整合研究,也未构建基于脂肪酸代谢的临床预后模型。
通过对比现有研究的未解决问题,本研究的创新价值凸显:首次整合bulk和单细胞转录组数据,构建了基于LPL、SOCS3、CNR1三个基因的FAM-score预后模型,系统解析了脂肪酸代谢调控CLL免疫细胞亚群的机制,发现FAO抑制可增强PI3K抑制剂的抗肿瘤效果,填补了CLL代谢-免疫整合研究的空白,为CLL的预后评估和联合治疗提供了新的思路。
3. 研究思路总结与详细解析
本研究的整体框架为:以CLL脂肪酸代谢重编程为切入点,通过数据挖掘筛选差异基因并构建预后模型,结合单细胞转录组解析免疫细胞表达特征,通过细胞实验验证代谢通路功能,最终探索FAO抑制与靶向药物的协同治疗潜力;核心科学问题是脂肪酸代谢如何塑造CLL免疫微环境并影响疾病进展;技术路线遵循“数据挖掘→模型构建→机制解析→功能验证”的闭环逻辑。
3.1 脂肪酸代谢差异基因筛选与预后模型构建
实验目的:筛选CLL与健康对照中差异表达的脂肪酸代谢基因,构建具有独立预后价值的风险评分模型,为CLL的预后评估提供新工具。
方法细节:整合Gene Expression Omnibus(GEO)、International Cancer Genome Consortium(ICGC)数据库中791例CLL患者的bulk转录组、单细胞转录组及临床预后数据,采用DESeq2分析CLL与健康对照的差异表达基因(DEGs),筛选|logFC|>1.2的脂肪酸代谢相关DEGs;在ICGC队列中采用Cox-LASSO回归分析,筛选具有独立预后意义的核心基因,构建FAM-score(计算公式为Risk Score=Σ(Coefi×ExpGenei),其中Coef为回归系数,ExpGene为基因表达量);通过Kaplan-Meier生存分析、时间依赖ROC曲线验证模型的预后性能,分析FAM-score与临床特征(年龄、性别、Binet分期、IGHV突变状态等)的相关性。
结果解读:共筛选出34个脂肪酸代谢相关DEGs,最终确定LPL、SOCS3、CNR1三个具有独立预后意义的基因构建FAM-score;该模型的预后性能优于传统Binet分期,与已建立的临床预后标志物相关;高FAM-score患者与年龄>60岁、男性、IGHV未突变、晚期Binet分期等不良临床特征显著相关(P<0.05)。
产品关联:文献未提及具体实验产品,领域常规使用生物信息学分析软件(R 4.2.3、DESeq2、glmnet包)、公共数据库(GEO、ICGC、MSigDB)。
3.2 单细胞转录组解析脂肪酸代谢基因的免疫细胞表达特征
实验目的:解析核心脂肪酸代谢基因在CLL免疫细胞亚群中的表达模式,探索脂肪酸代谢与免疫微环境的相互调控机制。
方法细节:采集5例初治CLL患者和2例健康对照的外周血单个核细胞,进行10x Genomics单细胞RNA测序;采用tSNE算法进行细胞分群,CellChat工具分析细胞间通讯网络,UCell计算单个细胞的脂肪酸代谢通路活性,knnDREMI分析核心基因与其他基因的功能关联;结合CIBERSORT算法分析不同FAM-score分组的免疫浸润模式。
结果解读:单细胞水平分析显示,LPL在CLL患者的B细胞中表达水平显著高于健康对照的CD4+T细胞,SOCS3在CLL患者的CD4+T细胞中表达量低于健康对照,CNR1在CLL患者的B细胞和CD8+T细胞中呈低表达;细胞通讯分析表明,耗竭B细胞、调节性T细胞(Tregs)、未转换记忆B细胞在CLL免疫微环境中发挥广泛调控作用,SOCS3高度富集于Treg群体;高FAM-score患者的免疫浸润模式呈现活化CD4+T细胞、CD8+T细胞、γδT细胞、树突状细胞减少,M2巨噬细胞、浆细胞、滤泡辅助T细胞、活化NK细胞增加的特征,提示脂肪酸代谢重编程塑造了免疫抑制微环境。
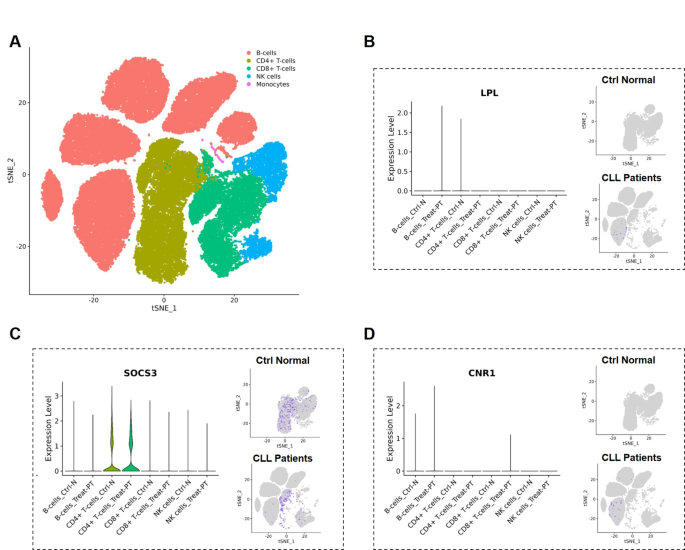
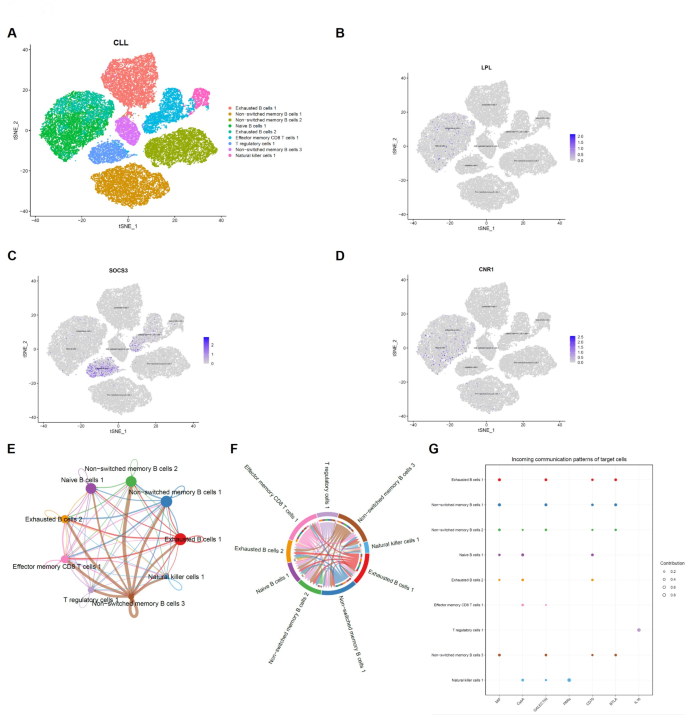
产品关联:实验所用关键产品:10x Genomics单细胞RNA测序平台,R软件(含Seurat、CellChat、UCell、knnDREMI工具包),CIBERSORT算法工具。
3.3 脂肪酸氧化通路的功能验证
实验目的:验证CLL细胞中脂肪酸氧化(FAO)通路的活性,探索FAO抑制对CLL细胞存活和基因表达的影响。
方法细节:采用scMetabolism算法量化单细胞转录组的脂肪酸代谢通路活性,ssGSEA分析ICGC队列中FAM相关通路的转录活性;使用Abcam细胞外氧消耗检测试剂盒、脂肪酸氧化检测试剂盒,检测CLL细胞系(MEC1、EHEB)、原代CLL细胞、健康对照外周血单个核细胞的氧消耗率和FAO活性;采用Perhexiline(FAO抑制剂)以0μM、2μM、4μM、8μM浓度处理CLL细胞,分别在24h、48h、72h采用CCK-8检测细胞活力,流式细胞术检测凋亡率,qRT-PCR检测核心基因(LPL、SOCS3、CNR1)的表达水平。
结果解读:单细胞代谢分析显示,CLL细胞中脂肪酸降解通路活性显著高于合成通路,FAO通路和细胞对脂肪酸的应答通路活性显著高于健康对照(P<0.05);ssGSEA分析表明,高FAM-score患者的FAO、脂肪酸合成、转运通路转录活性显著升高;细胞实验验证显示,CLL细胞的氧消耗率和FAO活性显著高于健康对照(P<0.01);Perhexiline处理后,CLL细胞活力呈浓度依赖性降低(n=3,P<0.01),凋亡率显著升高(n=3,P<0.01),LPL、CNR1基因表达下调,SOCS3基因表达上调。
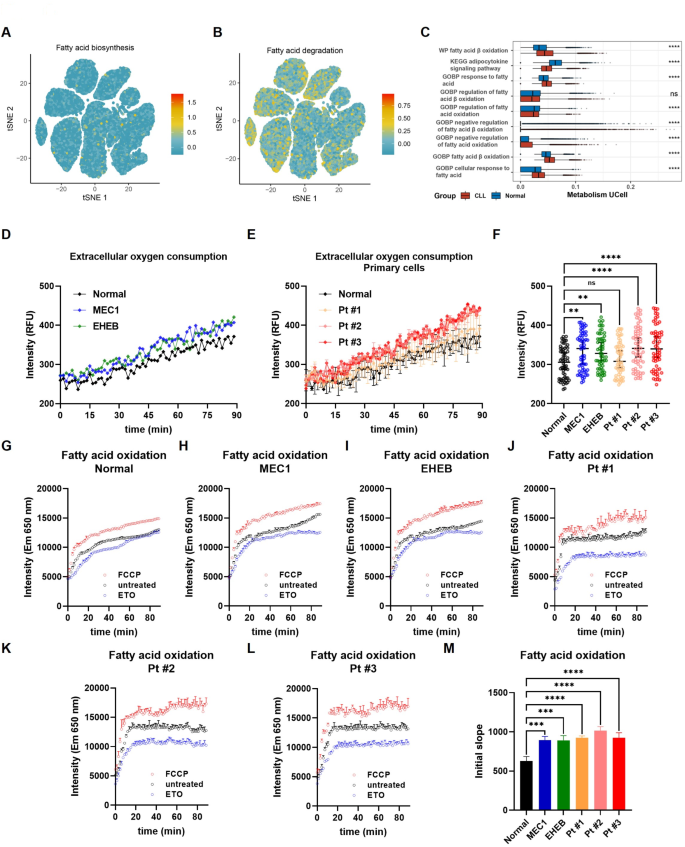
产品关联:实验所用关键产品:Abcam细胞外氧消耗检测试剂盒、脂肪酸氧化检测试剂盒,DOJINDO CCK-8试剂盒,Thermo Fisher ATTUNE NXT流式细胞仪,Roche Light Cycler 480 II实时荧光定量PCR系统,SparkJade SPARKeasy细胞RNA提取试剂盒,Agbio反转录试剂盒、SYBR Green荧光染料。
3.4 FAO抑制与PI3K抑制剂的协同作用验证
实验目的:探索FAO抑制与PI3K抑制剂idelalisib的协同抗肿瘤效果,为CLL的联合治疗提供实验依据。
方法细节:采用4μM Perhexiline与不同浓度的idelalisib联合处理CLL细胞系(MEC1、EHEB),在24h、48h、72h采用CCK-8检测细胞活力,分析联合用药的协同效应。
结果解读:FAO抑制显著增强CLL细胞对idelalisib的敏感性,联合用药组细胞活力显著低于单药处理组(n=3,P<0.001),提示FAO通路与PI3K通路存在协同调控作用,抑制FAO可逆转CLL细胞对PI3K抑制剂的耐药性。
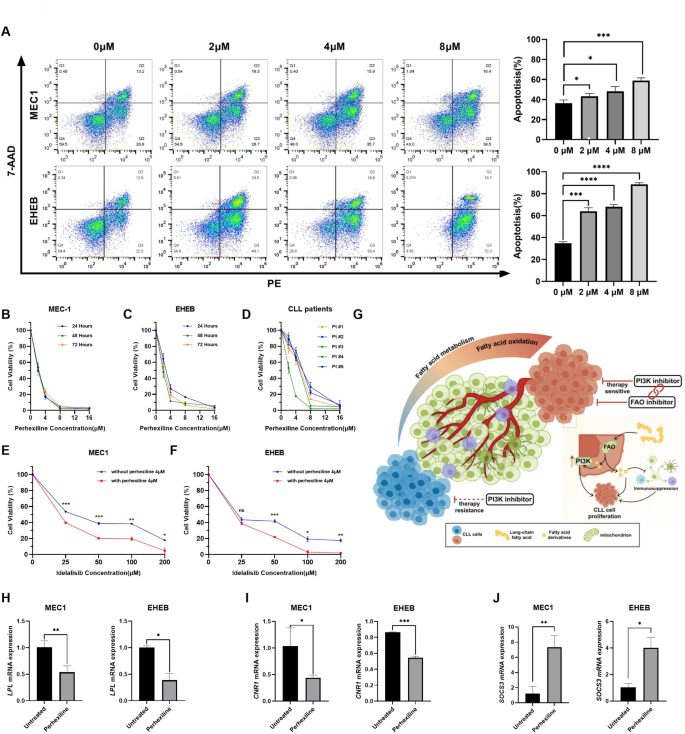
产品关联:文献未提及具体实验产品,领域常规使用PI3K抑制剂idelalisib,细胞活力检测试剂。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker为基于LPL、SOCS3、CNR1三个脂肪酸代谢基因构建的FAM-score预后风险评分,筛选与验证逻辑为:通过公共数据库挖掘差异表达的脂肪酸代谢基因→Cox-LASSO回归筛选独立预后基因→多队列验证模型的预后性能→分析模型与临床特征的相关性。
Biomarker的来源为CLL患者的外周血转录组数据,验证方法包括Kaplan-Meier生存分析、时间依赖ROC曲线、单因素与多因素Cox回归分析、临床特征相关性分析;特异性与敏感性方面,FAM-score在多队列中均能有效区分不同预后的CLL患者,其预后性能优于传统Binet分期,但文献未提供具体ROC曲线AUC值;核心成果提炼:FAM-score是CLL的独立预后标志物,高FAM-score与不良临床特征(年龄>60岁、男性、IGHV未突变、晚期Binet分期、疾病进展)显著相关(P<0.05);创新性在于首次整合代谢与免疫数据构建CLL预后模型,发现FAO调控免疫微环境的机制,以及FAO抑制与PI3K抑制剂的协同治疗潜力;统计学结果显示,FAM-score分组的生存差异具有统计学意义(log-rank检验P<0.05),但在TP53突变患者中预后预测能力不明确(因样本量仅16例,无法得出统计学结论)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。