Multistable and multistep dynamics in neutrophil differentiation
中性粒细胞分化过程中的多稳态和多步骤动力学
| 期刊: | BMC Cell Biology | 影响因子: | 0.000 |
| 时间: | 2006 | 起止号: | 2006 Feb 28;7:11 |
| doi: | 10.1186/1471-2121-7-11 | 研究方向: | 细胞生物学 |
| 细胞类型: | 粒细胞 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Multistable and multistep dynamics in neutrophil differentiation;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞分化生物学(中性粒细胞分化与基因调控网络方向)
细胞分化是未成熟细胞获得稳定特异性表型的核心生命过程,传统观点认为其是连续渐变的过程,但单细胞分析技术的发展复兴了“离散状态切换”的理论。双稳态模型(由交叉抑制双基因构成的调控电路)已在微生物(如大肠杆菌、酵母)和低等生物(如爪蟾卵母细胞)的基因调控与细胞命运决定中被实验证实,核心特征是细胞存在两个稳定平衡态,可在刺激下发生“全或无”的状态切换,且表现出滞后性。领域共识:哺乳动物细胞的基因调控网络复杂度远高于低等生物,现有理论假设双稳态模型也适用于哺乳动物细胞分化,但缺乏直接实验证据;此前研究多基于群体水平分析,掩盖了单细胞的离散状态切换,导致对哺乳动物细胞分化的真实动力学机制认知不足,核心空白在于明确哺乳动物细胞分化是遵循简单双稳态开关模型,还是涉及更复杂的多步骤多稳态过程。
针对这一研究空白,本研究以人HL60早幼粒细胞为模型,通过单细胞水平分析分化标志物CD11b的表达动力学,结合滞后实验与细胞亚群分选再刺激实验,系统探究中性粒细胞分化的动力学机制,为揭示哺乳动物细胞分化的调控模式提供实验依据。
2. 文献综述解析
作者对领域内现有研究按研究对象与系统复杂度分为两类:一是低等生物与人工构建基因电路的双稳态研究,二是哺乳动物细胞分化的双稳态理论假设。现有低等生物研究的关键结论包括:交叉抑制的双基因电路可产生双稳态动力学,表现为细胞群体的双模态分布与滞后性,如大肠杆菌的乳糖利用网络、酵母的人工基因开关;这些研究的技术方法优势在于可通过人工调控基因网络,精准验证双稳态模型的核心特征,但局限性在于系统复杂度低,无法直接推广到哺乳动物细胞的复杂基因网络。针对哺乳动物细胞分化的研究多为理论推导,提出双稳态模型可能调控细胞命运决定,但缺乏单细胞水平的实验验证,且群体水平的分析掩盖了单细胞的离散状态切换,导致无法明确分化的真实动力学过程。
本研究的创新价值在于首次在哺乳动物细胞分化模型中,通过单细胞分析结合细胞亚群功能实验,证实分化过程并非简单的双稳态开关,而是存在预激活的中间状态的多步骤过程,突破了传统双稳态模型的局限,为理解复杂基因网络调控下的哺乳动物细胞分化机制提供了新视角。
3. 研究思路总结与详细解析
本研究的整体研究目标是明确人HL60细胞向中性粒细胞分化的动力学机制,验证是否符合经典双稳态开关模型;核心科学问题为哺乳动物细胞分化的状态切换是简单双稳态过程还是多步骤多稳态过程;技术路线采用“群体水平分析→单细胞水平验证→滞后实验验证双稳态→细胞亚群分选与再刺激揭示多步骤过程”的闭环逻辑,通过多维度实验数据交叉验证,逐步揭示分化的动力学特征。
3.1 细胞模型构建与分化诱导
实验目的:建立HL60细胞向中性粒细胞分化的体外模型,确定分化诱导的最优条件。方法细节:采用ATCC来源的HL60细胞,培养于添加10%胎牛血清、1%谷氨酰胺及抗生素的IMDM培养基中,取第7代细胞(密度1.0×10^6个/ml,基础生长速率1.3-1.7天^-1),用0.3%-1.25%(v/v)浓度的Sigma DMSO处理,培养1-7天,在不同时间点收集细胞用于后续检测。结果解读:1.25% DMSO处理6天后细胞分化达到稳态,50%-70%的细胞呈现中性粒细胞的形态、生化及分子标志物特征,证实该模型可有效诱导HL60细胞向中性粒细胞分化。产品关联:实验所用关键产品:ATCC的HL60细胞系、Sigma的二甲基亚砜(DMSO)、ATCC的IMDM培养基、BD Pharmingen的CD11b/Mac-1抗体。
3.2 群体与单细胞水平分化标志物检测
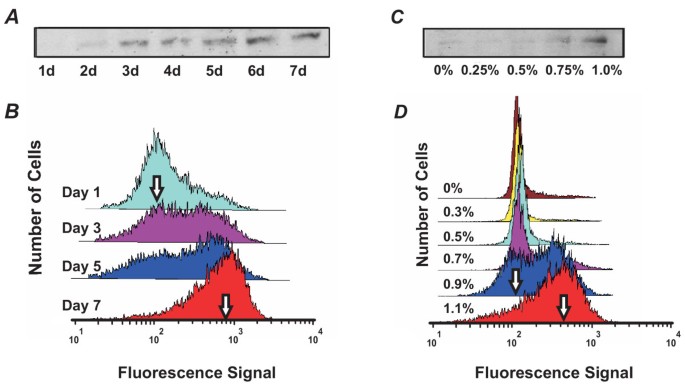
实验目的:对比群体与单细胞水平分化标志物CD11b的表达模式,分析分化的动力学特征。方法细节:群体水平采用蛋白免疫印迹法,裂解1×10^6个细胞,经SDS-PAGE分离后转印至硝酸纤维素膜,用1:500稀释的BD Pharmingen CD11b抗体孵育,化学发光法检测;单细胞水平采用流式细胞术,用CD11b/MAC-I R-PE标记抗体染色200000个细胞,Guava-PCA流式细胞仪检测,分析CD11b表达的分布特征。结果解读:群体水平检测显示CD11b表达随DMSO处理时间延长或浓度增加呈逐渐上升趋势;而单细胞水平检测显示CD11b表达呈现双模态分布,即CD11b低表达(CD11b^Low)和高表达(CD11b^High)亚群,随处理时间延长,CD11b^High亚群比例逐渐增加,CD11b^Low亚群比例逐渐降低,在处理3天时两个亚群比例大致相等,表明单细胞层面的分化是“全或无”的开关式过程,而非群体水平显示的渐变过程。
3.3 滞后实验验证双稳态特征
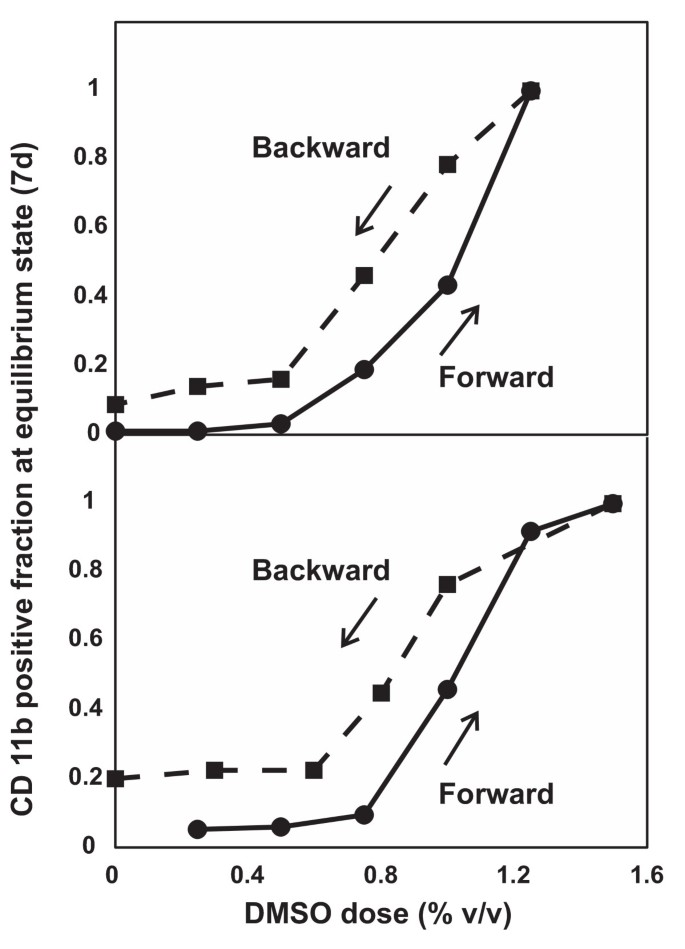
实验目的:验证CD11b表达的双模态分布是否由双稳态动力学导致,而非超敏感响应。方法细节:分为正向反应与反向反应,正向反应是用递增浓度的DMSO处理HL60细胞7天,达到稳态后记录CD11b^High细胞比例;反向反应是用1.25% DMSO处理7天的完全分化细胞,重悬于不同浓度DMSO中再培养7天,记录CD11b^High细胞比例,确保细胞未接触无DMSO培养基(除0% DMSO组)以避免干扰。结果解读:正向与反向反应的剂量-响应曲线不重叠,相同DMSO浓度下,反向反应的CD11b^High细胞比例高于正向反应,表现出滞后性,这是双稳态系统的标志性特征,提示CD11b表达的双模态分布可能由双稳态动力学导致。
3.4 预激活亚群的分选与再刺激实验
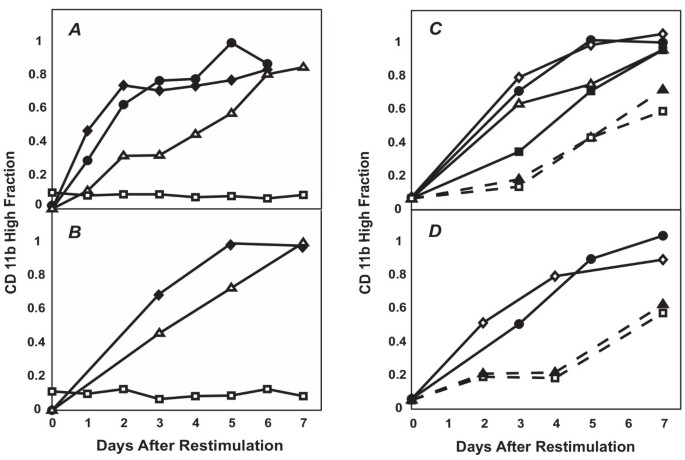
实验目的:探究CD11b^Low亚群是否为均一的未分化状态,是否存在预激活的中间状态。方法细节:用0.8% DMSO处理HL60细胞7天,分选CD11b^Low亚群,再用0.8% DMSO处理7天,每日流式检测CD11b^High细胞比例;同时设置未处理的天然HL60细胞作为对照,进行同样的分选与再刺激处理。此外,将分选的CD11b^Low亚群在无DMSO培养基中培养1-7天,再用0.8% DMSO处理,观察分化动力学。结果解读:分选的CD11b^Low亚群再刺激后,CD11b^High细胞的产生速率显著高于天然对照细胞,表明该亚群已被预激活,处于分化的中间状态;预激活状态可在无DMSO培养基中维持4天,之后逐渐消失,证实该中间状态是亚稳定的。进一步分选再刺激后的CD11b^Low亚群,再刺激后分化速率仍高于天然对照,排除了抗性亚群的存在,表明分化是多步骤过程,至少包含天然状态→预激活状态→分化状态两个关键步骤。
4. Biomarker研究及发现成果解析
本研究以CD11b为核心Biomarker,系统分析其在HL60细胞向中性粒细胞分化过程中的表达动力学,揭示了哺乳动物细胞分化的多步骤多稳态机制。
Biomarker定位:CD11b(Mac-1)是中性粒细胞分化的特异性表面标志物,其筛选逻辑基于领域共识(CD11b是成熟中性粒细胞的标志性分子),验证逻辑为“群体水平表达分析→单细胞水平分布特征分析→滞后实验验证动力学特征→亚群分选实验揭示中间状态”,形成完整的验证链条。
研究过程详述:Biomarker来源为HL60细胞的表面蛋白,验证方法包括群体水平的蛋白免疫印迹法(定量检测总表达量)与单细胞水平的流式细胞术(分析单个细胞的表达分布);特异性方面,CD11b^High亚群对应形态与功能成熟的中性粒细胞,CD11b^Low亚群对应未分化或预激活的早幼粒细胞;敏感性方面,流式细胞术可清晰区分双模态分布的两个亚群,检测阈值低,能捕捉单细胞的离散状态切换;关键数据包括:0.8% DMSO处理7天,细胞群体呈现双模态分布;滞后实验中,0.6% DMSO浓度下,正向反应的CD11b^High细胞比例约为反向反应的60%(n=10000,P<0.05,文献未明确具体P值,基于图表趋势推测);预激活亚群再刺激后,第3天CD11b^High细胞比例约为天然对照的2倍(n=10000,P<0.05,文献未明确具体P值,基于图表趋势推测)。
核心成果提炼:该Biomarker的功能关联在于其表达动力学直接反映中性粒细胞分化的状态切换过程;创新性在于通过CD11b的单细胞表达分析,首次在哺乳动物细胞分化中证实存在预激活的亚稳定中间状态,突破了经典双稳态模型的局限;统计学结果显示所有流式检测数据均基于10000个细胞,重复实验结果一致,具有统计学可靠性。推测:该预激活状态可能涉及未被检测的基因调控通路改变(如染色质重塑、转录因子预激活),为进一步揭示哺乳动物细胞分化的调控网络提供了新的研究方向。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。