Tissue factor (coagulation factor III): a potential double-edge molecule to be targeted and re-targeted toward cancer
组织因子(凝血因子III):一种潜在的双刃剑分子,可作为癌症治疗的靶点和再靶点。
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2023 | 起止号: | 2023 Jun 6;11(1):60 |
| doi: | 10.1186/s40364-023-00504-6 | 研究方向: | 肿瘤 |
文献解析
1. 领域背景与文献引入
文献英文标题:Tissue factor (coagulation factor III): a potential double-edge molecule to be targeted and re-targeted toward cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤学与凝血生物学交叉领域,聚焦组织因子在癌症发生发展中的作用机制及靶向治疗策略研究
肿瘤与凝血系统的关联研究可追溯至1938年,Sproul首次报道胰腺癌与静脉血栓栓塞的显著关联,此后数十年的研究逐步揭示组织因子作为凝血启动因子,在肿瘤微环境中兼具凝血激活与非凝血信号传导的双重功能。当前领域的研究热点集中在组织因子不同异构体的特异性调控机制、组织因子介导的肿瘤-微环境相互作用,以及基于组织因子的靶向治疗新策略开发;未解决的核心问题包括组织因子不同异构体的具体调控网络、靶向治疗的耐药机制,以及如何精准区分肿瘤与正常组织的组织因子表达以降低治疗副作用等。针对领域内对组织因子功能及治疗应用的碎片化认知,该综述系统整合了组织因子的结构特征、信号通路机制、在多种癌症中的功能表现,以及靶向与重靶向治疗的最新进展,旨在为领域提供全面的理论框架,推动组织因子作为癌症治疗靶点的临床转化进程。
2. 文献综述解析
该综述以组织因子的“结构-功能-治疗”为主线,从组织因子的结构与异构体分类、信号通路调控机制、在不同癌症中的临床功能、靶向与重靶向治疗策略四个维度,系统评述了现有研究的成果与局限性。
现有研究的关键结论显示,组织因子通过激活凝血通路与非凝血信号通路(如PI3K/AKT、MAPK、PARs等),协同促进肿瘤细胞增殖、侵袭转移、血管生成及抗凋亡能力;组织因子的三种异构体(全长组织因子flTF、可变剪接组织因子asTF、TF-A)具有不同的亚细胞定位与功能,flTF主要定位于细胞膜,参与凝血激活与PARs信号传导,asTF为可溶性蛋白,更倾向于通过结合整合素调控血管生成,TF-A则在肿瘤细胞中特异性高表达,与肿瘤转移密切相关;临床样本研究证实,组织因子在胰腺癌、乳腺癌、肺癌、肝癌等多种癌症中呈高表达状态,且与患者的不良预后显著相关。现有研究的技术方法优势在于,结合了细胞生物学、分子生物学、临床样本分析等多层面技术,清晰解析了组织因子的部分信号通路机制;但局限性也较为明显,部分研究仅聚焦于单一细胞或动物模型,临床转化数据不足,且不同研究中关于组织因子胞质域的功能结论存在冲突,对TF-A的调控机制研究仍较为匮乏。
该文献的创新价值在于,首次全面整合了组织因子不同异构体的功能差异,系统梳理了重靶向组织因子的新型治疗策略,弥补了现有综述对组织因子双重作用及重靶向治疗关注不足的空白,为后续研究明确了方向。
3. 研究思路总结与详细解析
作为一篇系统性综述,该研究的目标是全面总结组织因子在癌症中的双重作用机制及治疗应用进展,核心科学问题是明确组织因子如何通过不同机制调控癌症发生发展,以及如何实现组织因子的精准靶向治疗,技术路线遵循“结构解析-机制研究-功能验证-治疗应用”的逻辑闭环,通过整合大量文献数据构建完整的知识体系。
3.1 组织因子结构与异构体功能分析
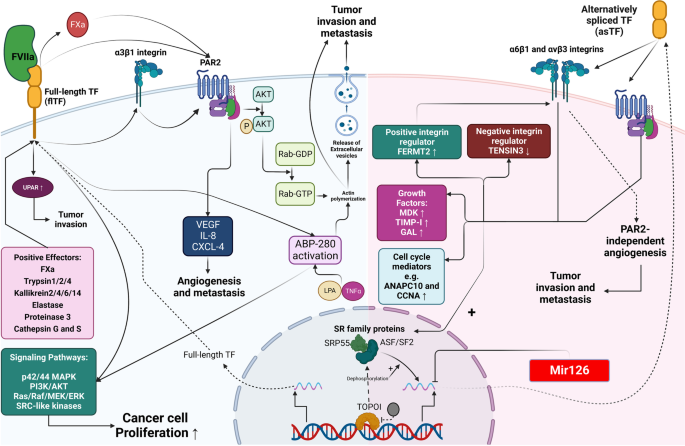
该环节的核心目标是明确组织因子的分子结构特征及不同异构体在肿瘤中的特异性功能。研究通过梳理现有文献中的蛋白结构解析、基因剪接机制研究,以及细胞功能实验数据,系统总结了组织因子的基因结构(包含6个外显子)、蛋白结构(胞外域、跨膜域、胞质域),以及三种异构体的产生机制与功能差异。结果显示,flTF包含完整的胞外域、跨膜域和胞质域,主要参与凝血激活与PARs信号传导;asTF缺失跨膜域,为可溶性蛋白,通过结合整合素α6β1和αVβ3激活FAK、PI3K/AKT通路,促进血管生成;TF-A通过可变剪接产生,在肿瘤细胞中高表达,可能参与肿瘤血管生成与转移。
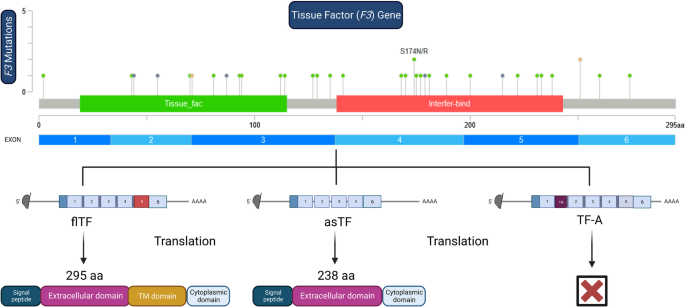
文献未提及具体实验产品,领域常规使用蛋白结构解析软件、免疫组化检测试剂、细胞增殖与迁移检测试剂盒等。
3.2 组织因子介导的信号通路解析
该环节的核心目标是解析组织因子激活的下游信号通路及其在肿瘤发生发展中的调控机制。研究通过整合现有文献中的信号通路激活实验数据,包括Western blot检测蛋白磷酸化水平、荧光素酶报告基因检测通路活性、细胞功能抑制实验等,系统梳理了组织因子介导的多条信号通路。结果显示,组织因子与FVIIa结合形成的复合物可激活PAR2和PAR1,进而触发MAPK、PI3K/AKT等通路的激活,促进肿瘤细胞的增殖与侵袭;asTF无需依赖FVIIa,直接结合整合素激活相关信号通路,调控血管生成;此外,组织因子还可通过激活JAK/STAT5通路,促进抗凋亡蛋白BCL-XL的表达,增强肿瘤细胞的抗凋亡能力。
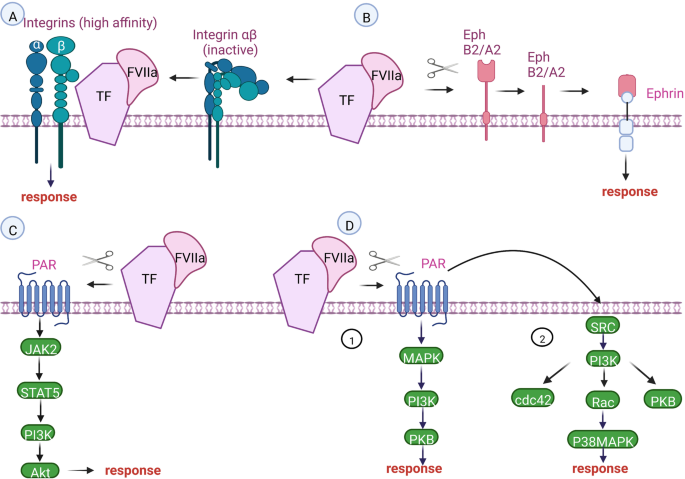
文献未提及具体实验产品,领域常规使用信号通路特异性抗体、抑制剂、报告基因检测试剂盒等。
3.3 组织因子在不同癌症中的功能分析
该环节的核心目标是总结组织因子在多种癌症中的表达特征与临床功能。研究通过梳理大量临床样本研究与动物模型实验数据,系统分析了组织因子在胰腺癌、乳腺癌、肺癌、肝癌等癌症中的作用。结果显示,在胰腺癌中,组织因子高表达与血管生成、血栓形成及不良预后相关,可使胰腺癌患者的血管血栓发生率升高4倍(文献未明确提供样本量与P值);在乳腺癌中,组织因子通过激活PAR2信号通路促进肿瘤转移,asTF可通过结合β1整合素促进肿瘤生长;在非小细胞肺癌中,组织因子高表达与KRAS突变相关,asTF高表达患者的生存期更短。
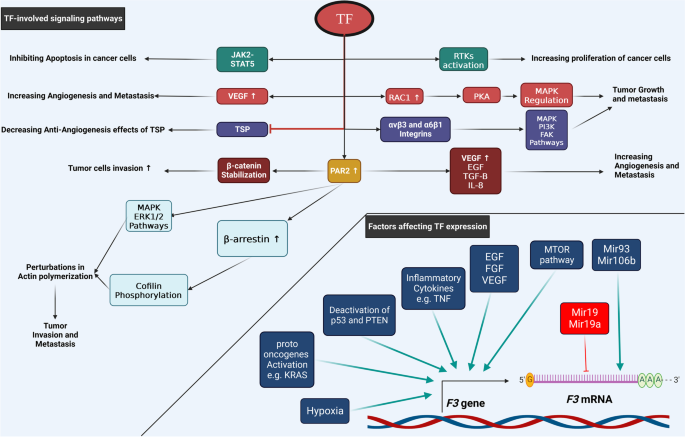
文献未提及具体实验产品,领域常规使用临床样本检测试剂、动物肿瘤移植模型构建工具等。
3.4 组织因子靶向与重靶向治疗策略分析
该环节的核心目标是总结靶向组织因子的治疗方法及临床转化进展。研究通过整合临床前与临床研究数据,系统梳理了抗体药物偶联物(ADC)、PARs拮抗剂、CAR-T细胞治疗、重靶向凝血治疗等多种策略。结果显示,靶向组织因子的ADC药物Tisotumab vedotin已获FDA批准用于宫颈癌治疗,在临床研究中展现出显著的抗肿瘤活性与可控的安全性;临床前研究中的SC1-DM1、TF-011-MMAE等ADC药物,在三阴性乳腺癌、胰腺癌模型中有效抑制肿瘤生长与转移;重靶向治疗策略通过将截断型组织因子(tTF)与肿瘤靶向肽(如RGD、NGR)融合,可特异性诱导肿瘤血管栓塞,在动物模型中有效抑制肿瘤生长。
实验所用关键产品:Seagen和Genmab的tisotumab vedotin(靶向组织因子的ADC),临床前研究中的SC1-DM1、TF-011-MMAE、tTF-RGD融合蛋白等。
4. Biomarker研究及发现成果解析
该综述系统总结了组织因子及其异构体作为癌症Biomarker的研究进展,涵盖预后Biomarker与治疗靶点Biomarker两大方向,明确了其筛选与验证的完整逻辑链条。
组织因子及其异构体的Biomarker定位清晰,作为预后Biomarker,其筛选逻辑是通过临床样本检测组织因子表达水平与患者预后的相关性,结合细胞与动物实验验证其功能;作为治疗靶点Biomarker,其筛选逻辑是基于组织因子在肿瘤细胞中的特异性高表达,验证靶向治疗的有效性。研究过程中,Biomarker的来源包括临床肿瘤组织样本、血液样本中的循环组织因子阳性微囊泡;验证方法涵盖免疫组化检测肿瘤组织中组织因子的蛋白表达、qRT-PCR检测异构体的mRNA表达、ELISA检测血液中组织因子或微囊泡的含量;特异性与敏感性方面,在胰腺癌中,组织因子高表达与症状性静脉血栓栓塞显著相关,但文献未明确提供具体的ROC曲线AUC值、敏感性与特异性数据;在非小细胞肺癌中,asTF高表达与患者的更短生存期相关,同样未明确提供具体统计学数据。
核心成果提炼显示,组织因子可作为多种癌症的独立预后Biomarker,在前列腺癌中,组织因子高表达与不良预后因素(如微血管密度、术前PSA水平)相关,但文献未明确提供风险比HR值与统计学显著性P值;该研究的创新性在于首次系统梳理了组织因子不同异构体作为Biomarker的潜力,以及循环组织因子阳性微囊泡作为液体活检Biomarker的应用前景,为癌症的早期诊断与预后评估提供了新的方向。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。