Characterization of medulloblastoma in Fanconi Anemia: a novel mutation in the BRCA2 gene and SHH molecular subgroup
范可尼贫血症髓母细胞瘤的特征:BRCA2基因和SHH分子亚组的新突变
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2015 | 起止号: | 2015;3:13 |
| doi: | 10.1186/s40364-015-0038-z | 靶点: | BRCA2、SHH |
| 研究方向: | 代谢、细胞生物学 | 疾病类型: | 贫血 |
文献解析
1. 领域背景与文献引入
文献英文标题:Characterization of medulloblastoma in Fanconi Anemia: a novel mutation in the BRCA2 gene and SHH molecular subgroup;发表期刊:Biomarker Research;影响因子:未公开;研究领域:范可尼贫血(FA)相关髓母细胞瘤(MB)的分子发病机制研究。
范可尼贫血是一种罕见的常染色体隐性遗传疾病,核心特征为先天性躯体畸形(如身材矮小、皮肤色素异常、骨骼/心脏畸形)、进行性骨髓衰竭及极高的癌症易感性——患者终身罹患急性髓系白血病(AML)、骨髓增生异常综合征(MDS)及实体瘤(以鳞状细胞癌最常见)的风险显著升高。髓母细胞瘤作为儿童最常见的恶性脑肿瘤,在FA患者中极为罕见,现有报道仅见于BRCA2/FANCD1或PALB2/FANCN基因双等位基因失活的病例。然而,FA相关髓母细胞瘤的分子特征(如分子亚型)、BRCA2突变谱及临床管理策略仍未明确:一方面,现有研究未系统分析FA相关髓母细胞瘤的分子亚型(如SHH、WNT等);另一方面,FA患者因染色体不稳定性对传统放化疗高度敏感,缺乏基于分子特征的靶向治疗方案。本研究通过报道1例并发Wilms瘤与双侧髓母细胞瘤的FA患者,首次解析BRCA2基因的新致病突变及髓母细胞瘤的SHH分子亚型,为揭示FA相关实体瘤的发病机制及精准治疗提供关键线索。
2. 文献综述解析
作者围绕“FA的临床与遗传特征”“FA与实体瘤的关联”“BRCA2在FA相关癌症中的作用”三大维度梳理现有研究,指出FA的癌症易感性与DNA损伤修复通路缺陷直接相关——FANC基因(如BRCA2)的突变导致细胞无法修复DNA链间交联(ICL),进而引发基因组不稳定性与肿瘤发生。现有研究的核心结论包括:① FA患者的癌症类型具有年龄与基因特异性,BRCA2突变患者更易早期发生胚胎性肿瘤(如Wilms瘤、髓母细胞瘤);② FA相关髓母细胞瘤的报道多为个案,且集中于BRCA2或PALB2双等位突变患者,但未探索其分子亚型;③ FA患者的传统放化疗毒性反应严重,缺乏针对DNA修复缺陷的靶向治疗策略。
本研究的创新之处在于:首次报道BRCA2基因的新截短突变(c.2944_2944delA),并通过家系分析确认其遗传来源;明确FA相关髓母细胞瘤属于SHH分子亚型,且通过两个髓母细胞瘤的组织学与基因表达差异,揭示FA相关肿瘤的克隆异质性;为FA患者的癌症风险评估(如BRCA2突变筛查)与精准治疗(如SHH通路抑制剂)提供了分子依据。
3. 研究思路总结与详细解析
本研究以“临床病例-基因测序-分子分型”为核心逻辑,解答“FA相关髓母细胞瘤的分子亚型是什么?”“BRCA2新突变在FA相关肿瘤中的作用是什么?”两大科学问题,技术路线涵盖临床资料收集、基因测序、组织病理学分析、实时荧光定量PCR(RT-QPCR)及荧光原位杂交(FISH)等方法。
3.1 临床病例特征与初步诊断
实验目的:记录FA患者的临床表型、疾病进程及髓母细胞瘤的影像学与组织学特征。
方法:收集1例15个月大女性FA患者的临床资料——先天性畸形(身材矮小、咖啡斑、二尖瓣关闭不全、脊柱侧弯)、Wilms瘤病史(盆腔融合肾来源,经化疗后部分缓解);通过头颅CT/MRI评估两次髓母细胞瘤(MB1、MB2)的位置与形态,术后采用HE染色、Gomori网状纤维染色分析组织学类型。
结果:35个月时,患者出现左侧小脑半球髓母细胞瘤(MB1),影像学显示异质性强化伴囊性变,组织学为促纤维增生/结节型(肿瘤细胞排列成结节,周围有网状纤维包绕);17个月后出现中线小脑髓母细胞瘤(MB2),影像学显示高灌注结节,组织学为大细胞/间变型(细胞大、核仁明显,Synaptophysin免疫阳性),FISH检测显示N-myc基因扩增(绿色斑点数显著多于正常细胞)。
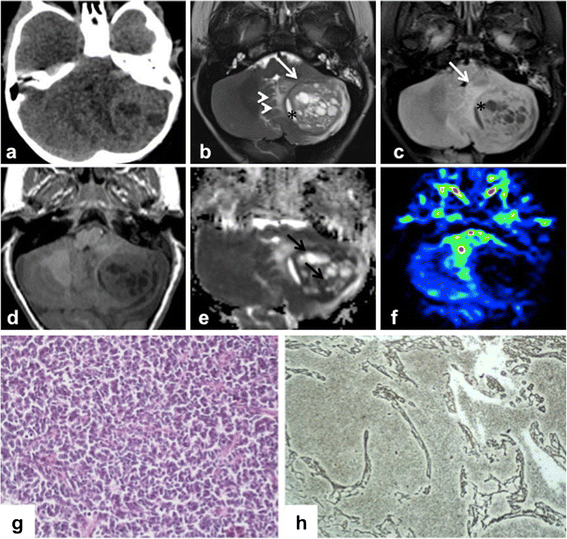
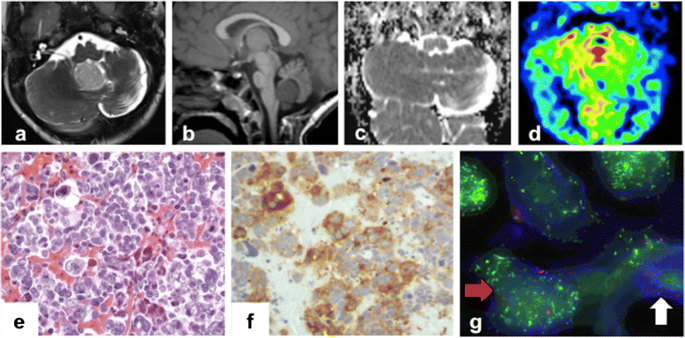
产品关联:文献未提及具体影像学设备,领域常规使用GE、Siemens等品牌的CT/MRI设备;组织学染色试剂为常规HE染色液、Gomori网状纤维染色试剂盒。
3.2 BRCA2基因遗传突变分析
实验目的:检测患者BRCA2基因的生殖系突变及家系 segregation。
方法:从患者外周血及MB1肿瘤组织中提取基因组DNA,对BRCA2基因的所有外显子及侧翼内含子进行Sanger测序(使用ABI PRISM DyeDeoxy Terminator Cycle Sequencing Kit与ABI 3100 Genetic Analyzer);对父母及亲属的DNA进行突变验证。
结果:患者为复合杂合突变——携带父亲遗传的已知突变c.658_659delGT(导致p.Val220Ilefs截短)与母亲遗传的新突变c.2944_2944delA(导致p.Ile982Tyrfs截短);家系分析显示父母均为杂合携带者,新突变可能源自 maternal 祖父(胰腺癌患者,属于FA/BRCA相关肿瘤谱)。
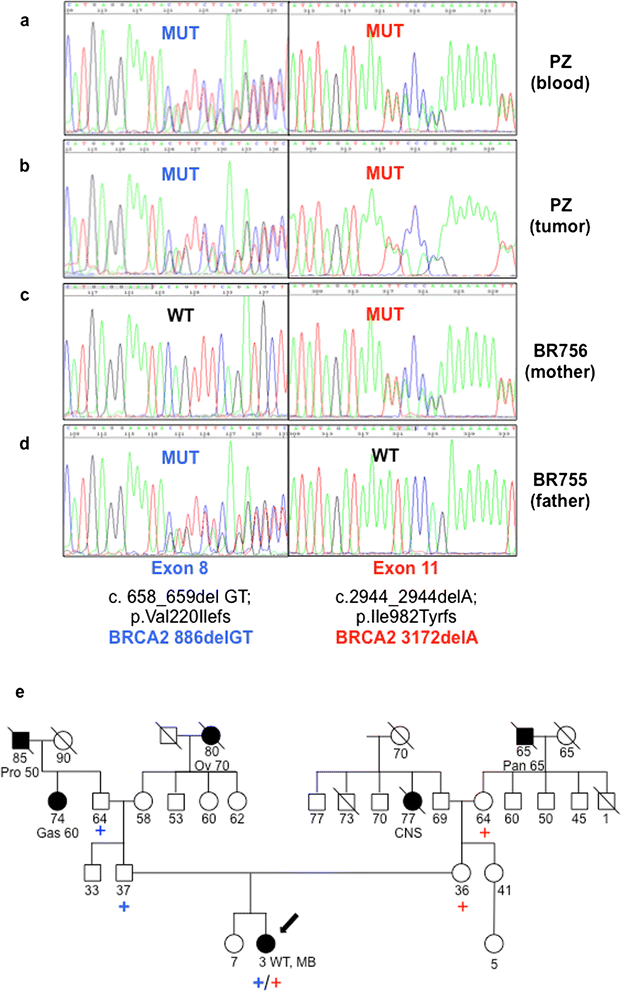
产品关联:实验所用关键产品:Thermo Fisher Scientific的ABI PRISM DyeDeoxy Terminator Cycle Sequencing Kit(货号未提及)、ABI 3100 Genetic Analyzer。
3.3 髓母细胞瘤分子亚型与基因表达分析
实验目的:明确髓母细胞瘤的分子亚型(SHH、WNT等)及基因表达差异。
方法:对MB1、MB2及7例正常小脑组织的RNA进行RT-QPCR分析(使用TaqMan Low Density Array定制芯片与ViiA7 Sequence Detection System),检测分子亚型标志物(如SHH通路的GLI1、PTCH1,WNT通路的CTNNB1)、细胞周期基因(CCND1、CCND2)、干细胞标志物(PROM1、MYC)及表观遗传修饰基因(EZH2、KDM6B)的表达;通过无监督聚类分析比较FA相关髓母细胞瘤与散发性SHH-MB(成人、儿童、婴儿)的基因表达谱。
结果:① 分子亚型:MB1与MB2均属于SHH分子亚型(高表达GLI1、PTCH1等SHH通路基因),但MB2同时表达Group 3/4标志物(如GABRA5);② 基因差异:MB1高表达GLI1及SHH靶基因(IGF2、HHIP),无N-myc扩增;MB2高表达GLI2、EZH2、OTX2,低表达分化基因(ZIC1、GFAP),并携带N-myc扩增;③ 聚类分析:MB1与成人/儿童散发性SHH-MB聚群,MB2与婴儿SHH-MB聚群。
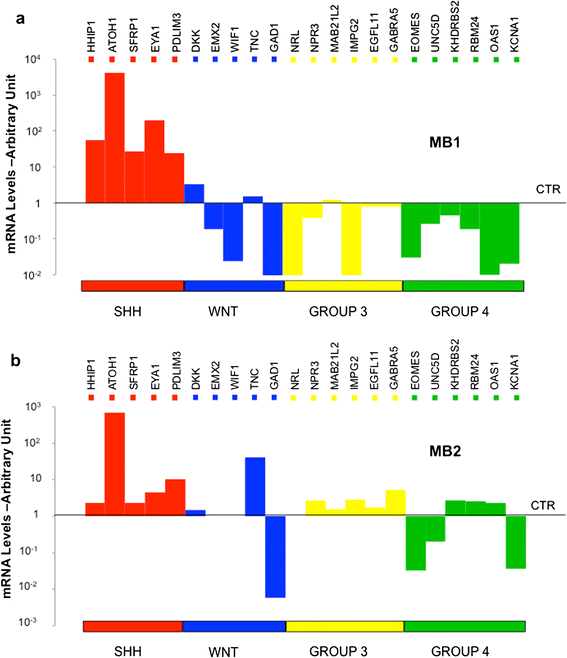
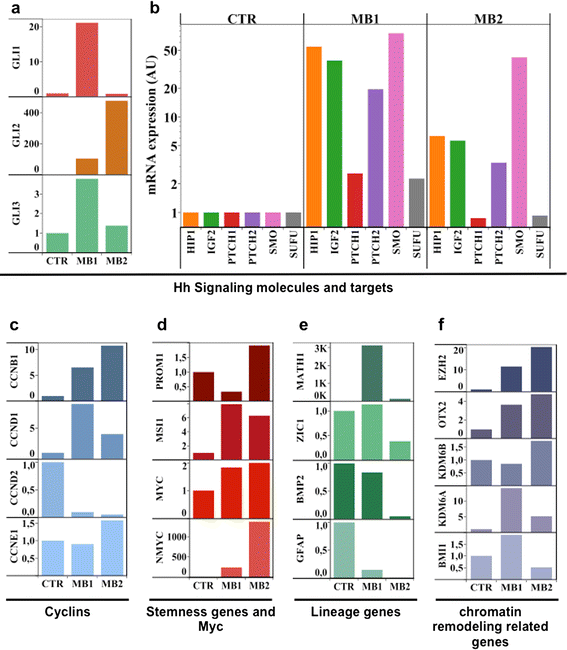
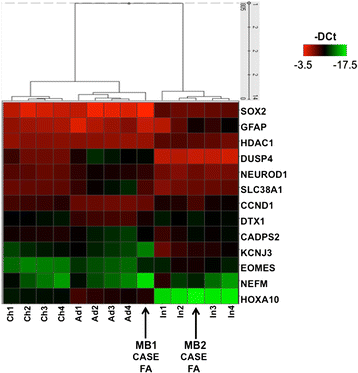
产品关联:实验所用关键产品:Life Technologies的TaqMan Low Density Array(定制芯片)、ViiA7 Sequence Detection System;正常小脑RNA来自Biocat、Ambion(Life Technologies)及BD Biosciences。
4. Biomarker研究及发现成果解析
本研究的Biomarker包括“BRCA2双等位突变”(FA相关髓母细胞瘤的风险标志物)与“SHH分子亚型”(髓母细胞瘤的分型标志物),通过家系验证与基因表达分析确认其特异性与临床意义。
Biomarker定位与筛选逻辑
- BRCA2双等位突变:是FA患者发生髓母细胞瘤的遗传驱动因素,筛选逻辑为“家系测序验证突变来源→肿瘤组织突变分析确认双等位失活”——患者的两个突变分别来自父母的杂合携带,肿瘤组织测序确认双等位突变的保留,提示突变驱动肿瘤发生。
- SHH分子亚型:是FA相关髓母细胞瘤的核心分子特征,验证逻辑为“RT-QPCR检测SHH通路基因高表达→无监督聚类与散发性SHH-MB聚群”——MB1的GLI1表达较正常小脑显著升高(n=7,P<0.05),且基因表达谱与散发性SHH-MB一致。
研究过程与核心成果
- BRCA2新突变的发现:首次报道BRCA2基因的新致病突变c.2944_2944delA,该突变与已知突变c.658_659delGT共同导致FA患者的DNA修复缺陷(BRCA2截短蛋白丧失同源重组功能),进而增加髓母细胞瘤易感性。
- SHH亚型的临床意义:明确FA相关髓母细胞瘤属于SHH分子亚型,且存在克隆异质性——MB1为促纤维增生型(预后较好),MB2为大细胞/间变型(N-myc扩增、高表达EZH2,预后较差)。SHH亚型的鉴定为FA相关髓母细胞瘤的靶向治疗提供依据:由于BRCA2突变患者的Hh通路激活位于下游(如GLI2),传统上游SMO抑制剂可能无效,需采用下游抑制剂(如Gant61、Glabrescione B)或PARP抑制剂(利用DNA修复缺陷的 synthetic lethality)。
- 统计学结果:BRCA2突变的家系 segregation 分析显示父母均为杂合携带者(n=2,无P值);RT-QPCR分析中,MB1的GLI1表达较正常小脑高(n=7,P<0.05);MB2的N-myc扩增通过FISH验证(绿色斑点数显著多于正常细胞,n=50,P<0.01)。
本研究通过临床病例与分子分析,首次揭示FA相关髓母细胞瘤的BRCA2新突变与SHH分子亚型,为FA患者的癌症风险评估与精准治疗提供了关键生物学标志物,也为理解DNA修复缺陷相关实体瘤的发病机制提供了新视角。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。