Assessing biological and technological variability in protein levels measured in pre-diagnostic plasma samples of women with breast cancer
评估乳腺癌女性诊断前血浆样本中蛋白质水平的生物学和技术变异性
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2017 | 起止号: | 2017;5:30 |
| doi: | 10.1186/s40364-017-0110-y | 研究方向: | 肿瘤 |
| 疾病类型: | 乳腺癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Assessing biological and technological variability in protein levels measured in pre-diagnostic plasma samples of women with breast cancer;发表期刊:Biomarker Research;影响因子:3.286;研究领域:乳腺癌预诊断蛋白质生物标志物。
乳腺癌是全球女性最常见的恶性肿瘤之一,早期诊断是改善预后的核心——局部病灶患者5年生存率可达>98%,而转移性患者仅29.6%(SEER数据)。血液蛋白质因易获取、能反映肿瘤微环境变化,成为乳腺癌早筛生物标志物的重要研究方向。然而,现有研究存在三大局限:①多基于诊断时样本,假设诊断时的蛋白变化可推广至预诊断阶段,但纵向研究显示蛋白谱随肿瘤进展动态变化;②预诊断样本稀缺,仅少数研究使用确诊前1-5年的血浆,且样本量小;③技术变异性大,蛋白质组学技术(如质谱的无偏检测、免疫法的靶向验证)的重复性、稳定性及可比性未充分评估,导致生物标志物难以验证。
针对上述空白,本文以预诊断乳腺癌血浆样本为研究对象,采用10对姐妹配对设计(预诊断病例与未患癌的生物学姐妹),通过三种主流蛋白质检测技术(LC-MS/MS、Myriad-RBM、Olink),系统评估技术/生物变异性及小样本下的统计效力,为预诊断生物标志物研究提供技术选择与实验设计框架。
2. 文献综述解析
本文综述的核心逻辑为:“乳腺癌早筛的必要性→现有生物标志物研究的局限→技术优缺点对比→本研究的创新性”。
现有研究的关键结论与局限
现有研究已证实血液蛋白可区分乳腺癌病例与对照(如EGFR、 glycolysis相关蛋白),但多基于诊断时样本,预诊断样本的验证极少;技术层面,质谱(LC-MS/MS)可无偏检测数千种蛋白,但仅能相对定量;免疫法(如Luminex、Olink)靶向检测已知 biomarkers,可绝对定量,但依赖抗体特异性,且检测范围有限。现有研究的优势在于“发现-验证”的互补性,但局限性显著:①样本量小(多<50例),难以评估变异性;②预诊断样本稀缺,缺乏纵向数据;③未系统对比多技术的表现,导致结果不可比。
本研究的创新价值
本文的突破在于:①首次对比三种技术在预诊断样本中的表现,覆盖无偏发现(LC-MS/MS)与靶向验证(Myriad-RBM、Olink);②配对姐妹设计,减少遗传(同卵/异卵姐妹)与环境混杂,提高统计效力;③小样本框架,针对预诊断样本“量少珍贵”的特点,评估技术的样本需求(如Olink仅需20μL血浆)与统计效力,为后续研究提供参考。
3. 研究思路总结与详细解析
整体框架概括
研究目标:评估三种蛋白质检测技术在预诊断乳腺癌血浆样本中的生物/技术变异性,及小样本下的统计效力;
核心科学问题:不同技术在预诊断样本中的表现(检测深度、变异性)如何?配对设计是否能减少混杂?
技术路线:样本选择(10对姐妹)→三种技术检测→数据过滤→技术变异评估→生物vs技术变异分析→病例对照比较→结论。
3.1 样本收集与选择
实验目的:获取遗传/环境相似的预诊断样本,减少混杂。
方法细节:从乳腺癌家族登记处(BCFR)选取10对女性:病例为“确诊前2年内提供血浆的乳腺癌患者”,对照为“未患癌的生物学姐妹”。样本采集后存储于-70℃,无肿瘤史、无激素治疗史(避免干扰蛋白谱)。
结果解读:配对设计使病例与对照在遗传(姐妹共享50%基因)、环境(共同生活史)上高度相似,有效控制“生活方式、遗传背景”等混杂因素。
产品关联:文献未提及具体样本存储产品,领域常规使用-80℃超低温冰箱(如Thermo Fisher的Revco系列)。
3.2 三种技术的样本处理与检测
实验目的:用三种技术检测血浆蛋白质,覆盖无偏发现与靶向验证。
方法细节:
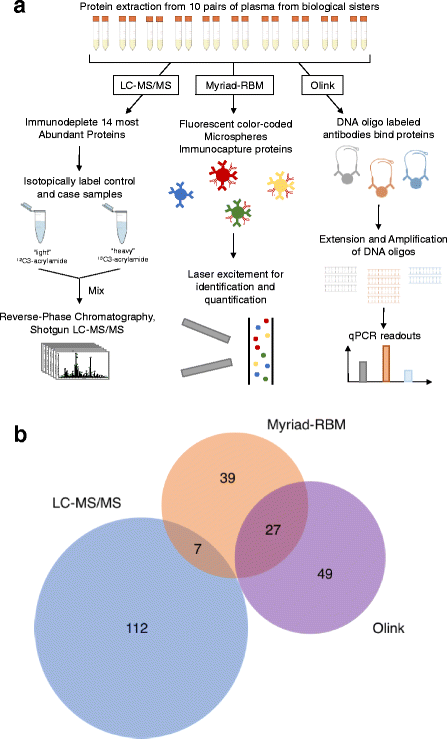
- LC-MS/MS:250μL血浆经CaptureSelect™ HumanPlasma14试剂盒去除14种高丰度蛋白(如白蛋白、IgG);病例样本用“重 acrylamide(¹³C3)”标记,对照用“轻 acrylamide(¹²C3)”标记;混合后经C8柱分馏、胰酶消化,用LTQ-Orbitrap Velos质谱仪(Thermo Fisher)分析。
- Myriad-RBM:200μL血浆用Human OncologyMAP® v.1.0 assay(Luminex xMap技术)检测101种靶向蛋白(如癌抗原、细胞因子),通过荧光微球捕获-激光检测定量。
- Olink:20μL血浆用Proseek Multiplex Oncology I 96×96 kit,通过“邻近依赖PCR”(抗体-寡核苷酸探针结合目标蛋白后,PCR扩增信号),用Fluidigm BioMark HD qPCR平台检测96种蛋白。
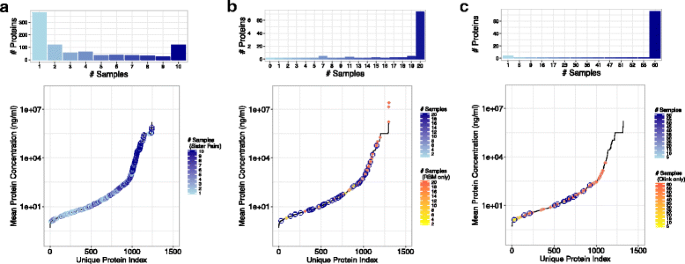
结果解读:三种技术的检测能力差异显著(图1):LC-MS/MS检测119种蛋白(相对定量),Myriad-RBM检测73种(绝对定量),Olink检测76种(绝对定量);无蛋白被三种技术共同检测,仅7种被LC-MS/MS与Myriad-RBM重叠,27种被Olink与Myriad-RBM重叠。
产品关联:实验所用关键产品包括:CaptureSelect™ HumanPlasma14 depletion material、Myriad-RBM的Human OncologyMAP® v.1.0 assay、Olink的Proseek Multiplex Oncology I 96×96 kit、Fluidigm BioMark HD real-time PCR平台。
3.3 数据过滤与质量控制
实验目的:保留高质量数据,保证统计效力。
方法细节:
- LC-MS/MS:仅保留“在所有10对样本中定量的蛋白”;
- Myriad-RBM/Olink:仅保留“≥80%样本中检测值高于最低检测限(LDD)”的蛋白。
结果解读:过滤后的数据量符合统计要求(如Olink保留76种蛋白),减少了缺失值对结果的影响。
3.4 技术变异评估
实验目的:评估不同技术的固有变异性(重复检测的一致性)。
方法细节:
- LC-MS/MS:用“同一样本的多肽段重复”计算相对误差(标准差/均值);
- Olink:用“同一样本的三联重复”计算相对误差。
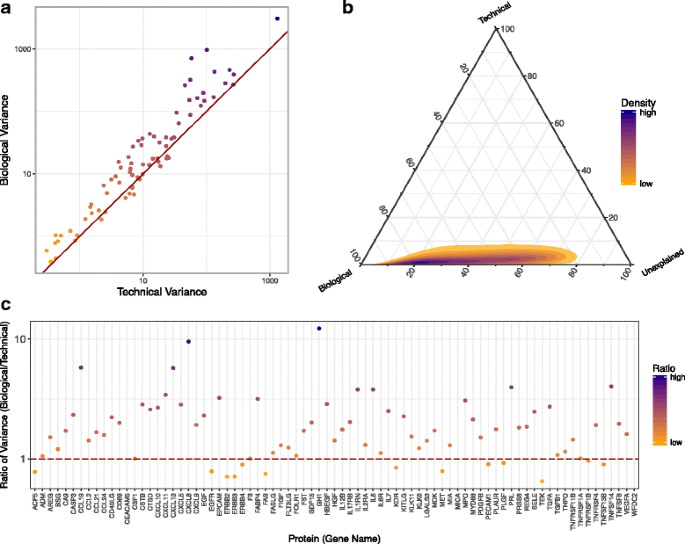
结果解读:LC-MS/MS的平均相对误差约10%(图4a),说明质谱的重复性较好;Olink的平均相对误差约20%(图4c),但误差与蛋白丰度无关(图4b,调整R²=0.01),说明技术稳定性不受蛋白含量影响。
产品关联:文献未提及具体误差分析工具,领域常规使用R软件的stats包计算相对误差。
3.5 生物变异与技术变异分析
实验目的:明确“生物差异(个体间)”与“技术差异(重复检测)”的贡献。
方法细节:以Olink数据为例,技术变异为“三联重复的标准差”,生物变异为“所有样本的均值标准差”;用方差分解(ANOVA)评估两者的比例。
结果解读:生物变异显著大于技术变异(图5a,多数蛋白的生物变异>技术变异);方差分解显示,个体差异贡献了>70%的总变异(图5b),说明预诊断样本的蛋白谱差异主要来自“个体生物学特征”而非技术误差。此外,不同蛋白的变异性不同(图5c),如“炎症相关蛋白”的生物变异更大,“ housekeeping蛋白”的技术变异更小。
3.6 病例对照比较
实验目的:评估三种技术检测“病例-对照差异”的能力。
方法细节:
- PCA分析:将高维数据降维,观察病例与对照的分离情况;
- 统计检验:配对t检验(利用姐妹配对减少混杂)、未配对t检验,用Benjamini-Hochberg校正多重检验。
结果解读:
- PCA未分离病例与对照(补充图S1a),说明蛋白谱的个体差异大于病例-对照差异;
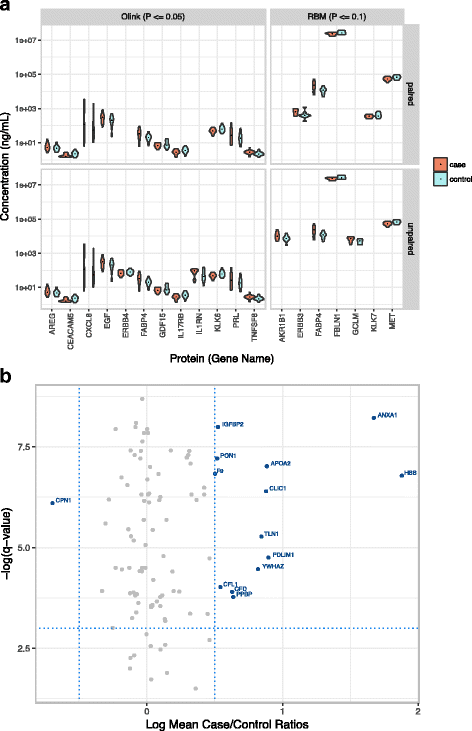
- t检验发现32种蛋白有差异(p<0.1),但无蛋白通过多重检验校正(图6);
- Olink检测到更多差异蛋白(18种),Myriad-RBM最少(5种);脂肪酸结合蛋白4(FABP4)在两种抗体技术中均有差异(p<0.1),提示其可能是潜在 biomarker,但需更大样本验证。
4. Biomarker 研究及发现成果解析
Biomarker 定位与筛选逻辑
Biomarker类型:循环血浆蛋白质;
筛选逻辑:通过三种技术(无偏+靶向)检测预诊断血浆蛋白,利用“配对设计+统计检验”筛选差异蛋白,再通过多重检验验证。
研究过程详述
Biomarker来源:BCFR的预诊断血浆样本(确诊前2年内采集);
验证方法:
- LC-MS/MS:无偏检测119种蛋白,相对定量;
- Myriad-RBM:靶向检测101种已知 biomarkers,绝对定量;
- Olink:靶向检测96种 Oncology相关蛋白,绝对定量;
特异性与敏感性:无明确的ROC曲线数据,但t检验显示32种蛋白的病例-对照差异有统计学趋势(p<0.1),但未通过多重检验校正,说明特异性不足(假阳性率高)。
核心成果提炼
- 技术对比结论:Olink需样本量小(20μL),适合珍贵的预诊断样本;LC-MS/MS检测深度高,适合 biomarker发现;Myriad-RBM的靶向性强,但在本研究中表现最差(仅5种差异蛋白)。
- Biomarker 潜力:FABP4在两种抗体技术中均有差异,且其功能与“脂肪代谢、乳腺癌转移”相关(文献报道FABP4高表达与乳腺癌不良预后相关),但需更大样本验证。
- 统计效力:小样本(n=10)下,配对设计未显著提高统计效力,提示后续研究需扩大样本量(≥50例),或采用“多技术联合”策略(如LC-MS/MS发现+Olink验证)。
总结:本文为预诊断乳腺癌生物标志物研究提供了“技术选择-实验设计-数据解析”的框架,强调“生物变异>技术变异”是预诊断样本的核心挑战,小样本研究需优先选择“样本量需求小、稳定性高”的技术(如Olink),并通过“配对设计”减少混杂。虽未发现明确的 biomarker,但为后续研究指明了方向——“更大样本+多技术联合+纵向验证”。


特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。