Decoding the mechanisms underlying breast cancer brain metastasis: paving the way for precision therapeutics
揭示乳腺癌脑转移的潜在机制:为精准治疗铺平道路
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2025 | 起止号: | 2025 Nov 11;13(1):144 |
| doi: | 10.1186/s40364-025-00854-3 | 研究方向: | 神经科学、肿瘤 |
| 疾病类型: | 乳腺癌 | ||
文献解析
1. 领域背景与文献引入
文献英文标题:Decoding the mechanisms underlying breast cancer brain metastasis: paving the way for precision therapeutics;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌脑转移机制与精准治疗
乳腺癌是全球最常见的恶性肿瘤,近年来随着早期诊断和系统治疗的进步,患者生存率显著提升,但远处转移的发生率也随之增加。乳腺癌细胞具有器官特异性转移倾向,脑是常见的转移部位之一,不同分子亚型的脑转移发生率存在差异:人表皮生长因子受体2(HER2)阳性乳腺癌患者中约30%会发生脑转移,三阴性乳腺癌患者为30%-50%,激素受体(HR)阳性患者为15%。一旦发生脑转移,患者的中位总生存期仅约7个月,1年生存率降至20%,预后极差。
当前乳腺癌脑转移的治疗面临诸多挑战:血脑屏障的存在限制了大部分药物的颅内穿透,现有系统治疗如抗HER2单抗、CDK4/6抑制剂、化疗等在脑转移患者中的疗效有限,且耐药性问题突出;同时,乳腺癌脑转移的核心机制尚未完全阐明,尤其是肿瘤微环境中的免疫抑制网络、细胞间互作的分子调控机制等仍存在研究空白。针对这一现状,本文系统综述了乳腺癌脑转移的多步骤核心机制,重点解析了肿瘤微环境的免疫抑制网络,并结合当前治疗现状提出了精准治疗的未来方向,为该领域寻找新型生物标志物和治疗靶点提供了全面的理论框架。
2. 文献综述解析
本文的综述内容按乳腺癌脑转移的核心生物学过程、肿瘤微环境免疫抑制网络、临床治疗现状与未来方向三个维度进行分类整合,系统梳理了领域内的研究进展与未解决问题。
在机制研究领域,现有研究已明确上皮-间质转化(EMT)、细胞外基质(ECM)重塑、代谢重编程是乳腺癌脑转移的关键生物学过程:EMT的驱动通路具有亚型特异性,HER2阳性乳腺癌主要依赖TGF-β/SMAD-SNAIL轴,三阴性乳腺癌则更倾向于Wnt/β-catenin通路激活;ECM重塑通过基质金属蛋白酶(MMPs)、赖氨酰氧化酶(LOX)等酶类改变基质结构,促进肿瘤侵袭,但第一代广谱MMP抑制剂因靶向范围过宽、毒性大等问题在临床Ⅲ期试验中失败;代谢重编程在转移的不同阶段呈现动态变化,原发肿瘤以Warburg效应为主,转移阶段则增强三羧酸循环和谷氨酰胺分解以满足能量需求,脑转移灶还会偏好脂肪酸氧化来适应颅内微环境。治疗研究方面,抗HER2抗体药物偶联物(ADC)如德曲妥珠单抗(T-DXd)在脑转移患者中显示出一定的颅内活性,但仍存在耐药问题;CDK4/6抑制剂可通过上调MHC-I表达、抑制调节性T细胞(Tregs)增殖来重塑免疫微环境,但相关临床数据仍较为有限;免疫检查点抑制剂如PD-1单抗在脑转移中的疗效不佳,因为脑转移的免疫抑制核心并非PD-1/PD-L1轴,而是LAG3-半乳糖凝集素3等替代通路。
现有研究的局限性在于:不同分子亚型的脑转移机制异质性研究不够深入,肿瘤微环境中各类细胞间互作的具体分子机制尚未完全阐明,缺乏有效的生物标志物用于脑转移的早期诊断和预后预测,治疗策略的联合应用也缺乏精准的患者分层依据。本文的创新点在于系统整合了乳腺癌脑转移的多步骤机制,重点剖析了肿瘤微环境的免疫抑制网络,包括适应性免疫细胞、固有免疫细胞与中枢神经系统特异性细胞的复杂互作,同时结合当前治疗现状提出了基于机制的精准治疗方向,为该领域的转化研究提供了全面的参考框架。
3. 研究思路总结与详细解析
本文作为一篇系统性综述,整体研究目标是全面阐述乳腺癌脑转移的核心分子机制、肿瘤微环境的免疫抑制网络,以及当前临床治疗的现状与未来精准治疗方向,核心科学问题聚焦于乳腺癌脑转移的多步骤调控机制、肿瘤微环境的免疫抑制核心通路,以及如何基于这些机制开发有效的诊断标志物和治疗策略。研究逻辑遵循“机制解析-微环境分析-治疗现状-未来方向”的闭环,通过系统检索和整合领域内的关键研究成果,构建了乳腺癌脑转移的完整机制框架。
3.1 乳腺癌脑转移核心生物学过程解析
本环节的核心目标是梳理乳腺癌脑转移从原发肿瘤侵袭到颅内定植的多步骤分子机制。研究方法为系统检索PubMed、Web of Science等数据库中关于乳腺癌脑转移机制的基础研究文献,按EMT、ECM重塑、代谢重编程、血脑屏障突破四个核心生物学过程分类整理,分析不同分子亚型的机制差异。
结果显示,EMT是乳腺癌脑转移的关键起始过程,HER2阳性乳腺癌主要由TGF-β/SMAD-SNAIL轴驱动EMT,而三阴性乳腺癌则更多依赖Wnt/β-catenin通路激活Snail、Twist等转录因子;ECM重塑通过TGF-β、Wnt、Hippo等信号通路调控MMPs、LOX等酶类的表达,改变基质的机械和结构特性,促进肿瘤细胞侵袭和血脑屏障突破;代谢重编程在转移的不同阶段呈现动态适应性变化,原发肿瘤阶段以糖酵解为主满足快速增殖需求,转移阶段则增强三羧酸循环和谷氨酰胺分解以提供能量,脑转移灶还会偏好脂肪酸氧化来适应颅内的营养环境;血脑屏障突破的机制包括破坏紧密连接(如ENPP1通过损伤胰岛素信号通路降低紧密连接蛋白表达,circBCBM1通过激活SHH通路上调MMP9表达)、免疫分子介导(补体C3激活脉络丛上皮细胞的C3a受体破坏血脑脊液屏障)、外泌体驱动(肿瘤细胞外泌体通过影响脑内皮细胞rab7表达破坏血脑屏障)。
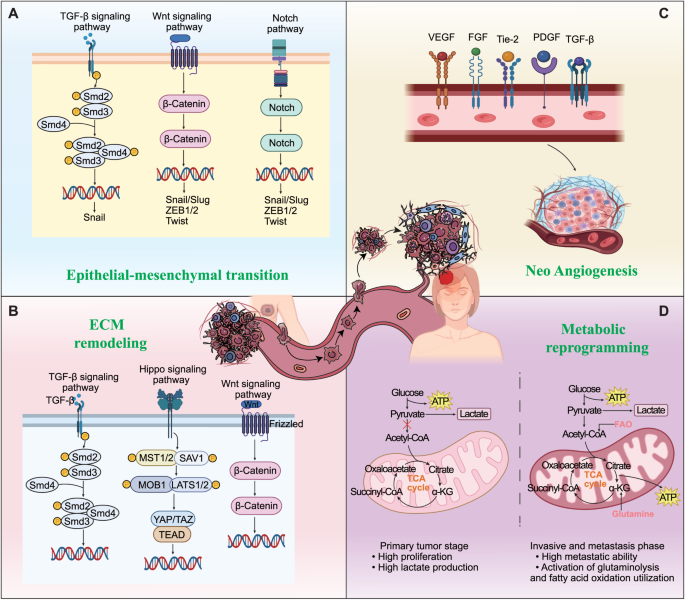
文献未提及具体实验产品,领域常规使用分子生物学试剂(如qRT-PCR试剂盒、Western Blot抗体)、细胞培养试剂、动物模型构建工具等。
3.2 肿瘤微环境免疫抑制网络解析
本环节的核心目标是解析乳腺癌脑转移肿瘤微环境中各类细胞的互作机制,揭示免疫抑制网络的核心组成。研究方法为系统检索关于乳腺癌脑转移肿瘤微环境的单细胞测序、空间转录组、动物实验等文献,按适应性免疫细胞、固有免疫细胞、中枢神经系统特异性细胞三类进行分类整理,总结细胞间的信号调控通路和功能互作。
结果显示,适应性免疫层面,脑转移灶中CD8+T细胞呈现耗竭表型且浸润不足,Tregs、M2型巨噬细胞等免疫抑制细胞富集,肿瘤细胞和巨噬细胞分泌的半乳糖凝集素3通过与T细胞表面的LAG3结合,抑制T细胞激活并诱导凋亡;固有免疫层面,脑相关巨噬细胞(BAMs)通过分泌VEGF、MMP9等因子增加血脑屏障通透性,促进肿瘤细胞颅内定植,肿瘤相关中性粒细胞(TANs)可从抗肿瘤的N1型极化为促转移的N2型,通过释放中性粒细胞胞外陷阱(NETs)捕获肿瘤细胞并促进其存活,自然杀伤(NK)细胞的功能被缺氧、腺苷等颅内微环境因素抑制,髓源性抑制细胞(MDSCs)通过抑制JAK3-Stat5通路阻断NK细胞激活;中枢神经系统特异性细胞层面,星形胶质细胞通过分泌IFNα、TNF-α等细胞因子促进肿瘤细胞生长,还可诱导肿瘤细胞上调神经元特异性周期蛋白依赖性激酶5(Cdk5),进而下调MHC-I表达逃避免疫识别,小胶质细胞可在不同微环境下极化为M1或M2型,M2型小胶质细胞通过分泌VEGF、TGF-β等因子促进肿瘤转移,脑转移相关成纤维细胞(bmCAFs)通过分泌信号因子增强肿瘤细胞的迁移和侵袭能力。
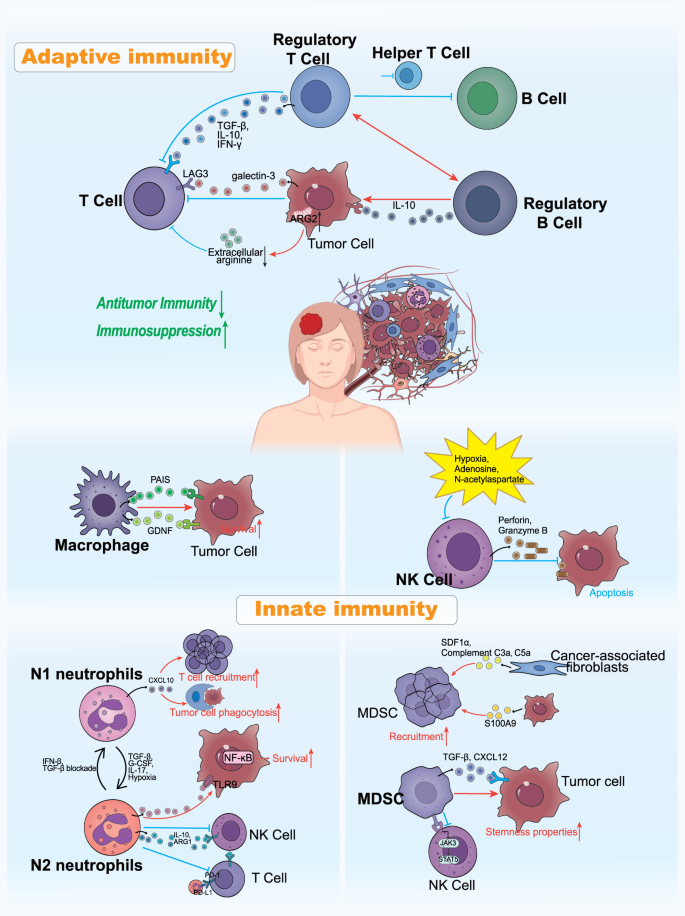
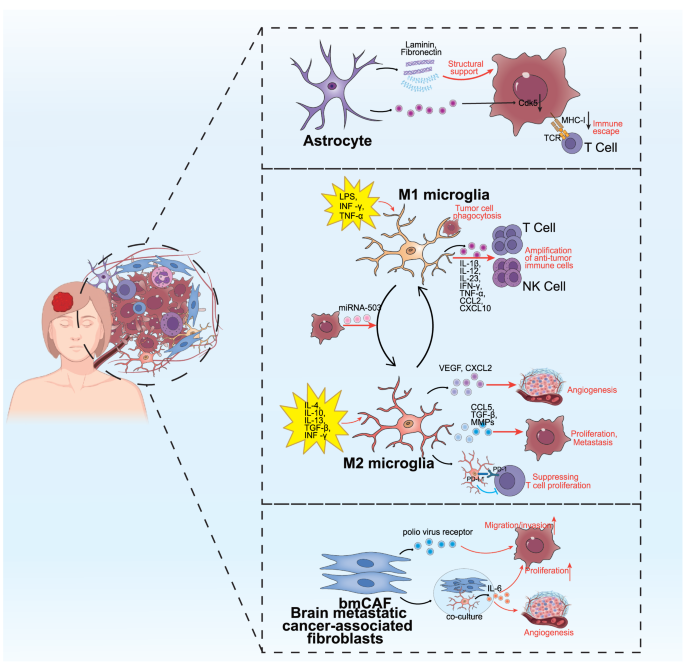
文献未提及具体实验产品,领域常规使用流式细胞仪、免疫组化(IHC)试剂盒、单细胞测序平台、空间转录组分析工具等。
3.3 临床治疗现状与未来方向解析
本环节的核心目标是评估当前乳腺癌脑转移的临床治疗策略疗效,提出基于机制的精准治疗方向。研究方法为系统检索关于乳腺癌脑转移治疗的临床研究文献,包括随机对照试验、单臂试验等,按治疗类型分类整理,分析疗效数据和局限性。
结果显示,抗HER2治疗中,T-DXd在HER2阳性脑转移患者中显示出较好的颅内客观缓解率,但仍存在耐药问题;CDK4/6抑制剂可通过恢复CD8+T细胞功能、抑制Tregs增殖来重塑免疫微环境,但其在脑转移患者中的临床数据仍较为有限;免疫治疗方面,PD-1单抗单药疗效不佳,联合LAG3抑制剂等替代免疫检查点阻断可能更具临床价值;ADC和肽-药物偶联物(PDC)如ANG1005通过主动靶向血脑屏障相关受体实现颅内药物递送,显示出一定的临床潜力。未来的精准治疗方向包括:基于亚型的EMT靶向联合治疗,如针对HER2阳性的TGF-β通路抑制剂联合抗HER2治疗;精准的ECM靶向治疗,选择亚型特异性的MMP或LOX抑制剂;血脑屏障调控策略,如通过聚焦超声瞬时开放血脑屏障、使用脑穿透性载体增强药物递送;免疫抑制网络的联合阻断,如LAG3与半乳糖凝集素3抑制剂联合PD-1单抗;以及人工智能(AI)与多组学技术结合,用于患者分层和治疗决策优化。
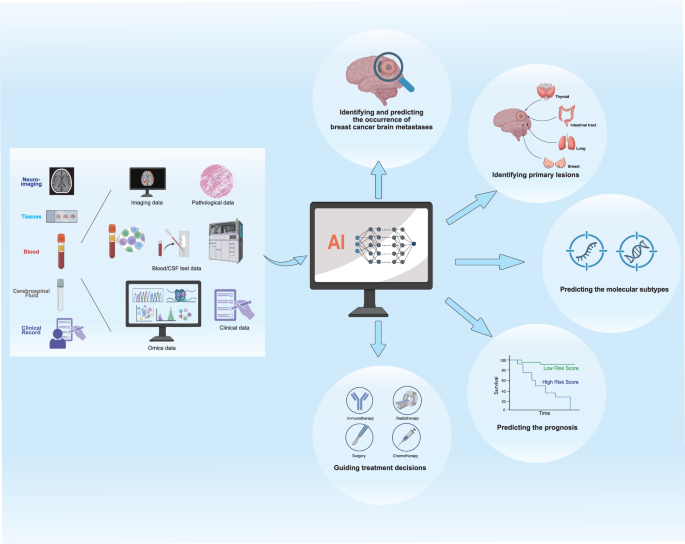
文献未提及具体实验产品,领域常规使用临床治疗药物(如T-DXd、帕博利珠单抗)、影像设备(如MRI)、AI分析平台等。
4. Biomarker研究及发现成果解析
本文中涉及的Biomarker类型包括循环肿瘤细胞(CTCs)、循环肿瘤DNA(ctDNA)、蛋白质标志物、代谢物标志物,其筛选与验证逻辑基于临床样本分析和数据库挖掘,通过评估Biomarker与乳腺癌脑转移的相关性,验证其诊断、预后预测价值。
在研究过程中,CTCs可作为动态监测乳腺癌进展的工具,但对脑转移的特异性有限,连续监测CTCs的动态变化比单次计数更能预测疾病进展;脑脊液ctDNA检测脑转移的准确率超过90%,但采样具有侵入性,限制了其临床应用;血浆中的神经元或胶质细胞来源的甲基化标志物可用于脑转移的早期定位,但其临床价值仍需多中心前瞻性研究验证;蛋白质标志物中,癌胚抗原(CEA)、糖类抗原153(CA153)是常规的乳腺癌监测指标,骨膜蛋白(POSTN)由CAFs分泌,其预测远处转移的效能与CA153相当,可作为补充标志物;代谢物标志物方面,脑转移患者血浆中的11种代谢物(如丙氨酸、鞘氨醇、果糖等)浓度显著升高,基于5种和10种代谢物构建的预测模型准确率分别为94.6%和95.2%,具有非侵入性的优势。
核心成果方面,这些Biomarker可用于乳腺癌脑转移的早期诊断、风险分层和预后预测,其中POSTN可作为CEA和CA153的补充标志物,代谢物标志物为非侵入性早期诊断提供了新的方向。本文的创新性在于系统总结了各类Biomarker的研究现状,提出了多组学整合的Biomarker模型的发展方向,为乳腺癌脑转移的早期筛查和精准治疗提供了依据。统计学结果方面,POSTN预测远处转移的效能与CA153相当(文献未明确具体数据),代谢物预测模型的准确率为94.6%(5种代谢物)和95.2%(10种代谢物)(文献未明确样本量和P值)。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。