Blood biomarkers for mild traumatic brain injury: a selective review of unresolved issues
轻度创伤性脑损伤的血液生物标志物:未解决问题的选择性综述
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2021 | 起止号: | 2021 Sep 16;9(1):70 |
| doi: | 10.1186/s40364-021-00325-5 | 研究方向: | 神经科学 |
文献解析
1. 领域背景与文献引入
文献英文标题:Blood biomarkers for mild traumatic brain injury: a selective review of unresolved issues;发表期刊:Biomark Res;影响因子:未公开;研究领域:轻度创伤性脑损伤(mTBI)血液生物标志物研究。
轻度创伤性脑损伤(mTBI,又称脑震荡)是一类格拉斯哥昏迷评分(GCS)13-15分的轻度脑损伤,临床特征为短暂意识丧失、逆行性遗忘或认知障碍,但头颅CT/MRI多无明显结构异常。其诊断主要依赖症状评估(如头痛、头晕),存在主观偏倚、漏诊或过度影像学检查的痛点。血液生物标志物作为客观量化指标,可辅助mTBI的早期诊断、严重程度分层及预后预测,成为近年研究热点。然而,现有研究仍存在多个关键瓶颈:生物标志物进入血液的具体途径不明确、动力学特征(半衰期、达峰时间)未精准定义、临床预测能力(如区分脑震荡与健康人)有限。本文针对神经丝轻链(NF-L)、泛素羧基末端水解酶L1(UCH-L1)、tau蛋白、S100钙结合蛋白B(S100B)、胶质纤维酸性蛋白(GFAP)五类常用生物标志物,聚焦“生物标志物进出血液的途径、血液动力学、临床预测能力”三个核心领域,系统梳理八个未解决问题,为mTBI血液生物标志物的临床转化与未来研究提供方向。
2. 文献综述解析
作者将现有mTBI血液生物标志物研究归纳为三个核心方向:生物标志物进入血液的途径、血液动力学特征、临床预测能力,并针对以下八个未解决问题展开聚焦回顾:①生物标志物进出血液的具体通路;②血液动力学参数(达峰时间、半衰期);③最佳采样时间;④生物标志物持续升高的时长与意义;⑤ confounding因素(如年龄、肾功)的影响;⑥诊断脑震荡/亚脑震荡的能力;⑦预测CT扫描阳性的有效性;⑧预测预后及严重程度的价值。
现有研究的核心结论包括:①mTBI后生物标志物可通过血脑屏障破坏、glymphatic系统(脑脊液-淋巴通路)或脑间质液的淋巴引流进入血液,但具体通路的相对贡献未量化;②动力学参数初步明确(如S100B半衰期0.5-2小时、GFAP半衰期约24小时),但达峰时间(Tmax)的估算存在差异(如NF-L的Tmax推测为100-300小时);③临床应用中,生物标志物预测CT阳性的效果最佳(如S100B的敏感性97%),但区分脑震荡与健康对照(AUROC多低于0.8)、预测预后(如恢复时间)的能力有限。
现有研究的优势在于初步建立了生物标志物与mTBI的关联,为临床应用提供了理论基础;局限则包括:通路机制未明确、动力学参数不精准、未常规校正confounding因素、预测预后的证据不足。作者通过对比这些“未解决问题”,凸显本文的创新价值——首次系统梳理mTBI血液生物标志物的研究瓶颈,明确了“机制-动力学-临床应用”的研究链条。
3. 研究思路总结与详细解析
本文为聚焦综述研究,研究思路遵循“问题提出→文献检索→问题分析→结论总结”的闭环逻辑,针对八个未解决问题展开系统回顾。
3.1 未解决问题的筛选
实验目的:基于现有研究的局限,提炼mTBI血液生物标志物研究中最关键的未解决问题。
方法细节:作者回顾近年mTBI生物标志物综述(如McDonald等2021年的研究),结合临床需求(如减少CT检查、预测预后),最终筛选出八个问题,涵盖“基础机制(途径、动力学)-临床应用(诊断、预测)”全链条。
结果解读:八个问题包括:生物标志物进出血液的途径、血液动力学特征、最佳采样时间、持续升高的时长与意义、confounding因素、诊断脑震荡/亚脑震荡、预测CT阳性、预测预后。这些问题是mTBI生物标志物临床应用的核心障碍。
3.2 文献检索策略
实验目的:获取与八个未解决问题相关的文献,确保综述的全面性与针对性。
方法细节:①检索Ovid MEDLINE(1946至2021年2月5日),关键词为“traumatic brain injuries”与“UCH-L1 OR GFAP OR tau proteins OR S100 proteins OR neurofilament proteins”,共获得406篇文献;②补充检索“glymphatic system OR periarterial drainage”相关文献202篇;③通过特设检索获取195篇文献。最终通过标题与摘要筛选,纳入140篇文献进行分析。
结果解读:检索策略覆盖了mTBI生物标志物的核心研究方向,确保了综述的文献基础。
3.3 未解决问题的分析与结果总结
实验目的:针对每个未解决问题,总结现有研究的结论与争议。
方法细节:对纳入的140篇文献按八个问题分类,提取关键结果(如生物标志物的途径、动力学参数、临床预测值)。
结果解读:
(1)生物标志物进出血液的途径:mTBI后生物标志物可通过三种途径进入血液——血脑屏障破坏、glymphatic系统(脑脊液沿血管周围间隙流动至淋巴系统)、脑间质液的淋巴引流,但具体通路的相对贡献未明确。例如,血脑屏障破坏仅在部分mTBI患者中存在,而glymphatic系统的贡献未量化。
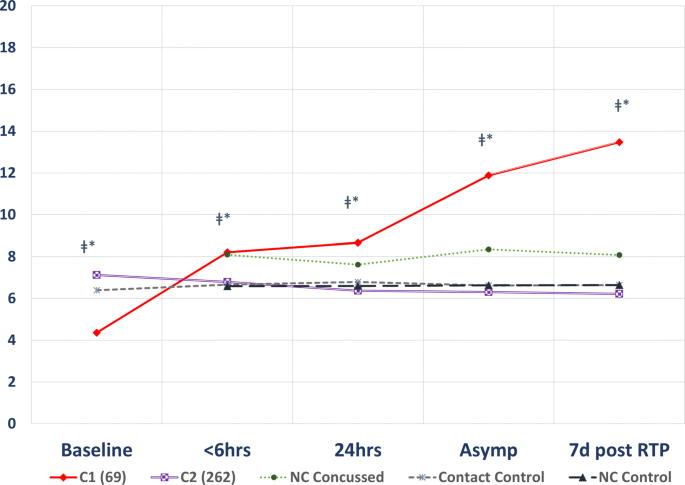
(Figure 1展示了NF-L在脑震荡患者中的轨迹聚类,提示生物标志物释放的异质性,可能与进入途径相关)。
(2)血液动力学特征:现有研究提供了部分动力学参数,但缺乏精准的达峰时间(Tmax)与消除速率常数。例如:S100B半衰期0.5-2小时,Tmax约1-3小时;GFAP半衰期约24小时,Tmax约12-36小时;NF-L的Tmax推测为100-300小时,但未实证验证。
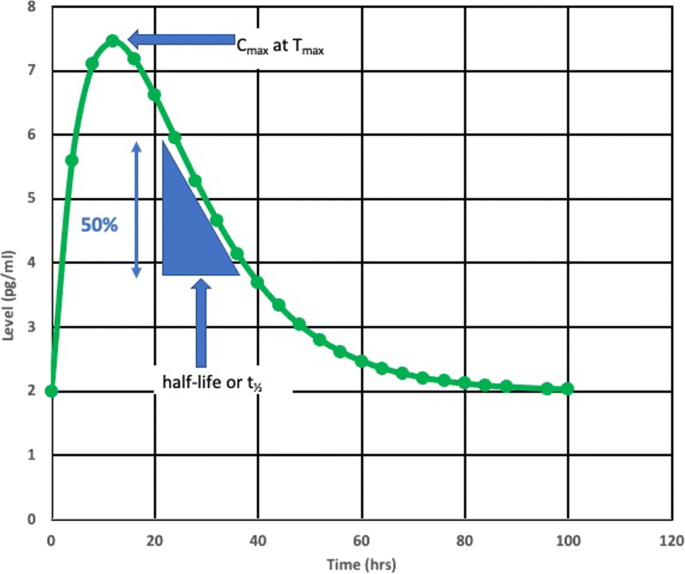
(Figure 2展示了生物标志物的时间-浓度曲线,说明动力学参数对采样时间的影响)。
(3)最佳采样时间:基于动力学参数推测:S100B最佳采样时间0-4小时,UCH-L1与tau为4-12小时,GFAP为12-36小时,NF-L为100-300小时,但缺乏实证研究验证。
(4)生物标志物持续升高的时长与意义:NF-L可能在mTBI后持续升高数月至数年,但其意义不明,可能与持续神经损伤或再损伤有关;S100B、UCH-L1等半衰期较短,30天后多恢复正常。
(5)confounding因素的影响:年龄、肾功不全、血容量增加会升高生物标志物水平(如老年患者GFAP水平更高),但现有研究未常规校正这些因素,可能影响结果准确性。
(6)诊断脑震荡/亚脑震荡的能力:生物标志物区分脑震荡与健康对照的AUROC多在0.6-0.7之间(如UCH-L1的AUROC 0.65);识别亚脑震荡(如运动中的头部撞击)的能力更有限,部分研究未发现S100B在亚脑震荡后升高。
(7)预测CT扫描阳性的有效性:S100B与GFAP表现最佳。S100B在6小时内的敏感性97%、特异性34%(cutoff 100 pg/ml),可辅助减少不必要的CT检查;GFAP的AUROC约0.85,预测效果优于S100B。
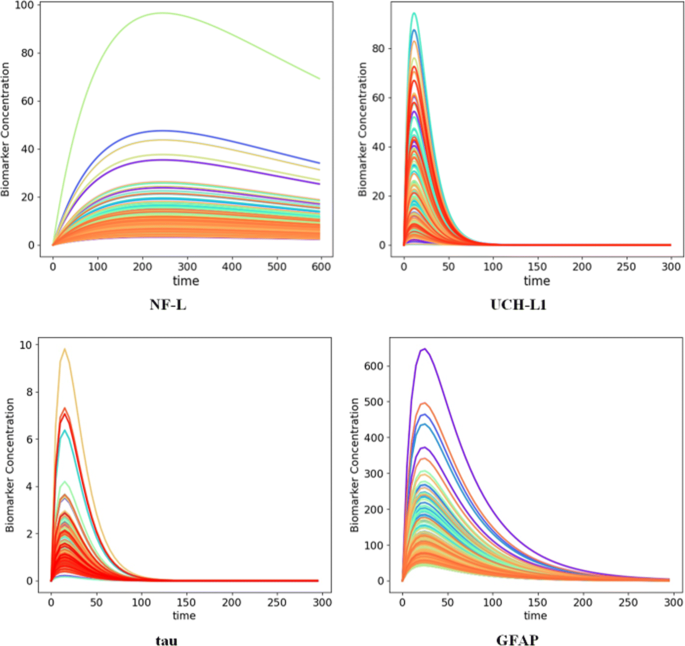
(Figure 3展示了基于动力学模型的生物标志物时间-浓度曲线,说明采样时间对预测CT阳性的影响)。
(8)预测预后及严重程度的价值:生物标志物预测mTBI预后(如恢复时间、post-concussion综合征)的AUROC多低于0.8,仅NF-L与tau对运动员返回赛场有一定预测价值(如NF-L水平与返回时间相关),但结果不一致。
4. Biomarker研究及发现成果解析
Biomarker定位
本文涉及的mTBI血液生物标志物分为两类:①神经源性标志物(来自神经元):神经丝轻链(NF-L)、泛素羧基末端水解酶L1(UCH-L1)、tau蛋白;②胶质源性标志物(来自胶质细胞):S100钙结合蛋白B(S100B)、胶质纤维酸性蛋白(GFAP)。筛选逻辑基于“研究热度”与“临床相关性”,这五类标志物是mTBI中研究最广泛的血液生物标志物。
研究过程详述
- 来源:生物标志物均来自mTBI患者的血液样本(血浆或血清)。
- 验证方法:常用检测方法包括酶联免疫吸附试验(ELISA)、单分子阵列(SIMOA)、点护理测试(POCT)等。例如,GFAP与UCH-L1的点护理测试可在15分钟内获得结果,适用于急诊场景。
- 特异性与敏感性:
- S100B:预测CT阳性的敏感性97%(6小时内)、特异性34%(cutoff 100 pg/ml);
- GFAP:预测CT阳性的AUROC约0.85;
- 区分脑震荡与健康对照:GFAP的AUROC最高(约0.76),tau最低(约0.55)。
核心成果提炼
- 临床价值分层:生物标志物的临床价值存在差异——S100B与GFAP在预测CT阳性中表现最佳,可辅助减少不必要的影像学检查;NF-L与tau对运动员返回赛场有一定预测价值,但需更多研究验证。
- 未解决问题:①生物标志物的具体作用机制(如NF-L持续升高的原因);②最佳采样时间(如NF-L的Tmax未确定);③confounding因素的校正(如年龄对GFAP的影响)。
- 创新性:首次系统梳理了mTBI血液生物标志物的八个未解决问题,明确了“机制-动力学-临床应用”的研究链条。例如,作者提出“生物标志物释放量(D0)可能比单次采样浓度更能反映损伤severity”,为动力学模型的优化提供了新思路。
注:本文为综述类研究,未涉及原创实验,部分数据(如动力学参数)来自纳入的原始研究。文中未提及具体实验产品,领域常规使用ELISA、SIMOA等试剂检测生物标志物水平。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。