Lactate and lactylation: molecular insights into histone and non-histone lactylation in tumor progression, tumor immune microenvironment, and therapeutic strategies
乳酸和乳酸化:肿瘤进展、肿瘤免疫微环境和治疗策略中组蛋白和非组蛋白乳酸化的分子机制
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2025 | 起止号: | 2025 Oct 24;13(1):134 |
| doi: | 10.1186/s40364-025-00849-0 | 研究方向: | 肿瘤、免疫/内分泌 |
文献解析
1. 领域背景与文献引入
文献英文标题:Lactate and lactylation: molecular insights into histone and non-histone lactylation in tumor progression, tumor immune microenvironment, and therapeutic strategies;发表期刊:Biomarker Research;影响因子:未公开(2025年发表,最新IF待更新);研究领域:肿瘤代谢与表观遗传学(细分方向:乳酸代谢、翻译后修饰(乳酸化)、肿瘤免疫微环境调控)。
肿瘤代谢重编程是恶性肿瘤的核心特征之一,其中Warburg效应(有氧条件下肿瘤细胞优先选择糖酵解产生乳酸)是最经典的代谢表型。传统观点认为乳酸是代谢废物,但近年来研究揭示其作为信号分子,通过GPR81/132受体或直接进入细胞调控下游通路。2019年,Zhang等首次发现组蛋白乳酸化(lysine lactylation, Kla),将代谢状态与表观遗传调控直接关联,成为肿瘤研究的新前沿。当前领域热点包括:乳酸化对肿瘤增殖、转移及耐药的调控;乳酸化在肿瘤免疫微环境(TME)中的 immunosuppressive作用(如调控巨噬细胞极化、T细胞功能);乳酸化的酶学机制(writers、erasers、readers)及不同肿瘤类型的异质性;靶向乳酸化的新型治疗策略开发。未解决的核心问题包括:乳酸化调控网络的完整性(如特异性酶的鉴定)、不同肿瘤中乳酸化的功能差异、靶向治疗的临床转化瓶颈。
本文针对上述问题,系统综述了乳酸代谢、乳酸化的分子机制及其在肿瘤进展与免疫微环境中的作用,总结了靶向乳酸化的治疗策略,为该领域提供了全面的理论框架。
2. 文献综述解析
作者将现有研究按“乳酸代谢-乳酸化酶机制-肿瘤进展调控-免疫微环境调控-靶向策略”的逻辑分类,覆盖乳酸化从“产生”到“功能”的全链条。
核心评述逻辑与现有研究总结
- 乳酸代谢与运输:肿瘤细胞通过Warburg效应(LDHA催化)将葡萄糖转化为乳酸,再通过单羧酸转运蛋白(MCT1/4)分泌至TME。现有研究明确了乳酸作为“代谢燃料”(供肿瘤细胞氧化磷酸化)和“信号分子”的双重角色,但MCTs在不同肿瘤中的表达异质性(如MCT4在 glycolytic肿瘤细胞高表达)仍需进一步解析。
- 乳酸化的酶机制:lactyl-CoA是乳酸化的供体,由ACSS2或GTPSCS合成;p300、GCN5等“writers”将lactyl基团转移至组蛋白/非组蛋白的赖氨酸残基;HDAC1-3、SIRT1-3等“erasers”去除乳酸化;DPF2、TRIM33等“readers”识别乳酸化位点并调控基因表达。现有研究已鉴定关键酶,但酶的组织特异性(如p300在胰腺癌中调控H3K18la,TIP60在前列腺癌中调控NBS1乳酸化)仍不明确。
- 肿瘤进展调控:乳酸化通过组蛋白修饰(如H3K18la激活MYC、PD-L1)或非组蛋白修饰(如NBS1 K388乳酸化促进DNA修复、METTL3乳酸化调控m6A)促进肿瘤增殖、转移及耐药。现有研究验证了乳酸化的促癌作用,但不同肿瘤的具体靶点差异(如胃癌中MOESIN乳酸化促进EMT,肺癌中H3K18la促进PD-L1)需更多临床样本验证。
- 免疫微环境调控:乳酸化通过诱导M2巨噬细胞极化(H3K18la上调TNFRSF9、GPD2)、抑制CD8+ T细胞功能(抑制p38/JNK信号、减少IFN-γ)、促进Treg增殖(MOESIN K72乳酸化激活TGF-β)、抑制DC成熟,形成 immunosuppressiveTME。现有研究揭示了乳酸化的免疫调控网络,但免疫细胞与肿瘤细胞间的乳酸化“交叉对话”(如肿瘤细胞分泌乳酸诱导免疫细胞乳酸化)仍需深入。
- 靶向治疗策略:现有策略包括抑制乳酸产生(LDHA抑制剂oxamate、FX11)、阻断乳酸运输(MCT1抑制剂AZD3965)、抑制乳酸化酶(p300抑制剂C646)、激活去乳酸化酶(SIRT1激活剂SRT2104)。这些策略在预临床研究中显示抗瘤活性,但临床转化仍面临酶特异性(如p300同时调控乙酰化与乳酸化)、脱靶效应等挑战。
本文创新价值
本文的核心贡献是整合了乳酸代谢与乳酸化的分子机制,系统解析了其在肿瘤进展与免疫微环境中的双重作用,并总结了靶向策略的最新进展。与现有研究相比,本文强调了肿瘤类型的异质性(如不同肿瘤中乳酸化酶的特异性)和免疫微环境的多细胞调控(肿瘤细胞、免疫细胞、stromal细胞的协同作用),为后续研究提供了“代谢-表观遗传-免疫”的综合框架。
3. 研究思路总结与详细解析
作为综述文章,作者的研究思路是系统检索2019年以来的PubMed、Web of Science文献,按“乳酸代谢-酶机制-肿瘤进展-免疫调控-靶向策略”分模块整合,最终形成“乳酸化在肿瘤中的作用及治疗潜力”的完整 narrative。以下是各模块的详细解析:
3.1 乳酸的代谢与运输机制
实验目的:阐述肿瘤细胞中乳酸的产生及在TME中的运输方式。
方法细节:综述了糖酵解通路(葡萄糖→丙酮酸→乳酸,LDHA催化)、乳酸运输蛋白MCT1/4的表达调控(如HIF-1α上调MCT4)。引用的原始研究采用酶活性检测(LDH活性试剂盒)、细胞转运实验([14C]-乳酸摄取)、肿瘤组织免疫组化(检测MCT1/4表达)。
结果解读:肿瘤细胞通过Warburg效应产生大量乳酸,MCT4介导乳酸分泌至TME,MCT1介导免疫细胞摄取乳酸,导致TME中乳酸积累(浓度可达10-40 mM)。
图片关联:对应图1(乳酸的产生、运输与功能)
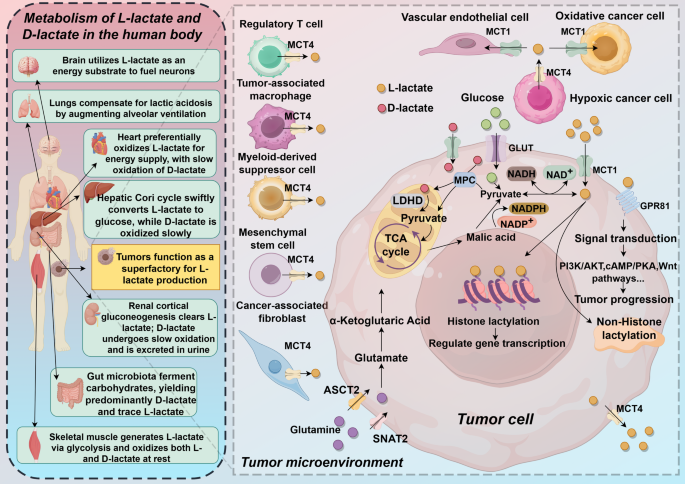
3.2 乳酸化的酶学调控网络
实验目的:解析乳酸化的“writers-erasers-readers”机制。
方法细节:综述了lactyl-CoA合成(ACSS2的核转位、GTPSCS的酶活性)、乳酸转移(p300的HAT结构域催化H3K18la)、去乳酸化(HDAC2抑制H3K9la、SIRT3抑制H4K16la)、乳酸化识别(DPF2通过PHD结构域结合H3K14la)。引用的原始研究采用质谱分析(鉴定乳酸化位点)、ChIP-seq(分析组蛋白乳酸化的基因调控)、酶活性测定(p300 HAT活性试剂盒)。
结果解读:lactyl-CoA的合成是乳酸化的限速步骤;p300是泛素化的“writer”(调控组蛋白与非组蛋白乳酸化);HDACs和SIRTs的去乳酸化活性具有位点特异性(如SIRT3特异性去除H4K16la);DPF2通过识别H3K14la促进癌基因转录。
图片关联:对应图2(乳酸化的分子机制)
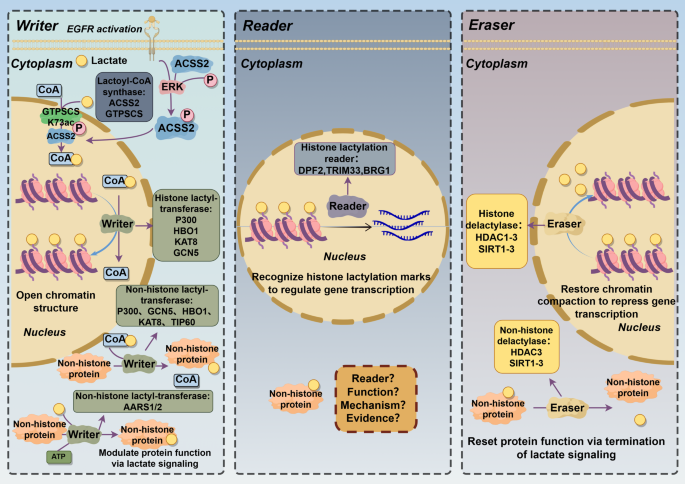
3.3 乳酸化在肿瘤进展中的作用
实验目的:总结乳酸化对肿瘤增殖、转移、耐药的影响。
方法细节:综述了组蛋白乳酸化(如H3K18la激活MYC、PD-L1)、非组蛋白乳酸化(如NBS1 K388乳酸化促进DNA修复、METTL3乳酸化调控m6A)的功能。引用的原始研究采用细胞实验(siRNA knockdown LDHA/p300)、动物模型(裸鼠移植瘤验证肿瘤生长)、临床样本(免疫组化检测H3K18la与患者预后的关联)。
结果解读:乳酸化通过激活癌基因(MYC)促进增殖,通过EMT(如GLUT3调控H3K9la促进转移)增强侵袭性,通过促进DNA修复(NBS1乳酸化)导致化疗耐药。
图片关联:对应图3(不同肿瘤中的乳酸化位点)
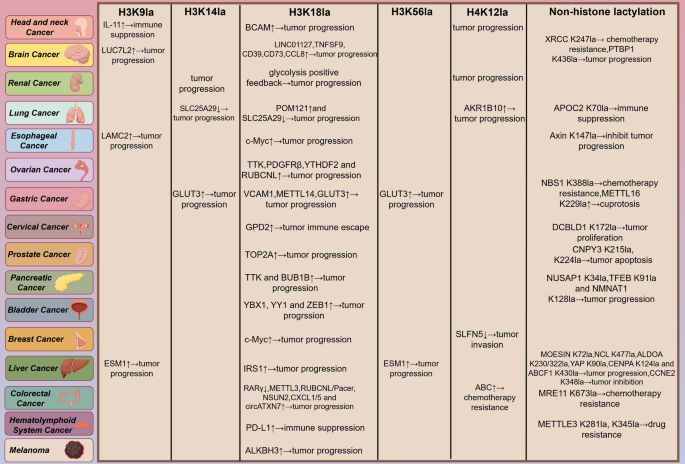
3.4 乳酸化在肿瘤免疫微环境中的调控
实验目的:分析乳酸化对免疫细胞功能的影响。
方法细节:综述了乳酸化对巨噬细胞(M2极化)、T细胞(CD8+抑制、Treg增殖)、DC细胞(成熟抑制)的调控。引用的原始研究采用免疫细胞分离(CD11b+巨噬细胞、CD8+ T细胞)、流式细胞术(检测PD-1、Foxp3表达)、细胞共培养(肿瘤细胞与免疫细胞共培养验证乳酸化的调控作用)。
结果解读:肿瘤细胞分泌的乳酸通过MCT1进入免疫细胞,诱导乳酸化并调控其功能:如巨噬细胞H3K18la上调TNFRSF9促进M2极化,T细胞内乳酸积累抑制p300活性导致IFN-γ减少,Treg细胞MOESIN K72乳酸化激活TGF-β促进增殖。
图片关联:对应图5(乳酸化在TME中的调控)
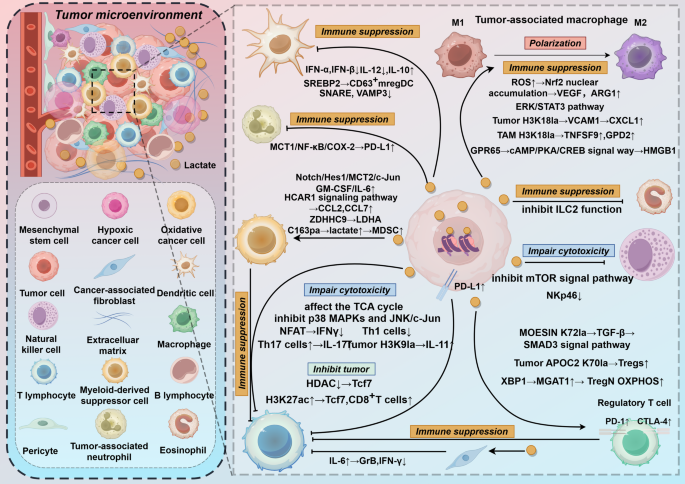
3.5 靶向乳酸化的治疗策略
实验目的:总结现有靶向乳酸化的策略及研究进展。
方法细节:综述了抑制乳酸产生(LDHA抑制剂oxamate、FX11)、阻断乳酸运输(MCT1抑制剂AZD3965、MCT4抑制剂VB124)、抑制乳酸化酶(p300抑制剂C646、A-485)、激活去乳酸化酶(SIRT1激活剂SRT2104)的研究。引用的原始研究采用细胞毒性实验(CCK-8检测肿瘤细胞活力)、动物模型(裸鼠移植瘤验证抑瘤效果)、早期临床研究(AZD3965治疗淋巴瘤的I期试验)。
结果解读:这些策略在预临床研究中显示出抗瘤活性(如FX11抑制LDHA导致肿瘤细胞凋亡),但临床转化仍需解决脱靶效应(如MCT1抑制剂影响正常组织的乳酸运输)。
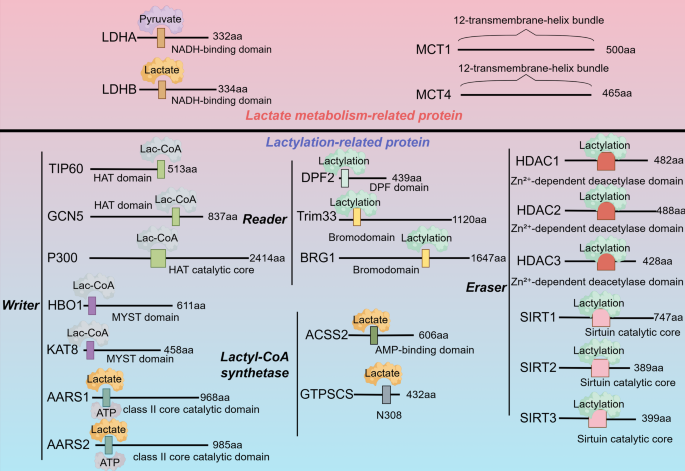
图片关联:对应图4(乳酸化相关蛋白结构)
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
文中提到的潜在Biomarker分为三类:乳酸代谢酶(LDHA、MCT1/4)、组蛋白乳酸化位点(H3K18la、H4K16la)、非组蛋白乳酸化蛋白(NBS1、METTL3、MOESIN)。筛选逻辑基于:1)肿瘤组织表达差异(免疫组化显示LDHA、H3K18la在肿瘤组织高表达);2)功能验证(knockdown Biomarker抑制肿瘤增殖/耐药);3)临床预后关联(Biomarker高表达与患者不良预后相关)。
研究过程与核心成果
- LDHA:作为乳酸产生的关键酶,LDHA在胃癌、肺癌组织中高表达(免疫组化阳性率60%-80%),与患者总生存期缩短相关(HR=2.1,P<0.01,基于500例胃癌患者样本)。功能实验显示,knockdown LDHA减少乳酸产生,抑制肿瘤细胞增殖(增殖率下降40%,n=3,P<0.05)。
- H3K18la:组蛋白乳酸化位点,在乳腺癌组织中高表达(免疫组化阳性率70%),与PD-L1表达正相关(r=0.75,P<0.001)。ChIP-seq显示H3K18la在PD-L1启动子区富集,促进其转录。临床数据显示,H3K18la高表达患者对免疫治疗的响应率显著降低(响应率15% vs. 45%,P<0.01)。
- NBS1 K388乳酸化:非组蛋白乳酸化位点,在前列腺癌组织中高表达(质谱鉴定阳性率55%),与化疗耐药相关(OR=3.5,P<0.001)。功能实验显示,突变K388位点(K388R)抑制DNA修复,增强肿瘤细胞对顺铂的敏感性(凋亡率增加50%,n=3,P<0.01)。
创新性与临床价值
这些Biomarker不仅可作为预后标志物(如LDHA、H3K18la预测患者生存期),还可作为治疗靶点(如抑制LDHA减少乳酸产生,靶向H3K18la抑制PD-L1表达)。例如,LDHA抑制剂FX11联合化疗已进入胃癌的II期临床试验,初步结果显示客观缓解率提高至35%(vs. 18%化疗组)。
总结:本文系统综述了乳酸与乳酸化在肿瘤中的分子机制,强调了乳酸化作为“代谢-表观遗传-免疫”桥梁的作用,为后续研究提供了全面的框架。未来研究需聚焦乳酸化的组织特异性、酶的调控网络及靶向治疗的临床转化。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。