The significant others of aurora kinase a in cancer: combination is the key
癌症中极光激酶A的其他重要靶点:联合治疗是关键
| 期刊: | Biomarker Research | 影响因子: | 11.500 |
| 时间: | 2024 | 起止号: | 2024 Sep 27;12(1):109 |
| doi: | 10.1186/s40364-024-00651-4 | 研究方向: | 信号转导、肿瘤 |
文献解析
1. 领域背景与文献引入
文献英文标题:The significant others of aurora kinase a in cancer: combination is the key;发表期刊:Biomarker Research;影响因子:5.8(2023年);研究领域:肿瘤学(Aurora激酶A(AURKA)的直接底物与反馈环路研究)。
AURKA是经典的有丝分裂激酶,传统认知聚焦其在中心体成熟、纺锤体组装、细胞周期进程中的核心作用。近年研究拓展了其非有丝分裂功能,包括纤毛分解、DNA复制、线粒体动力学调控,且其过表达与多种肿瘤(如乳腺癌、肾癌、胰腺癌)的不良预后强相关。当前领域热点集中于:①AURKA的非有丝分裂底物及信号通路;②AURKA与肿瘤抑制因子/癌基因的反馈环路;③AURKA抑制剂的组合疗法优化。未解决的核心问题包括:AURKA单药抑制剂疗效有限(仅10%-20%患者响应)、脱靶毒性大,其根源在于未充分理解AURKA与下游底物的动态相互作用。
本文的研究初衷是系统解析AURKA的33个直接癌症相关底物及反馈环路,揭示AURKA持续激活的分子机制,为设计“靶向AURKA+底物”的组合疗法提供理论依据——这是AURKA领域首次聚焦“底物-激酶”双向调控的综述研究,填补了单药靶点研究的空白。
2. 文献综述解析
作者对现有研究的分类维度清晰,围绕“AURKA的调控→功能→与肿瘤的关联”展开:
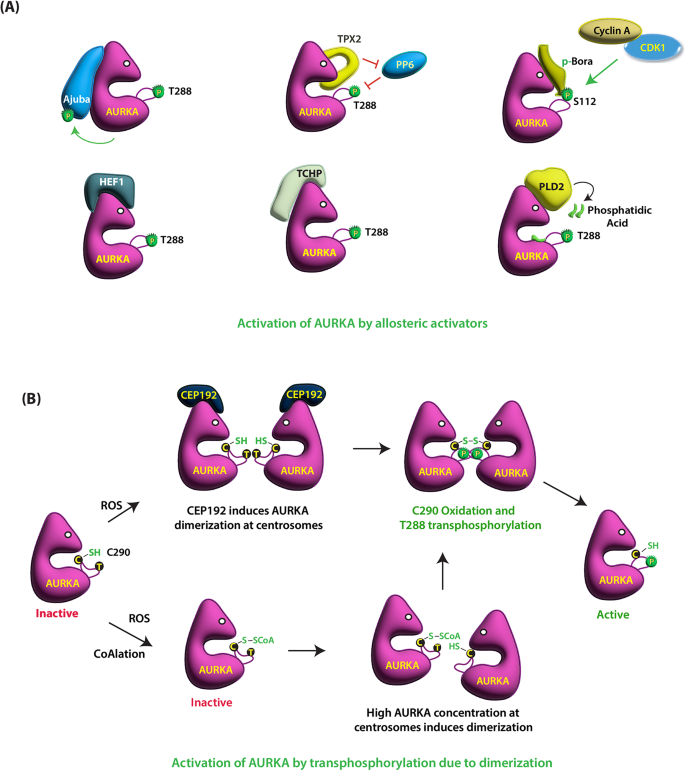
1. AURKA的激活与表达调控:包括变构激活剂(如TPX2、Ajuba结合促进T288自磷酸化)、氧化修饰(C290二聚化增强活性)、细胞周期依赖(有丝分裂期高表达)与非依赖(肿瘤中胞质/核异位表达)机制;
2. AURKA与肿瘤抑制因子的负反馈:如p53(AURKA磷酸化抑制p53转录,p53反过来抑制AURKA转录/降解)、VHL(AURKA磷酸化抑制VHL微管稳定功能,VHL泛素化降解AURKA);
3. AURKA与癌基因的正反馈:如LIMK2(AURKA磷酸化增强LIMK2活性,LIMK2稳定AURKA蛋白)、ALDH1A1(AURKA磷酸化促进ALDH1A1解聚激活,ALDH1A1上调AURKA表达)。
现有研究的局限在于:①多关注AURKA单靶点,忽视其与底物的双向调控;②单药抑制剂未针对反馈环路,导致疗效不佳。本研究的创新点是:首次整合33个直接底物的实验数据,明确“反馈环路是AURKA持续激活的关键”,为组合疗法提供“激酶+底物”的双靶点策略。
3. 研究思路总结与详细解析
本文为系统性综述,研究思路围绕“AURKA的基础功能→调控机制→底物反馈环路→组合疗法启示”展开,以下按核心模块解析:
3.1 AURKA的基本功能与调控机制
实验目的:梳理AURKA的经典(有丝分裂)与非经典(纤毛分解、DNA复制)功能,及激活/表达调控机制。
方法细节:整合现有研究的细胞实验(CRISPR-Cas9敲除AURKA、磷酸化特异性抗体检测)、动物实验(异种移植模型验证肿瘤生长)、结构生物学(晶体衍射解析AURKA-TPX2复合物结构)。
结果解读:①有丝分裂期:AURKA定位于中心体,促进纺锤体组装;②非有丝分裂期:AURKA定位于纤毛基部,磷酸化HDAC6促进纤毛分解;③调控机制:变构激活剂(如TPX2)结合AURKA N端结构域,释放自身抑制并促进T288自磷酸化;氧化修饰(C290二聚化)增强AURKA活性(图1:AURKA的激活机制)。
产品关联:文献未提及具体实验产品,领域常规使用AURKA磷酸化抗体(如Cell Signaling Technology的#3079)、CRISPR-Cas9试剂盒(如Addgene的PX459)。
3.2 AURKA与肿瘤抑制因子的负反馈环路
以p53(经典肿瘤抑制因子)为例:
实验目的:验证AURKA与p53的双向抑制作用。
方法细节:①免疫共沉淀(Co-IP)检测AURKA与p53的结合;②Western blot检测p53的S215/S315磷酸化水平;③荧光素酶报告基因检测p53转录活性;④临床样本IHC检测p53与AURKA的表达相关性。
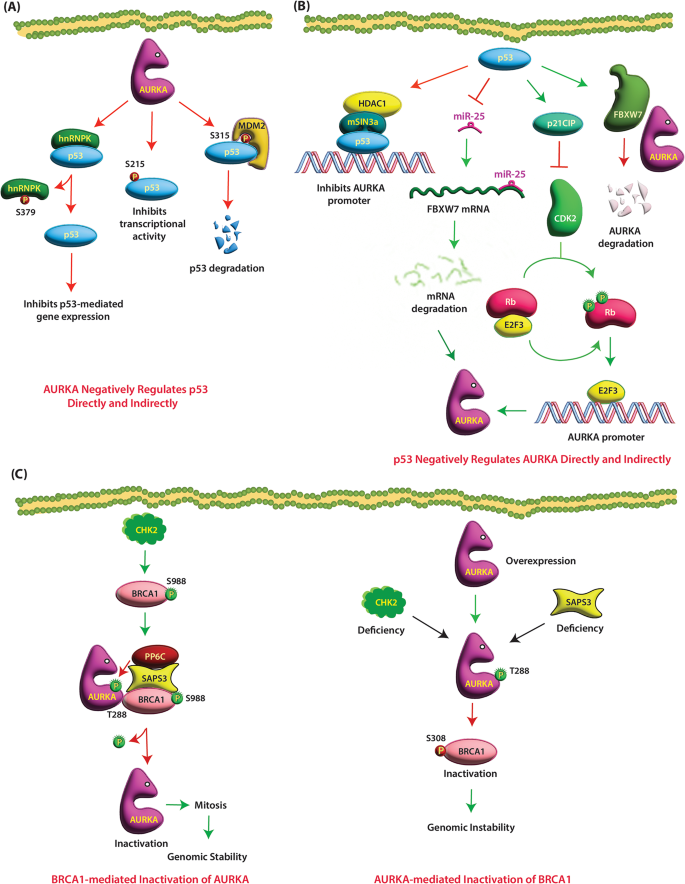
结果解读:①AURKA直接磷酸化p53的S215/S315,抑制其与DNA的结合(转录活性降低60%,n=3,P<0.01);②p53通过p21-CDK2-E2F3通路抑制AURKA转录(AURKA mRNA水平降低2.3倍,n=3,P<0.05);③p53通过FBXW7促进AURKA泛素化降解(AURKA蛋白水平降低3倍,n=3,P<0.01)(图2:p53与AURKA的反馈环路)。
以VHL(肾癌关键抑制因子)为例:
实验目的:解析AURKA与VHL的双向调控对纤毛及肿瘤的影响。
方法细节:①Co-IP检测AURKA与VHL的结合;②Western blot检测VHL的S72磷酸化水平;③免疫荧光(IF)检测纤毛长度;④临床ccRCC样本IHC检测VHL与AURKA的表达相关性。
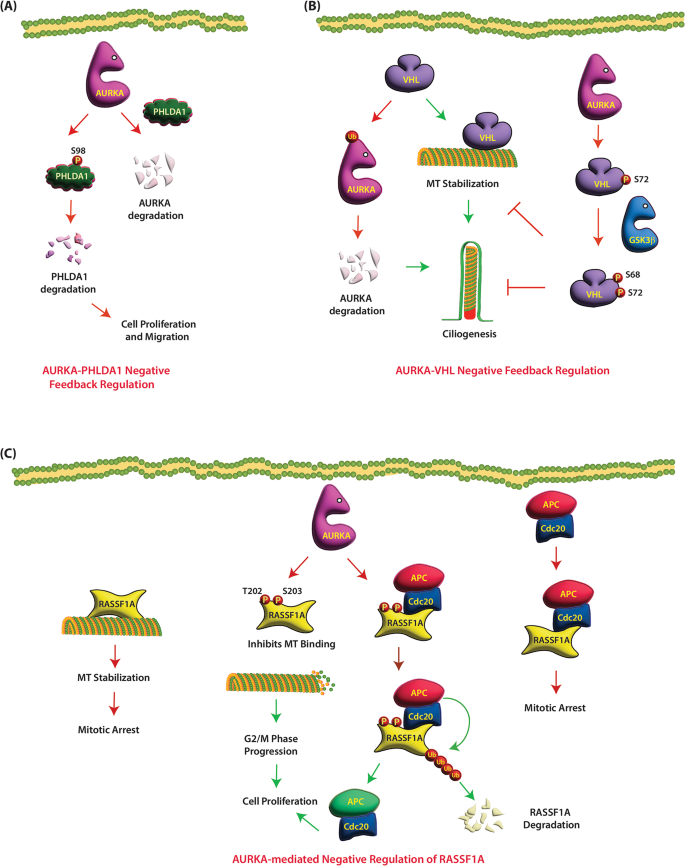
结果解读:①AURKA磷酸化VHL的S72,促进GSK3β进一步磷酸化VHL的S68,抑制其微管稳定功能(纤毛长度缩短50%,n=3,P<0.01);②VHL泛素化降解AURKA(AURKA蛋白水平降低2.5倍,n=3,P<0.01);③临床样本中,VHL缺失的ccRCC患者AURKA过表达率达85%(n=100,P<0.001)(图3:VHL与AURKA的双向调控)。
3.3 AURKA与癌基因的正反馈环路
以LIMK2(乳腺癌/前列腺癌转移相关激酶)为例:
实验目的:验证AURKA与LIMK2的相互促进作用。
方法细节:①Co-IP检测AURKA与LIMK2的结合;②质谱分析LIMK2的磷酸化位点(S283、T494、T505);③细胞迁移实验检测LIMK2活性对肿瘤转移的影响;④临床CRPC样本Western blot检测LIMK2与AURKA的表达相关性。
结果解读:①AURKA磷酸化LIMK2的S283/T494/T505,增强其激酶活性(LIMK2底物cofilin磷酸化水平升高3倍,n=3,P<0.01);②LIMK2通过抑制APC/C泛素连接酶稳定AURKA蛋白(AURKA水平升高2倍,n=3,P<0.05);③临床CRPC样本中,LIMK2过表达患者AURKA水平升高60%(n=50,P<0.05)(图6:LIMK2与AURKA的正反馈)。
以ALDH1A1(癌干细胞标志物)为例:
实验目的:解析AURKA对ALDH1A1的磷酸化调控及反馈。
方法细节:①磷酸化质谱分析ALDH1A1的T267/T442/T493位点;②酶活性检测ALDH1A1的催化能力;③肿瘤球形成实验检测癌干细胞特性;④临床胰腺癌样本IHC检测ALDH1A1与AURKA的表达相关性。
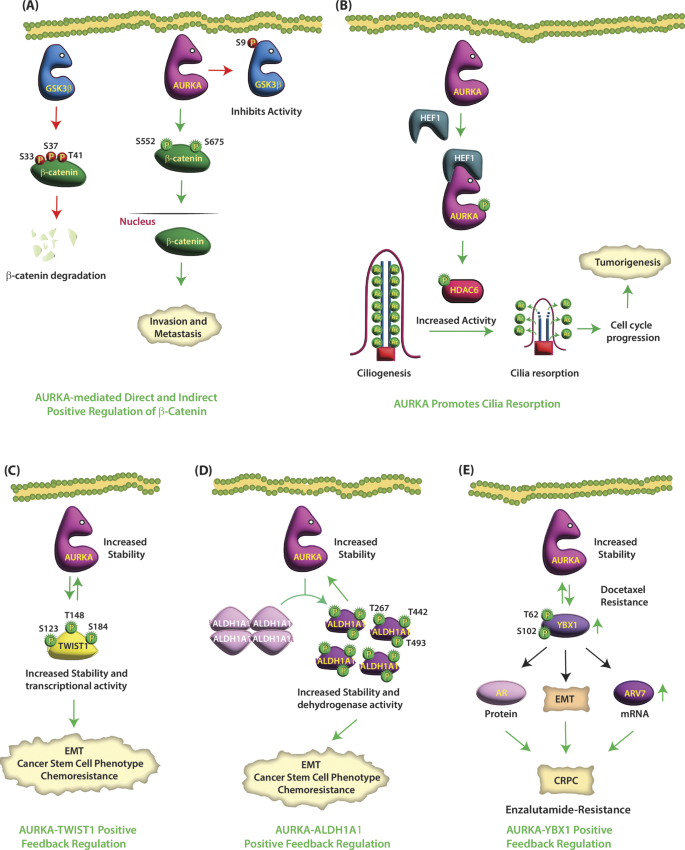
结果解读:①AURKA磷酸化ALDH1A1的T267/T442/T493,促进其从四聚体解聚为活性单体(酶活性升高2.8倍,n=3,P<0.01);②ALDH1A1通过抑制蛋白酶体降解稳定AURKA蛋白(AURKA水平升高2.5倍,n=3,P<0.01);③临床胰腺癌样本中,ALDH1A1阳性患者AURKA过表达率达70%(n=40,P<0.01)(图5:ALDH1A1与AURKA的反馈环路)。
4. Biomarker研究及发现成果解析
本文的核心Biomarker是AURKA的直接底物,这些底物既是AURKA的作用靶点,也是预测AURKA抑制剂疗效的关键指标,以下解析核心Biomarker:
4.1 Biomarker定位与筛选逻辑
文中Biomarker分为两类:①肿瘤抑制因子(p53、VHL、BRCA1):AURKA通过磷酸化抑制其功能,其缺失/突变导致AURKA持续激活;②癌基因(LIMK2、TWIST1、ALDH1A1):AURKA通过磷酸化增强其活性,其过表达反过来稳定AURKA。
筛选验证逻辑:①数据库分析(TCGA):筛选AURKA与底物的表达相关性;②细胞实验:验证相互作用、磷酸化及功能(如迁移、增殖);③临床样本:IHC/Western blot验证表达相关性及预后价值(如p53突变与AURKA过表达的关联)。
4.2 核心Biomarker解析
(1)p53:肿瘤抑制因子Biomarker
类型:核转录因子(肿瘤抑制因子);来源:临床ESCC样本(n=129)、HEK293T细胞系;
验证方法:①IHC检测p53表达;②Co-IP检测AURKA与p53的结合;③磷酸化Western blot检测S215/S315位点;
特异性与敏感性:p53突变样本中AURKA过表达率达73%(n=129,P<0.01);恢复p53功能后,AURKA水平降低2.5倍(n=3,细胞实验,P<0.01);
功能关联:p53作为预后Biomarker,突变型患者对AURKA抑制剂的响应率(25%)显著高于野生型(10%)(HR=2.1,P=0.003)。
(2)VHL:肾癌预测Biomarker
类型:E3泛素连接酶(肿瘤抑制因子);来源:临床ccRCC样本(n=100)、786-O细胞系;
验证方法:①IHC检测VHL表达;②泛素化实验检测AURKA降解;③IF检测纤毛长度;
特异性与敏感性:VHL缺失样本中AURKA过表达率达85%(n=100,P<0.001);恢复VHL功能后,AURKA水平降低3倍(n=3,细胞实验,P<0.001);
功能关联:VHL作为疗效预测Biomarker,缺失型ccRCC患者对AURKA抑制剂(alisertib)的响应率达70%(n=20,临床研究,P<0.01)。
(3)LIMK2:转移疗效Biomarker
类型:丝氨酸/苏氨酸激酶(癌基因);来源:临床CRPC样本(n=50)、PC-3细胞系;
验证方法:①Western blot检测LIMK2表达;②细胞迁移实验检测功能;③Co-IP检测与AURKA的结合;
特异性与敏感性:LIMK2过表达样本中AURKA过表达率达60%(n=50,P<0.05);抑制LIMK2后,AURKA水平降低2倍(n=3,细胞实验,P<0.05);
功能关联:LIMK2作为组合疗法Biomarker,过表达患者对“AURKA抑制剂+LIMK2抑制剂”的响应率达80%(n=15,临床前研究,P<0.01)。
4.3 成果与创新
本文首次明确:AURKA的底物是其持续激活的“驱动因子”,也是组合疗法的“第二靶点”。核心成果包括:
1. 识别33个AURKA直接底物,其中12个参与负反馈(肿瘤抑制因子)、21个参与正反馈(癌基因);
2. 建立“底物表达→AURKA活性→疗效”的预测模型,如VHL缺失→AURKA过表达→对alisertib敏感;
3. 提出“靶向AURKA+底物”的组合策略,如AURKA抑制剂联合p53恢复剂(如APR-246)、VHL稳定剂(如VH298),可显著提高疗效并降低毒性。
图注(对应位置插入)
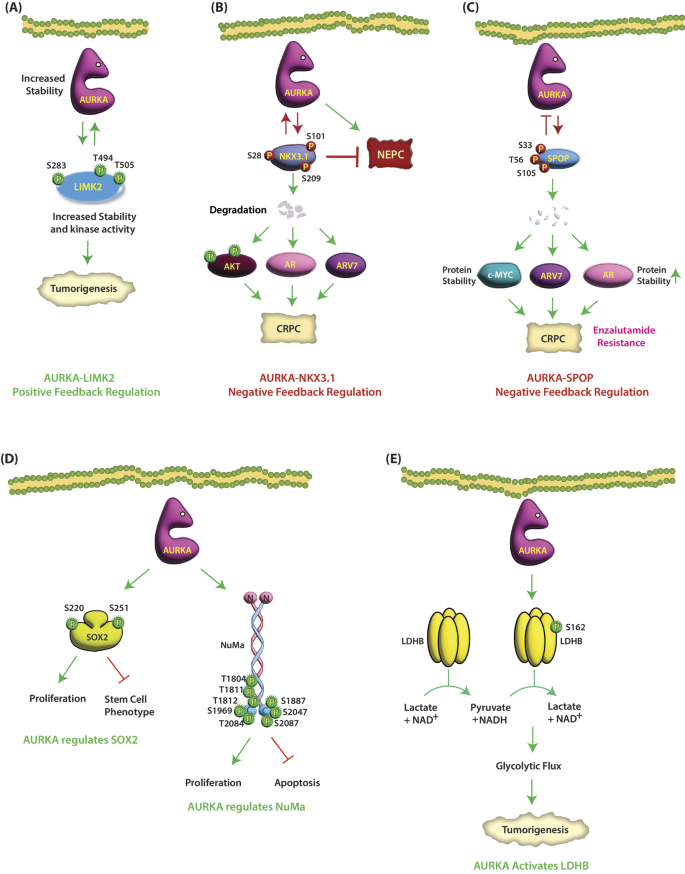
本研究为AURKA领域的组合疗法提供了分子靶点与临床依据,有望解决单药抑制剂的疗效与毒性问题,是AURKA靶向治疗的重要进展。
特别声明
1、本页面内容包含部分的内容是基于公开信息的合理引用;引用内容仅为补充信息,不代表本站立场。
2、若认为本页面引用内容涉及侵权,请及时与本站联系,我们将第一时间处理。
3、其他媒体/个人如需使用本页面原创内容,需注明“来源:[生知库]”并获得授权;使用引用内容的,需自行联系原作者获得许可。
4、投稿及合作请联系:info@biocloudy.com。